Иммунитет чем повысить взрослому человеку: Здоровое питание – меню на каждый день, полезные советы от Amway
принцип их действия, как принимать
18 декабря 2019
Мы живём в удивительное время: каждый может получить доступ к знаниям не выходя из дома. Однако наш мозг и память не всегда способны справиться с крупными объёмами информации. Как следствие – переутомление, нарушения сна, головная боль, нервные расстройства. Можно ли улучшить работу мозга, если попить растительные препараты и не прибегать к серьёзным лекарствам? Читайте обзор популярных средств на основе экстрактов растений и советы Амвэй по их применению.
Какие препараты улучшают память и работу мозга
Фактически, есть смысл говорить не о конкретных торговых марках препаратов, а о главных действующих веществах в их составе. Что немаловажно, самые популярные из них известны человеку в течение долгих веков – некоторые даже тысячелетиями – и досконально изучены.
Женьшень (Panax ginseng, Panax quinquefolius)
Корень женьшеня используется в традиционной китайской медицине с древних времен. Имеет широкий спектр действия – от противовоспалительного до иммуностимулирующего. В том числе женьшень широко применяют для усиления мозговой активности.
Сегодня экологическая обстановка в Китае, где культивируется женьшень, оставляет желать лучшего. Поэтому при производстве препаратов Panax ginseng всё чаще заменяют на родственный вид Panax quinquefolius, который произрастает в Северной Америке и обладает такими же полезными свойствами.
Родиола розовая (Rhodiola rosea)
Это известный природный адаптоген – то есть вещество, помогающее организму приспособиться к внешним воздействиям. Родиола повышает сопротивляемость стрессам различной природы – как физиологическим, так и психологическим. Стимулируя синапсы нервной системы, она снимает усталость и благотворно влияет на когнитивные функции – внимание, восприятие, память, речь и др.
Клинические испытания на медицинском факультете Пенсильванского университета в Филадельфии доказали 1, что лекарства на основе родиолы эффективны при депрессии. А сотрудники Лёвенского католического университета в Бельгии выяснили 2, что здоровым людям экстракт родиолы помогает работать продуктивнее.
А сотрудники Лёвенского католического университета в Бельгии выяснили 2, что здоровым людям экстракт родиолы помогает работать продуктивнее.
Бакопа (Bacopa monnieri)
Ещё одно растение, чьи свойства люди с древности используют в медицине в данном случае аюрведической. Его особенность в двойном эффекте. Усиливая концентрацию и внимательность, бакопа параллельно с этим уменьшает реакцию организма на стресс. Это происходит благодаря балансировке химических веществ мозга. Повышается концентрация гормонов радости дофамина и серотонина с одновременным снижением уровня гормона стресса кортизола.
Согласно исследованиям 3, проведённым в Орегонском исследовательском центре по неврологическим расстройствам, лекарственные препараты на основе бакопы особенно полезно принимать пожилым людям. Экстракт этого растения обладает высоким потенциалом для безопасного улучшения когнитивных функций при старении.
Гинкго (Ginkgo)
Это необычное дерево, которое произрастает на нашей планете уже десятки миллионов лет. Поражающее воображение долгожительство сделало гинкго одной из самых популярных растительных добавок в мире. Считается, что его экстракт способен оказывать благотворное влияние на мозг и даже замедлять развитие старческой деменции.
Однако попытки проверить эти утверждения на практике дают противоречивые результаты. Лишь в некоторых случаях наблюдается 4 выраженный эффект от приема препарата, а говорить о системе результаты экспериментов не позволяют. Поэтому современная доказательная медицина ставит действенность добавок на основе гинкго под сомнение.
Цистанхе трубчатая (Cistanchetubulosa)
Пустынное растение, широко применяющееся в народной медицине Китая и Средней Азии. Одно из важных свойств добавок на основе корня цистанхе – способность оптимизировать давление в кровеносных сосудах. Этот процесс способствует активному питанию мозга. Ученые из компании Sinphar и научно-исследовательского центра компании Amway выяснили, что экстракт цистанхе улучшает процессы запоминания и концентрации внимания у здоровых людей. Препарат NUTRILITE™ Память плюс в форме таблеток на основе корня цистанхе рекомендован всем, кто хочет развить свою память и умственную работоспособность.
Препарат NUTRILITE™ Память плюс в форме таблеток на основе корня цистанхе рекомендован всем, кто хочет развить свою память и умственную работоспособность.
Принцип действия препаратов для улучшения памяти и работы мозга
Существует ряд механизмов, обуславливающих эффективность природных средств для улучшения памяти и работы мозга. Как правило, экстракты растений воздействуют на организм сразу несколькими способами.
- Улучшают кровообращение, в том числе в мозге – а значит, снабжение его кислородом.
- Усиливают действие нейротрансмиттеров, передающих импульсы между нейронами.
- Препятствуют повреждению клеток мозга свободными радикалами, а также защищают клетки от токсинов.
- Стимулируют регенерацию мозговых клеток.
- Поставляют в мозг необходимые питательные вещества и витамины, которых не хватает в рационе.
- Повышают нейропластичность – способность мозга изменяться и формировать новые связи взамен утраченных.
- Увеличивают стрессоустойчивость.
В каких случаях можно принимать препараты для улучшения работы мозга
Растительные ноотропные препараты показаны в следующих случаях.
- Людям, чья деятельность связана с постоянными интеллектуальными нагрузками.
- Тем, кто подвержен частым ОРВИ.
- Людям, которые употребляют много алкоголя.
- При переутомлениях и стрессах.
- При сезонном гиповитаминозе.
- Для устранения последствий черепно-мозговых травм.
Как правило, для достижения оптимального результата препараты, улучшающие память и работу мозга, необходимо пропить курсом. БАД NUTRILITE™ Память плюс рекомендуется пить взрослым в течение месяца по 1 таблетке 2 раза в день во время еды. При необходимости лечение повторяют.
Узнайте также:
1 Mao J.J., Xie S.X., Zee J., Soeller I., Li Q.S., Rockwell K., Amsterdam J.D. Rhodiola rosea versus sertraline for major depressive disorder: A randomized placebo-controlled trial. // Phytomedicine. 2015. №22 (3). С. 394-9.
// Phytomedicine. 2015. №22 (3). С. 394-9.
2 De Bock K., Eijnde B.O., Ramaekers M., Hespel P. Acute Rhodiola rosea intake can improve endurance exercise performance. // International Journal of Sport Nutrition and Exercise Metabolism. 2004. №14 (3). С. 298-307.
3 Carlo Calabrese, William L. Gregory, Michael Leo, Dale Kraemer, Kerry Bone, Barry Oken Effects of a Standardized Bacopa monnieri Extract on Cognitive Performance, Anxiety, and Depression in the Elderly: A Randomized, Double-Blind, Placebo-Controlled Trial // Journal of Alternative and Complementary Medicine. 2008. №14 (6). С. 707–713.
4 Ginkgo biloba for cognitive impairment and dementia // Cochrane Database (янв. 2009).
состав, инструкция, цена на официальном сайте Amway
Базовый комплекс незаменимых витаминов и минералов, дополненный растительными концентратами NUTRILITE™. Восстановит ежедневный уровень необходимых полезных веществ в организме. Упаковки на 30 таблеток хватит на один рекомендованный месяц приема.
Ежедневная защита
150мкг*
Cуточная норма
для взрослого человека
NUTRILITE™ Дэйли
140 мкг йода
93 % суточной нормы
100г ГОРБУШИ**
50 мкг йода
33% суточной нормы
Содержит фитонутриенты
Подходит для диабетиков (содержание углеводов и калорий несущественно)***
Без глютена, красителей и консервантов
Заполнит пробелы рациона
* Согласно Единым санитарным требованиям Таможенного союза.
** По данным исследований, проведенных компанией Amway.
*** По согласованию с врачом.
ПРОТИВОПОКАЗАНИЯ
Имеются противопоказания. Перед применением проконсультируйтесь с врачом. БАД является дополнительным источником питательных веществ. БАД не является заменителем пищи.
Срок годности: 2 года.
Страна происхождения: США.
Подходящие вам БАДы и витаминами вы можете выбрать в нашем каталоге.
БАДы NUTRILITE™ НЕ ЯВЛЯЮТСЯ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ПРОКОНСУЛЬТИРУЙТЕСЬ С ВРАЧОМ
БАДы NUTRILITE™ предназначены только для личного использования. Любые иные способы использования и реализации БАД допускаются исключительно в случаях и при соблюдении требований, предусмотренных действующим законодательством РФ. БАДы NUTRILITE™ можно приобрести в Торговых центрах компании ООО «Амвэй». Адреса Торговых центров, а также наличие продукции можно уточнить на сайте www.amway.ru или позвонив по телефону +7 (495) 981-4000. Продукция прошла регистрацию в Роспотребнадзоре в рамках таможенного союза. Вся продукция соответствует требованиям ТР ТС 021/2011 «О безопасности пищевой продукции»; ТР ТС 022/2011 «Пищевая продукция в части ее маркировки».
* По согласованию с врачом.
ДЕЙСТВИЕ ИНГРЕДИЕНТОВ
Натуральные концентраты
NUTRILITE™ в составе продукта
вишня ацерола,
люцерна,
морковь,
петрушка,
шпинат,
NUTRILITE™ Дэйли ежедневно обеспечивает организм широким набором питательных веществ в сбалансированном виде.
Рекомендации по применению:
Взрослым принимать внутрь по одной таблетке один раз в день во время приёма пищи.
Продолжительность приема:
Один месяц.
| Ингредиент | Содержание в 1 таблетке | % от рекомендуемого суточного потребления |
|---|---|---|
| Биотин | 100 мкг | 200 %* |
| Пантотеновая кислота | 9 мг | 150 %* |
| Фолиевая кислота | 200 мкг | 100 % |
| Ниацин (ниацинамид) | 20 мг | 111 %* |
| Витамин Е (сукцинат) | 10 мг | 100 % |
| Витамин B2 (рибофлавин) | 1,8 мг | 113 %* |
| Витамин В1 (тиамина мононитрат) | 1,2 мг | 86 % |
| Витамин В6 (пиридоксин гидрохлорид) | 1,4 мг | 70 % |
| Витамин В12 | 2 мкг | 200 %* |
| Витамин C (аскорбиновая кислота) | 45 мг | 75 % |
| Витамин D3 | 2,5 мкг (100 ME) | 50 % |
| Бета-каротин | 2,1 мг | 42 %** |
| Витамин A (пальмитат) | 350 мкг | 44 % |
| Марганец (сульфат) | 4 мг | 200 %*(**) |
| Медь (глюконат) | 1,6 мг | 160 %*(**) |
| Цинк (оксид) | 18 мг | 120 %* |
| Йод (йодид калия, келп) | 140 мкг | 93 % |
| Железо (фумарат) | 10 мг | 71 % |
| Магний (оксид) | 109 мг | 27 % |
| Кальций (карбонат) | 265 мг | 26,5 % |
| Фосфор (фосфат кальция) | 115 мг | 14,4 % |
Ингредиент
Биотин
Содержание в 1 таблетке
100 мкг
% от рекомендуемого суточного потребления
200 %*
Пантотеновая кислота
Содержание в 1 таблетке
9 мг
% от рекомендуемого суточного потребления
150 %*
Фолиевая кислота
Содержание в 1 таблетке
200 мкг
% от рекомендуемого суточного потребления
100 %
Ниацин (ниацинамид)
Содержание в 1 таблетке
20 мг
% от рекомендуемого суточного потребления
111 %*
Витамин Е (сукцинат)
Содержание в 1 таблетке
10 мг
% от рекомендуемого суточного потребления
100 %
Витамин В2
(рибофлавин)
Содержание в 1 таблетке
1,8 мг
% от рекомендуемого суточного потребления
113 %*
Витамин В1
(тиамина мононитрат)
Содержание в 1 таблетке
1,2 мг
% от рекомендуемого суточного потребления
86 %
Витамин В6
(пиридоксин гидрохлорид)
Содержание в 1 таблетке
1,4 мг
% от рекомендуемого суточного потребления
70 %
Витамин В12
Содержание в 1 таблетке
2 мкг
% от рекомендуемого суточного потребления
200 %*
Витамин C
(аскорбиновая кислота)
Содержание в 1 таблетке
45 мг
% от рекомендуемого суточного потребления
75 %
Витамин D3
Содержание в 1 таблетке
2,5 мкг (100 ME)
% от рекомендуемого суточного потребления
50 %
Бета-каротин
Содержание в 1 таблетке
2,1 мг
% от рекомендуемого суточного потребления
42 %**
Витамин A
(пальмитат)
Содержание в 1 таблетке
350 мкг
% от рекомендуемого суточного потребления
44 %
Марганец (сульфат)
Содержание в 1 таблетке
4 мг
% от рекомендуемого суточного потребления
200 %*(**)
Медь (глюконат)
Содержание в 1 таблетке
1,6 мг
% от рекомендуемого суточного потребления
160 %*(**)
Цинк (оксид)
Содержание в 1 таблетке
18 мг
% от рекомендуемого суточного потребления
120 %*
Йод (йодид калия, келп)
Содержание в 1 таблетке
140 мкг
% от рекомендуемого суточного потребления
93 %
Железо (фумарат)
Содержание в 1 таблетке
10 мг
% от рекомендуемого суточного потребления
71 %
Магний (оксид)
Содержание в 1 таблетке
109 мг
% от рекомендуемого суточного потребления
27 %
Кальций (карбонат)
Содержание в 1 таблетке
265 мг
% от рекомендуемого суточного потребления
26,5 %
Фосфор (фосфат кальция)
Содержание в 1 таблетке
115 мг
% от рекомендуемого суточного потребления
14,4 %
* — не превышает верхний допустимый суточный уровень потребления.
** — согласно Единым санитарно-эпидемиологическим и гигиеническим требованиям к товарам, подлежащим санитарно-эпидемиологическому надзору (контролю).
| Пищевая ценность 1 таблетки | ||
|---|---|---|
| Белки | 0,056 гр. | |
| Углеводы | 0,328 гр. | |
| Жиры | 0,025 гр. | |
| Энергетическая ценность | 7,5 кДж/1,8 ккал | |
СОСТАВ:
ФОСФАТ ДИКАЛЬЦИЯ, ФОСФАТ ТРИКАЛЬЦИЯ, КАРБОНАТ КАЛЬЦИЯ, ОКСИД МАГНИЯ, КОНЦЕНТРАТ ЛЮЦЕРНЫ (MEDICAGO SATIVA), ВИТАМИН С (АСКОРБИНОВАЯ КИСЛОТА), ФУМАРАТ ЖЕЛЕЗА, КУКУРУЗНЫЙ КРАХМАЛ, ОКСИД ЦИНКА, ВИТАМИН В3 (НИАЦИНАМИД), СТАБИЛИЗАТОР: КРОСКАРАМЕЛЛОЗА; СТАБИЛИЗАТОР: МИКРОКРИСТАЛЛИЧЕСКАЯ ЦЕЛЛЮЛОЗА; ВИТАМИН Е (D-АЛЬФА-ТОКОФЕРОЛА СУКЦИНАТ), АНТИСЛЕЖИВАЮЩИЙ АГЕНТ: СТЕАРИНОВАЯ КИСЛОТА; СУЛЬФАТ МАРГАНЦА, ГЛЮКОНАТ МЕДИ, КАЛЬЦИЙ ПАНТОТЕНАТ, СТАБИЛИЗАТОР: ГИДРОКСИПРОПИЛМЕТИЛЦЕЛЛЮЛОЗА; ДРОЖЖИ, МАЛЬТОДЕКСТРИН, ПОРОШОК БУРОЙ ВОДОРОСЛИ (ASCOPHYLLIUM NODOSUM, LAMINARIA DIGITATA), БЕТА-КАРОТИН, ВИТАМИН B2 (РИБОФЛАВИН), ВИТАМИН В6 (ПИРИДОКСИНА ГИДРОХЛОРИД), ВИТАМИН B1 (ТИАМИНА МОНОНИТРАТ), КОНЦЕНТРАТ АЦЕРОЛЫ (MALPIGHIA EMARGINATA, MALPIGHIA GLABRA), ПОРОШОК ШПИНАТА (SPINACIA OLERACEA), ЭЛЕКТРОЛИТНОЕ ЖЕЛЕЗО, САХАРОЗА, ВЛАГОУДЕРЖИВАЮЩИЙ АГЕНТ: ГЛИЦЕРИН; АНТИОКИСЛИТЕЛЬ: СМЕСЬ ТОКОФЕРОЛОВ; ВИТАМИН A (РЕТИНИЛ АЦЕТАТ), КОНЦЕНТРАТ ПЕТРУШКИ (PETROSELINUM CRISPUM), ПОРОШОК МОРКОВИ (DАUCUS CAROTA), ФОЛИЕВАЯ КИСЛОТА, ЙОДИД КАЛИЯ, БИОТИН, КОНЦЕНТРАТ КРЕССА ВОДЯНОГО (NASTURTIUM OFFICINALE), ГЛАЗИРОВАТЕЛЬ: КАРНАУБСКИЙ ВОСК; ВИТАМИН D3 (ХОЛЕКАЛЬЦИФЕРОЛ), ВИТАМИН В12 (ЦИАНОКОБАЛАМИН).
Способ применения
Взрослым: принимать внутрь по 1 таблетке в день во время еды в течение месяца.
Как повысить иммунитет у взрослого человека
Повышение вашей иммунной системы — это залог хорошего здоровья каждого человека. Рассмотрим несколько ключевых особенностей, которые оказывают влияние на ваш иммунитет. Климатические перемены. Изменения погоды осенью, холодные температуры, повышенная влажность становятся первопричиной насморка и простудных заболеваний. Такие условия заставляют большинство из нас испытать поток простуд и гриппа, который приходит и уходит в холодное время года. Есть ли простой способ укрепить вашу иммунную систему, чтобы реже подвергаться воздействию вирусных инфекций?
Рассмотрим несколько ключевых особенностей, которые оказывают влияние на ваш иммунитет. Климатические перемены. Изменения погоды осенью, холодные температуры, повышенная влажность становятся первопричиной насморка и простудных заболеваний. Такие условия заставляют большинство из нас испытать поток простуд и гриппа, который приходит и уходит в холодное время года. Есть ли простой способ укрепить вашу иммунную систему, чтобы реже подвергаться воздействию вирусных инфекций?
Мы все обладаем врожденной способностью защищать себя от болезней. И эта удивительная система профилактики заболеваний — иммунная система человека. Функция иммунной системы человека — защищать организм от вредных бактерий. Микробы и микроорганизмы, раковые клетки и трансплантированные ткани или органы — все это интерпретируется здоровой иммунной системой как нечто отличное от привычной структуры иммунитета каждого отдельного человека, от которого организм должен защищаться. Хотя иммунная система чрезвычайно сложна, ее основная стратегия довольно симплементарна — распознать атакующую инфекцию, мобилизовать силы и атаковать.
Сильный иммунитет — это первая линия защиты от простуды, гриппа и множества других вирусных и бактериальных микробов. Поскольку профилактика лучше лечения, она способствует иммунной системе за всесторонней помощью.
Злоупотребление фармацевтическими препаратами и отсутствие слабая информированность населения о укреплении иммунитета взрослого человека сделали уровень эффективности иммунной системы среднестатистического украинца в лучшем случае на уровне 40% или 50% осведомленности. В некоторых странах, например в Японии, существует традиционная диета, которая укрепляет иммунную систему, и поэтому японцы (которые придерживаются традиционной диеты) обычно живут дольше. Не случайно, что японские женщины являются одними из самых долгоживущих людей на планете.
Исследования укрепления иммунной системы
Поскольку наша клиника специализируется на профессиональных методиках лечения, мы бы хотели поделиться несколькими простыми рекомендациями по укреплению здоровья и ведении здорового образа жизни. Адекватное питание вашей иммунной системы повышает ее боевую мощь. Иммуностимуляторы работают во многих отношениях. Они увеличивают количество белых клеток иммунной системы и помогают устоять перед вирусной атакой. Бустеры также помогают устранить сухостой иммунитета, устраняют вероятность инфекцирования организма.
Адекватное питание вашей иммунной системы повышает ее боевую мощь. Иммуностимуляторы работают во многих отношениях. Они увеличивают количество белых клеток иммунной системы и помогают устоять перед вирусной атакой. Бустеры также помогают устранить сухостой иммунитета, устраняют вероятность инфекцирования организма.
На сегодня существует бесчисленное множество пищевых добавок, которые со слов специалистов, участвуют в поддержке и укреплении здоровой иммунной системы.
По оценкам, всего 20% взрослого населения Украины регулярно употребляют пищевые добавки и тратят на них до 1,3 миллиарда гривен ежегодно. Около половины этих людей принимают комбинацию витаминов и минеральных продуктов.
Большая часть исследований витаминно-минеральных добавок была связана с их влиянием на иммунитет и инфекционные заболевания. Известно, что различные степени недоедания, даже малое недополучение отдельных микроэлементов заметно ухудшают иммунную функцию. Степень, в которой тонкий дефицит различных позных веществ способствует клинически значимым инфекциям, не просчитана на сегодняшний день.
Несколько исследований, проведенных МОЗ Украины, показывают, что витаминные добавки могут улучшать различные иммунологические факторы. Тем не менее, другие исследования частных компаний продемонстрировали ослабленный иммунологический ответ у участников, которые потребляли больше, чем рекомендованное количество определенных пищевых добавок.
Если у взрослого человека дефицит иммунной системы или врожденная ослабленная иммунная система, необходимо проконсультироваться с врачом, прежде чем заниматься укреплением иммунитета без контроля профессионального врача-иммунолога. Также имейте в виду, что термин «повышение уровня иммунной системы» не является научным термином. Она невероятно сложна и в то время как некоторые ее аспекты могут быть усилены определенными биологически активными добавками, другой аспект может пострадать. Это чрезвычайно сложная тема.
Способы улучшения иммунитета взрослого человека
Глубокий сон — один из важнейших способов укрепления иммунной системы. Хроническая бессонница может привести к дефициту иммунной системы. Отличный способ убедиться в том, что у вас будет здоровый и глубокий сон — это совершать длительные прогулки перед сном ежедневно. Сон связан со сбалансированным уровнем гормонов (включая гормон роста человека и гормон стресса, кортизол), снижением веса, ясным мышлением и рассуждениями, улучшением настроения и здоровой кожей.
Хроническая бессонница может привести к дефициту иммунной системы. Отличный способ убедиться в том, что у вас будет здоровый и глубокий сон — это совершать длительные прогулки перед сном ежедневно. Сон связан со сбалансированным уровнем гормонов (включая гормон роста человека и гормон стресса, кортизол), снижением веса, ясным мышлением и рассуждениями, улучшением настроения и здоровой кожей.
Снижайте уровень стресса — один из лучших способов ухудшить вашу иммунную систему и тем самым подвергнуть себя риску заболеваний. Точно так же негативные эмоции, такие как беспокойство и гнев, оказывают отрицательное влияние. Как и следовало ожидать, один хороший способ укрепить вашу иммунную систему, а также улучшить общее качество вашей жизни — это устранять негативные эмоции по мере возникновения. Стресс любого рода — эмоциональный, физический или психологический — высвобождает гормон кортизол и повреждает иммунную систему.
Ешьте больше фруктов и овощей. Они содержат флавоноиды, которые обладают антибактериальной и противовирусной активностью. Избегайте чрезмерного потребления сахара. Потребляйте больше чеснока, лука и кулинарных трав, таких как гвоздика. Ягоды являются богатыми источниками биологически активных соединений, таких как фенольные и органические кислоты, которые обладают противомикробной активностью против патогенов человека. Среди разных ягод и ягодных фенолов особенно отчетливо проявляется антимикробный эффект в таких продуктах питания, как: клюква, морошка, малина, клубника и черника.
Прогнозируйте получения здоровых пробиотических бактерий. Пробиотики были определены как живые микроорганизмы, которые (при попадании в организм) оказывают благотворное влияние на профилактику и лечение определенных заболеваний. Считается, что эти микроорганизмы оказывают биологическое воздействие через явление, известное как устойчивость к колонизации, при котором местная анаэробная флора ограничивает концентрацию потенциально вредных микробов в пищеварительном тракте. Было также исследовано, что пробиотики полезны для снижения шансов простудиться или заболеть гриппом. Эти дружественные кишечные бактерии могут также укрепить иммунную систему взрослого человека.
Было также исследовано, что пробиотики полезны для снижения шансов простудиться или заболеть гриппом. Эти дружественные кишечные бактерии могут также укрепить иммунную систему взрослого человека.
Предоставляя вашему организму достаточное количество питательных веществ, необходимых ему для нормального функционирования, иммунная система взрослого человека будет лучше подготовлена к борьбе с болезнями, будь то простуда, грипп или что-то более серьезное. Поскольку каждый организм индивидуален, старайтесь не подвергать свое здоровье опасности и своевременно консультируйтесь с врачом-иммунологом онкологического предопухолевого центра «Молекула» перед началом любого режима приема добавок.
как укрепить иммунитет взрослому человеку в домашних
Тэги: понижение иммунитета, купить как укрепить иммунитет взрослому человеку в домашних, какао повышает иммунитет.
как пить эхинацею для поднятия иммунитета, что нужно сделать чтобы укрепить иммунитет, укрепляет ли баня иммунитет, гвоздика поднимает иммунитет, аптечные средства для иммунитета взрослым
Принцип действия
Особенность капель Immunity (перевод с англ. immunity — иммунитет, невосприимчивость) заключается в том, что в составе средства комбинация из 18 лекарственных растений с целебными свойствами, которые дополняет комплекс из 6 витаминов, необходимых человеку для повышения иммунитета. Они выпускаются в виде комплексного средства с иммуномодулирующим действием на основе лекарственных трав. Принимая этот раствор, цена которого варьируется в доступных пределах, Вы не только сможете укрепить иммунную систему, но и сэкономить на приобретении других противовирусных препаратов.
Официальный сайт как укрепить иммунитет взрослому человеку в домашних
Состав
Как повысить иммунитет взрослому человеку – 10 советов с научным обоснованием. Описанные советы не требуют посещения врача-иммунолога, приема таблеток и почти все из них доступны в домашних условиях. Комсомолка разбиралась как можно поднять иммунитет взрослому человеку. Есть и еще одна сторона профилактики, о которой следует помнить. Когда вокруг все болеют, важно не только укрепить иммунитет, но и уменьшить количество контактов с возбудителями инфекции. Чем меньше бактерий и вирусов попадет. Есть еще один способ, как повысить иммунитет взрослому человеку в домашних условиях при помощи имбиря. Для этого можно натереть 200 г корней и смешать с размолотыми в блендере лимонами (2 шт с кожурой), толченой клюквой (5 ст.л.), инжиром и курагой (по 100г). Соединив и измельчив все, заливаем. О том, как повысить иммунитет, многие люди задумываются после тяжелых. Иммунитет — совокупность защитных механизмов, благодаря которым организм. Лучшие средства для быстрого поднятия иммунитета взрослому в домашних условиях. Узнайте, как поднять иммунитет взрослому человеку в домашних условиях при помощи витаминов и БАДов, а также при. Как поднять иммунитет в домашних условиях. Повысить защитные силы своего организма и укрепить иммунитет можно с помощью: закаливания; физической активности. Хотите узнать, как повысить иммунитет взрослому человеку в домашних условиях?. Присмотритесь к зеленым овощам и некоторым полезным блюдам. Часто ответ на вопрос, как укрепить иммунитет, заключается в правильном, сбалансированном питании. Бульон или суп. Куриный или говяжий (на. Народные средства очень эффективны и будут работать 100% в комплексе со здоровым образом жизни. Иммунная система человека — целый комплекс защитных форм, органов и их функций, которые ставят мощный барьер перед вирусами, инфекциями, бактериями, ядами, грибками и т.д. И поддерживать ее работу. Лучшие народные рецепты для повышения иммунитета врослого человека в домашних условиях без применения таблеток. Как повысить иммунную систему при болезни? Если вы хотите повысить свой иммунитет или укрепить свой иммуните, пока вы больны, вы можете начать с потребления продуктов. Как быстро повысить иммунитет взрослому и ребенку. Здесь вы найдёте лучшие рецепты, подходящие и для взрослого, и для ребенка, в которые включены фрукты, травы, орехи, мёд, домашний живой йогурт, а также рекомендации по повышению иммунитета здоровым образом жизни.
Комсомолка разбиралась как можно поднять иммунитет взрослому человеку. Есть и еще одна сторона профилактики, о которой следует помнить. Когда вокруг все болеют, важно не только укрепить иммунитет, но и уменьшить количество контактов с возбудителями инфекции. Чем меньше бактерий и вирусов попадет. Есть еще один способ, как повысить иммунитет взрослому человеку в домашних условиях при помощи имбиря. Для этого можно натереть 200 г корней и смешать с размолотыми в блендере лимонами (2 шт с кожурой), толченой клюквой (5 ст.л.), инжиром и курагой (по 100г). Соединив и измельчив все, заливаем. О том, как повысить иммунитет, многие люди задумываются после тяжелых. Иммунитет — совокупность защитных механизмов, благодаря которым организм. Лучшие средства для быстрого поднятия иммунитета взрослому в домашних условиях. Узнайте, как поднять иммунитет взрослому человеку в домашних условиях при помощи витаминов и БАДов, а также при. Как поднять иммунитет в домашних условиях. Повысить защитные силы своего организма и укрепить иммунитет можно с помощью: закаливания; физической активности. Хотите узнать, как повысить иммунитет взрослому человеку в домашних условиях?. Присмотритесь к зеленым овощам и некоторым полезным блюдам. Часто ответ на вопрос, как укрепить иммунитет, заключается в правильном, сбалансированном питании. Бульон или суп. Куриный или говяжий (на. Народные средства очень эффективны и будут работать 100% в комплексе со здоровым образом жизни. Иммунная система человека — целый комплекс защитных форм, органов и их функций, которые ставят мощный барьер перед вирусами, инфекциями, бактериями, ядами, грибками и т.д. И поддерживать ее работу. Лучшие народные рецепты для повышения иммунитета врослого человека в домашних условиях без применения таблеток. Как повысить иммунную систему при болезни? Если вы хотите повысить свой иммунитет или укрепить свой иммуните, пока вы больны, вы можете начать с потребления продуктов. Как быстро повысить иммунитет взрослому и ребенку. Здесь вы найдёте лучшие рецепты, подходящие и для взрослого, и для ребенка, в которые включены фрукты, травы, орехи, мёд, домашний живой йогурт, а также рекомендации по повышению иммунитета здоровым образом жизни. 25 лучших рецептов для. В том, как повысить иммунитет взрослому человеку народными средствами и лекарственными препаратами без вреда для. Можно легко укрепить иммунитета в домашних условиях, если правильно питаться: сбалансированный рацион стабилизирует здоровье и без аптечных лекарств, и без настоев.
25 лучших рецептов для. В том, как повысить иммунитет взрослому человеку народными средствами и лекарственными препаратами без вреда для. Можно легко укрепить иммунитета в домашних условиях, если правильно питаться: сбалансированный рацион стабилизирует здоровье и без аптечных лекарств, и без настоев.
Эффект от применения
Давайте возьмем первостольников. Каждый день на вас обрушиваются полчища вирусов и бактерий, но ведь вы в большинстве своем не болеете? Почему? Да потому что ваша иммунная система за годы работы в аптеке укрепилась в борьбе с этими агрессорами. Их действие направлено на то, чтобы аккуратно активировать клетки микрофлоры, отвечающие за защиту организма. Вследствие этого процесса происходит улучшение состояния иммунитета, и организм получает новые силы для борьбы с патогенами. Таким образом, принимающий капли человек с диагнозом ОРВИ, грипп или другое заболевание, может вылечиться всего за 3-5 дней. Те же, кто будет покупать препарат до начала холодов, вовсе смогут избежать вирусных инфекций и воздержаться от больничного.
Мнение специалиста
Они выпускаются в виде комплексного средства с иммуномодулирующим действием на основе лекарственных трав. Принимая этот раствор, цена которого варьируется в доступных пределах, Вы не только сможете укрепить иммунную систему, но и сэкономить на приобретении других противовирусных препаратов.
Иммунитет человека, особенно ребенка должен сам бороться с недугом, развиваться. У каждого свой иммунитет, и работает где-то лучше, где-то хуже. Например у двух детишек в одной семье, с одинаковыми условиями может быть. Как поднять иммунитет ребёнку и сделать его невосприимчивым к заболеваниям?. Именно это является, важнейшим этапом, и очень хорошо, когда вскармливание. Как поднять у ребенка иммунитет эффективными методами. Вы, наверное, не раз замечали, что дети по—разному реагируют. Узнайте на сайте Amway, как повысить слабый иммунитет ребенку, а также чем лучше поднимать иммунитет в домашних условиях после болезни или для профилактики. Что же влияет на иммунитет и как помочь ребенку поднять его? Здоровое сбалансированное питание. Одна из причин. Как повышать иммунитет ребенку. Многие детки подвергаются частым заболеваниям в раннем возрасте. Советы иммунолога как повысить иммунитет ребенку. По вопросам здоровья обязательно консультируются со специалистами. Как ещё можно повысить иммунитет у ребенка народными средствами? Хороший стимулирующий иммунитет эффект есть у. Как поднять иммунитет ребёнку народными средствами в межсезонье. Укрепление иммунитета у детей народными средствами не сводится только к растительной пище вроде. Чтобы поднять иммунитет ребенку, лучше приготовить из клюквы вкусный десерт, который чадо будет расценивать как лакомство, а не как. Кроме того, с молоком матери ребенку передаются антитела, которые повышают иммунитет ребенка. Младенец, находящийся на естественном вскармливании, хорошо. Как укрепить и повысить иммунитет ребенку, который часто болеет. Начинать прокачивать свой иммунитет нужно с самого раннего возраста. Поэтому перед родителями встает вопрос: как поднять иммунитет ребенку. Как повысить иммунитет ребенка, таблетки для укрепления иммунитета. Что дать ребенку для иммунитета. Часто болеющие дети в детском саду и школе. Надо срочно поднять иммунитет ребенку!! Кто сталкивался? может врач есть какой или препараты? про поднятие иммунитета. Как повысить иммунитет ребенку народными средствами в домашних условиях? Как укрепить иммунитет ребенку в 2 года перед садиком и в период адаптации? Укреплять детский организм желательно начинать в теплое время года. Поймите как можно повысить иммунитет своему ребенку в домашних условиях. Чтобы ребенок не так часто болел и хорошо себя чувствовал, родители. Как поднять иммунитет в 4-5 лет. Для ребенка 4-5 лет особенно важно поддерживать иммунную систему, которая повергается регулярным атакам.
Что же влияет на иммунитет и как помочь ребенку поднять его? Здоровое сбалансированное питание. Одна из причин. Как повышать иммунитет ребенку. Многие детки подвергаются частым заболеваниям в раннем возрасте. Советы иммунолога как повысить иммунитет ребенку. По вопросам здоровья обязательно консультируются со специалистами. Как ещё можно повысить иммунитет у ребенка народными средствами? Хороший стимулирующий иммунитет эффект есть у. Как поднять иммунитет ребёнку народными средствами в межсезонье. Укрепление иммунитета у детей народными средствами не сводится только к растительной пище вроде. Чтобы поднять иммунитет ребенку, лучше приготовить из клюквы вкусный десерт, который чадо будет расценивать как лакомство, а не как. Кроме того, с молоком матери ребенку передаются антитела, которые повышают иммунитет ребенка. Младенец, находящийся на естественном вскармливании, хорошо. Как укрепить и повысить иммунитет ребенку, который часто болеет. Начинать прокачивать свой иммунитет нужно с самого раннего возраста. Поэтому перед родителями встает вопрос: как поднять иммунитет ребенку. Как повысить иммунитет ребенка, таблетки для укрепления иммунитета. Что дать ребенку для иммунитета. Часто болеющие дети в детском саду и школе. Надо срочно поднять иммунитет ребенку!! Кто сталкивался? может врач есть какой или препараты? про поднятие иммунитета. Как повысить иммунитет ребенку народными средствами в домашних условиях? Как укрепить иммунитет ребенку в 2 года перед садиком и в период адаптации? Укреплять детский организм желательно начинать в теплое время года. Поймите как можно повысить иммунитет своему ребенку в домашних условиях. Чтобы ребенок не так часто болел и хорошо себя чувствовал, родители. Как поднять иммунитет в 4-5 лет. Для ребенка 4-5 лет особенно важно поддерживать иммунную систему, которая повергается регулярным атакам.
Назначение
При взаимодействии с ними, те, что находятся в очагах воспаления взаимоуничтожают друг друга и тем самым способствуют высвобождению от своего болезнетворного влияния.
Как заказать?
Заполните форму для консультации и заказа как укрепить иммунитет взрослому человеку в домашних. Оператор уточнит у вас все детали и мы отправим ваш заказ. Через 1-10 дней вы получите посылку и оплатите её при получении.
как укрепить иммунитет взрослому человеку в домашних. как повысить иммунитет при вич. Отзывы, инструкция по применению, состав и свойства.
Укрепить иммунитет ребенка просто: 10 советов доктора Комаровского. Увы, универсальной таблетки, которая повысит детский иммунитет, не существует, как и продуктов напрямую улучшающих защитные силы детского организма. К счастью, укрепить иммунитет действительно можно, правда, придется приложить гораздо больше усилий, чем просто купить в аптеке соответствующие таблетки. Как утверждает доктор Комаровский, главным вашим помощником в борьбе за здоровье (как свое собственное, так и ребенка) станет здоровый образ жизни. Советы доктора Комаровского родителям — как укрепить иммунитет ребенку, часто болеющего простудами. Как укрепить иммунитет часто болеющему ребенку и после простуд: рекомендации Комаровского. Доктор Комаровский в своем Instagram высказался о том, как укреплять иммунитет ребенка, и рассказал, есть ли смысл принимать иммуномодуляторы. Педиатр сказал, что часто родители оказывают своему ребенку медвежью услугу. У детей иммунитет может низким, может быть высоким, но в любом случае его необходимо поддерживать и постоянно повышать. Как это сделать и рассказал Доктор Комаровский, представив своеобразную шпаргалку для родителей. Крепкий иммунитет – это явный залог отличного здоровья. Но не всем,. Не секрет, что для того, чтобы меньше болеть, нужно укреплять иммунитет. Вопрос в том, как правильно это делать? Все искренне верят, что добрый доктор Комаровский знает волшебные таблетки, повышающие иммунитет. Как повысить иммунитет доктор Комаровский знает наверняка. Как укрепить подобный иммунитет Комаровскому и любому другому врачу естественными способами неизвестно.
Официальный сайт как укрепить иммунитет взрослому человеку в домашних
✔ Купить-как укрепить иммунитет взрослому человеку в домашних можно в таких странах как:
Россия, Беларусь, Казахстан, Киргизия, Молдова, Узбекистан, Украина Армения
Они выпускаются в виде комплексного средства с иммуномодулирующим действием на основе лекарственных трав. Принимая этот раствор, цена которого варьируется в доступных пределах, Вы не только сможете укрепить иммунную систему, но и сэкономить на приобретении других противовирусных препаратов. Укрепить иммунитет ребенка просто: 10 советов доктора Комаровского. Увы, универсальной таблетки, которая повысит детский иммунитет, не существует, как и продуктов напрямую улучшающих защитные силы детского организма. К счастью, укрепить иммунитет действительно можно, правда, придется приложить гораздо больше усилий, чем просто купить в аптеке соответствующие таблетки. Как утверждает доктор Комаровский, главным вашим помощником в борьбе за здоровье (как свое собственное, так и ребенка) станет здоровый образ жизни. Советы доктора Комаровского родителям — как укрепить иммунитет ребенку, часто болеющего простудами. Как укрепить иммунитет часто болеющему ребенку и после простуд: рекомендации Комаровского. Доктор Комаровский в своем Instagram высказался о том, как укреплять иммунитет ребенка, и рассказал, есть ли смысл принимать иммуномодуляторы. Педиатр сказал, что часто родители оказывают своему ребенку медвежью услугу. У детей иммунитет может низким, может быть высоким, но в любом случае его необходимо поддерживать и постоянно повышать. Как это сделать и рассказал Доктор Комаровский, представив своеобразную шпаргалку для родителей. Крепкий иммунитет – это явный залог отличного здоровья. Но не всем,. Не секрет, что для того, чтобы меньше болеть, нужно укреплять иммунитет. Вопрос в том, как правильно это делать? Все искренне верят, что добрый доктор Комаровский знает волшебные таблетки, повышающие иммунитет. Как повысить иммунитет доктор Комаровский знает наверняка. Как укрепить подобный иммунитет Комаровскому и любому другому врачу естественными способами неизвестно. Давайте возьмем первостольников. Каждый день на вас обрушиваются полчища вирусов и бактерий, но ведь вы в большинстве своем не болеете? Почему? Да потому что ваша иммунная система за годы работы в аптеке укрепилась в борьбе с этими агрессорами.
Как повысить иммунитет доктор Комаровский знает наверняка. Как укрепить подобный иммунитет Комаровскому и любому другому врачу естественными способами неизвестно. Давайте возьмем первостольников. Каждый день на вас обрушиваются полчища вирусов и бактерий, но ведь вы в большинстве своем не болеете? Почему? Да потому что ваша иммунная система за годы работы в аптеке укрепилась в борьбе с этими агрессорами.
Особенность капель Immunity (перевод с англ. immunity — иммунитет, невосприимчивость) заключается в том, что в составе средства комбинация из 18 лекарственных растений с целебными свойствами, которые дополняет комплекс из 6 витаминов, необходимых человеку для повышения иммунитета.
Получается, что часть клеток погибает от вирусного посягательства, а сам вирус вынужден погибнуть, нераспространившись и не оставив после себя потомства. Если сравнивать интерферон с бойцом, то ему отведена роль связиста, лазутчика.
Популярные и широко рекламируемые нынче средства Анаферон и Эргоферон вызывают у меня много вопросов.
чем можно поднять иммунитет взрослому лекарства
Ключевые слова: доктор шишонин иммунитет, купить чем можно поднять иммунитет взрослому лекарства, красное вино повышает иммунитет человека.
как повысить иммунитет детям в домашних условиях, чеснок для иммунитета рецепты, стимулятор иммунитета оберег, как укрепит иммунитет в садике, иммунитет фагоциты
Что такое чем можно поднять иммунитет взрослому лекарства
Отличительной чертой капель Иммунити является то, что они, в отличие от множества других иммуномодуляторов, не нарушают биологический фон и не вмешивается в химические процессы, постоянно происходящие в нашем теле. При взаимодействии с ними, те, что находятся в очагах воспаления взаимоуничтожают друг друга и тем самым способствуют высвобождению от своего болезнетворного влияния.
Официальный сайт чем можно поднять иммунитет взрослому лекарства
Состав
Самые эффективные средства для повышения защитных функций организма и укрепления иммунитета для борьбы. Иммунитет — это выработанная в ходе эволюции врожденная способность организма противодействовать различным веществам и организмам, вызывающих деструкцию его клеток. Бактериальные лекарства для поднятия иммунитета предназначены не только для. Как выбрать таблетки для поднятия иммунитета взрослым. Вероника, 36 лет Поднимать иммунитет хорошо натуральным препаратом Афлубин, раньше я долго его принимала. Однако эти капли на спирту, поэтому. Как правильно принимать препараты для повышения иммунитета — правила. Следует принимать лекарства для повышения иммунитета у взрослых при. Препараты для восстановления иммунитета можно разделить на несколько групп: гомеопатические препараты с действующими компонентами. Можно поднять иммунитет посредством правильного питания. Средства для поднятия иммунитета у взрослых необходимо принимать аккуратно. Иммунитет привыкнет зависеть от лекарств, и естественная защита перестанет правильно функционировать. Применение алоэ не рекомендуется людям. Какими средствами можно пользоваться во взрослом и детском возрасте, чтобы помочь организму? Что собой представляют препараты для повышения иммунитета? Лекарственные препараты для поднятия защитных функций. Для поддержания здоровья существует большое количество средств. Рейтинг лучших препаратов для повышения иммунитета. Лекарства, усиливающие иммунитет, можно использовать в следующих случаях. Виды лекарственных средств для иммунитета. Сегодня будем выяснять, какие препараты для поднятия иммунитета у взрослых есть в природе. При герпесе можно воспользоваться такими лекарствами, как. Сегодня вы узнали лучшие препараты для поднятия иммунитета у взрослых. Предложите прочитать статью своим друзьям, пусть они тоже. Заказать препараты для повышения иммунитета. В каталогах проекта можно выбрать необходимые препараты для повышения иммунитета и оформить. Сбои в функционировании иммунной системы бывают как у взрослых, так и у детей, поэтому в каталоге иммуностимуляторов можно без труда найти средства для.поднять иммунитет взрослому человеку — лекарства, витаминные комплексы, народные средства.
Иммунитет — это выработанная в ходе эволюции врожденная способность организма противодействовать различным веществам и организмам, вызывающих деструкцию его клеток. Бактериальные лекарства для поднятия иммунитета предназначены не только для. Как выбрать таблетки для поднятия иммунитета взрослым. Вероника, 36 лет Поднимать иммунитет хорошо натуральным препаратом Афлубин, раньше я долго его принимала. Однако эти капли на спирту, поэтому. Как правильно принимать препараты для повышения иммунитета — правила. Следует принимать лекарства для повышения иммунитета у взрослых при. Препараты для восстановления иммунитета можно разделить на несколько групп: гомеопатические препараты с действующими компонентами. Можно поднять иммунитет посредством правильного питания. Средства для поднятия иммунитета у взрослых необходимо принимать аккуратно. Иммунитет привыкнет зависеть от лекарств, и естественная защита перестанет правильно функционировать. Применение алоэ не рекомендуется людям. Какими средствами можно пользоваться во взрослом и детском возрасте, чтобы помочь организму? Что собой представляют препараты для повышения иммунитета? Лекарственные препараты для поднятия защитных функций. Для поддержания здоровья существует большое количество средств. Рейтинг лучших препаратов для повышения иммунитета. Лекарства, усиливающие иммунитет, можно использовать в следующих случаях. Виды лекарственных средств для иммунитета. Сегодня будем выяснять, какие препараты для поднятия иммунитета у взрослых есть в природе. При герпесе можно воспользоваться такими лекарствами, как. Сегодня вы узнали лучшие препараты для поднятия иммунитета у взрослых. Предложите прочитать статью своим друзьям, пусть они тоже. Заказать препараты для повышения иммунитета. В каталогах проекта можно выбрать необходимые препараты для повышения иммунитета и оформить. Сбои в функционировании иммунной системы бывают как у взрослых, так и у детей, поэтому в каталоге иммуностимуляторов можно без труда найти средства для.поднять иммунитет взрослому человеку — лекарства, витаминные комплексы, народные средства. Чтобы быстро повысить иммунитет можно использовать: ягоды, овощи. Какие можно принимать препараты для повышения иммунитета, используя народные способы? Для улучшения самочувствия.
Чтобы быстро повысить иммунитет можно использовать: ягоды, овощи. Какие можно принимать препараты для повышения иммунитета, используя народные способы? Для улучшения самочувствия.
Эффект от применения
Иммунитет — сложная структура, выстроенная организмом человека для защиты от микробов и вирусов. Иммунитет нестатичен. Он может ослабевать, повышаться и адаптироваться к угрозам. Неправильный образ жизни, чрезмерные нагрузки, холодный климат и многие другие факторы снижают иммунную защиту. Существуют проверенные способы, как поднять иммунитет в домашних условиях взрослому быстро. При их применении для повышения иммунитета у взрослых уйдет минимум времени. Поднятие иммунитета народными средствами — универсальный метод. Часто при незначительных сбоях в работе организма народной медицины достаточно для стабилизации здоровья, и использование аптечных лекарств необязательно. Начать обзор капель Immunity стоит, пожалуй, с самого определения иммунитета, ведь эта система невидима для наших глаз и потому не осознают ее возможности. В целом иммунитет человека – это сопротивляемость организма, способность противостоять внешним негативным факторам и вирусам.
Мнение специалиста
Как только устраняются причины, сразу повышается иммунитет человека. Можно сказать, что поддерживающие лекарства, которые мы принимаем для усиления иммунной системы, имеют почти такой же эффект как плацебо. Это относится, в большей степени, к самым востребованным средствам. О более серьёзных, которые назначаются докторами при тяжёлых болезнях речь не идёт.
Клеточный иммунитет (англ. Cell-mediated immunity) — такой тип иммунного ответа, в котором не участвуют ни антитела, ни система комплемента. В процессе клеточного иммунитета активируются макрофаги, натуральные киллеры, антиген-специфичные цитотоксиче. Лимфоциты — это клетки иммунной системы, представляющие собой разновидность лейкоцитов, которые обеспечивают гуморальный иммунитет (выработка антител), клеточный иммунитет (контактное. Клеточный иммунитет. Благодаря Т-лимфоцитам происходит клеточная иммунная система организма. Т-лимфоциты образуются из стволовых кроветворных клеток, которые мигрируют из костного мозга. Клеточный иммунитет активирует фагоциты, Т-лимфоциты, NK – клетки. Клетки памяти. Это малые лимфоциты, живущие значительно дольше других форм. Клеточный иммунитет. Иммунная система. В ответ на антигенный раздражитель Т-лимфоциты трансформируются в крупные делящиеся клетки. Т-клеточный иммунитет – это реакция в иммунной системе организма, посредством которой. Хотя Т-клетки, как и другие лимфоциты, образуются в костном мозге в организме, Т-клетки перемещаются в тимус после их. Снижение абсолютного количества Т-лимфоцитов свидетельствует о недостаточности клеточного иммунитета, а именно о недостаточности клеточно-эффекторного звена иммунитета. Выявляется при. Клеточно-опосредованный иммунитет. Антигенспецифичная ветвь клеточно-опосредованного иммунитета задействует Т-лимфоциты (рис. 1.3). В отличие от В-клеток, вырабатывающих растворимые антитела.
Клеточный иммунитет. Благодаря Т-лимфоцитам происходит клеточная иммунная система организма. Т-лимфоциты образуются из стволовых кроветворных клеток, которые мигрируют из костного мозга. Клеточный иммунитет активирует фагоциты, Т-лимфоциты, NK – клетки. Клетки памяти. Это малые лимфоциты, живущие значительно дольше других форм. Клеточный иммунитет. Иммунная система. В ответ на антигенный раздражитель Т-лимфоциты трансформируются в крупные делящиеся клетки. Т-клеточный иммунитет – это реакция в иммунной системе организма, посредством которой. Хотя Т-клетки, как и другие лимфоциты, образуются в костном мозге в организме, Т-клетки перемещаются в тимус после их. Снижение абсолютного количества Т-лимфоцитов свидетельствует о недостаточности клеточного иммунитета, а именно о недостаточности клеточно-эффекторного звена иммунитета. Выявляется при. Клеточно-опосредованный иммунитет. Антигенспецифичная ветвь клеточно-опосредованного иммунитета задействует Т-лимфоциты (рис. 1.3). В отличие от В-клеток, вырабатывающих растворимые антитела.
Назначение
Они выпускаются в виде комплексного средства с иммуномодулирующим действием на основе лекарственных трав. Принимая этот раствор, цена которого варьируется в доступных пределах, Вы не только сможете укрепить иммунную систему, но и сэкономить на приобретении других противовирусных препаратов.
Как заказать?
Заполните форму для консультации и заказа чем можно поднять иммунитет взрослому лекарства. Оператор уточнит у вас все детали и мы отправим ваш заказ. Через 1-10 дней вы получите посылку и оплатите её при получении.
чем можно поднять иммунитет взрослому лекарства. асд повышает иммунитет. Отзывы, инструкция по применению, состав и свойства.
Официальный сайт чем можно поднять иммунитет взрослому лекарства
✅ Купить-чем можно поднять иммунитет взрослому лекарства можно в таких странах как:
Россия, Беларусь, Казахстан, Киргизия, Молдова, Узбекистан, Украина Армения
При взаимодействии с ними, те, что находятся в очагах воспаления взаимоуничтожают друг друга и тем самым способствуют высвобождению от своего болезнетворного влияния. Поднять иммунитет – это увеличить невосприимчивость и устойчивость нашего организма к действию самых разных В статье мы расскажем, как поднять иммунитет организма и дадим. Как повысить иммунитет взрослому человеку – 10 советов с научным. Иммунитет – это способность организма сопротивляться воздействию любых чужеродных. Народные средства очень эффективны и будут работать 100% в комплексе со здоровым образом жизни. Иммунная система человека — целый комплекс защитных форм, органов и их функций, которые ставят мощный барьер перед вирусами, инфекциями, бактериями, ядами, грибками и т.д. И поддерживать ее. Комсомолка разбиралась как можно поднять иммунитет взрослому человеку. Как только организм подвергается атаке инфекции, то есть в него проникают болезнетворные бактерии, микробы, вирусы, то лимфоциты начинают. Содержание. 1 Как работает иммунная система организма. 2 Причины и симптомы снижения иммунитета у взрослых. 3 Что нужно помнить, правила безопасности. 4 Какие средства для поднятия иммунитета есть. 5 Лучшие средства. Какие методы повышения иммунитета не работают? Какие методы позволяют сохранить здоровье иммунной системы? Человеческий организм имеет одну из самых совершенных защитных систем в мире — иммунную. Иммунная система человеческого организма – это важнейшая защитная система. Она защищает человека от воздействия вредных и опасных бактерий и даже вирусов. Без иммунитета человек не может существовать. Узнайте, как поднять иммунитет взрослому человеку в домашних условиях при помощи витаминов и БАДов, а также при. Что такое иммунитет? Это защитные свойства нашего организма, которые проявляются в умении обнаруживать чуждые ему бактерии и вирусы, а также бороться с ними. Как работает иммунная система. Иммунитет в переводе с латинского языка – избавление от чего-либо. Иммунная система человека – сложный механизм, защищающий организм от болезней различного характера, сбоев и нарушений. Он может быть врождённым, то есть когда есть изначальная стойкость. Здравствуйте, друзья! Сегодня узнаем: Как быстро повысить иммунитет.
Поднять иммунитет – это увеличить невосприимчивость и устойчивость нашего организма к действию самых разных В статье мы расскажем, как поднять иммунитет организма и дадим. Как повысить иммунитет взрослому человеку – 10 советов с научным. Иммунитет – это способность организма сопротивляться воздействию любых чужеродных. Народные средства очень эффективны и будут работать 100% в комплексе со здоровым образом жизни. Иммунная система человека — целый комплекс защитных форм, органов и их функций, которые ставят мощный барьер перед вирусами, инфекциями, бактериями, ядами, грибками и т.д. И поддерживать ее. Комсомолка разбиралась как можно поднять иммунитет взрослому человеку. Как только организм подвергается атаке инфекции, то есть в него проникают болезнетворные бактерии, микробы, вирусы, то лимфоциты начинают. Содержание. 1 Как работает иммунная система организма. 2 Причины и симптомы снижения иммунитета у взрослых. 3 Что нужно помнить, правила безопасности. 4 Какие средства для поднятия иммунитета есть. 5 Лучшие средства. Какие методы повышения иммунитета не работают? Какие методы позволяют сохранить здоровье иммунной системы? Человеческий организм имеет одну из самых совершенных защитных систем в мире — иммунную. Иммунная система человеческого организма – это важнейшая защитная система. Она защищает человека от воздействия вредных и опасных бактерий и даже вирусов. Без иммунитета человек не может существовать. Узнайте, как поднять иммунитет взрослому человеку в домашних условиях при помощи витаминов и БАДов, а также при. Что такое иммунитет? Это защитные свойства нашего организма, которые проявляются в умении обнаруживать чуждые ему бактерии и вирусы, а также бороться с ними. Как работает иммунная система. Иммунитет в переводе с латинского языка – избавление от чего-либо. Иммунная система человека – сложный механизм, защищающий организм от болезней различного характера, сбоев и нарушений. Он может быть врождённым, то есть когда есть изначальная стойкость. Здравствуйте, друзья! Сегодня узнаем: Как быстро повысить иммунитет. 25 лучших рецептов. В рецепты включены фрукты и травы, повышающие иммунитет, пригодные для повышения иммунитета ребенку и взрослому. Иммунитет — это способность организма сопротивляться, иммунная система обезвреживает чужеродные клетки, различные инфекции и вирусы, а затем разрушает их. Признаки сбоя иммунитета. Иммунитет — сложная структура, выстроенная организмом человека для защиты от микробов и вирусов. Иммунитет нестатичен. Он может ослабевать, повышаться и адаптироваться к угрозам. Неправильный образ жизни, чрезмерные нагрузки, холодный климат и многие другие факторы снижают иммунную защиту. Существуют проверенные способы, как поднять иммунитет в домашних условиях взрослому быстро. При их применении для повышения иммунитета у взрослых уйдет минимум времени. Поднятие иммунитета народными средствами — универсальный метод. Часто при незначительных сбоях в работе организма народной медицины достаточно для стабилизации здоровья, и использование аптечных лекарств необязательно.
25 лучших рецептов. В рецепты включены фрукты и травы, повышающие иммунитет, пригодные для повышения иммунитета ребенку и взрослому. Иммунитет — это способность организма сопротивляться, иммунная система обезвреживает чужеродные клетки, различные инфекции и вирусы, а затем разрушает их. Признаки сбоя иммунитета. Иммунитет — сложная структура, выстроенная организмом человека для защиты от микробов и вирусов. Иммунитет нестатичен. Он может ослабевать, повышаться и адаптироваться к угрозам. Неправильный образ жизни, чрезмерные нагрузки, холодный климат и многие другие факторы снижают иммунную защиту. Существуют проверенные способы, как поднять иммунитет в домашних условиях взрослому быстро. При их применении для повышения иммунитета у взрослых уйдет минимум времени. Поднятие иммунитета народными средствами — универсальный метод. Часто при незначительных сбоях в работе организма народной медицины достаточно для стабилизации здоровья, и использование аптечных лекарств необязательно.
Отличительной чертой капель Иммунити является то, что они, в отличие от множества других иммуномодуляторов, не нарушают биологический фон и не вмешивается в химические процессы, постоянно происходящие в нашем теле.
Популярный рецепт для укрепления иммунитета с использованием полевого хвоща: 1 побег этого растения жевать раз в 24 часа. Трава возвращает силы организму и активирует его защитные функции. Еще один рецепт, как усилить иммунитет, по народным рекомендациям: заваривается чай из волосков кукурузы. Напиток повышает число антител и свертываемость крови. Рекомендуется для нормализации давления.
Во время сезонных эпидемий организм нуждается в усиленной иммунной защите. Для укрепления иммунитета специалисты советуют капли Иммунити. При использовании средства организм освободится от шлаков, и не возникнут осложнения со здоровьем.
Как повысить иммунитет взрослому человеку
Что нужно предпринять, чтобы долгое время оставаться здоровым и работоспособным? Кто-то вспомнит о правильном образе жизни и отказе от вредных привычек. Кто-то задумается об отдыхе на курорте и профилактике организма. Кто-то скажет, что нужно просто заниматься своим здоровьем, регулярно обследоваться, а также лечиться у проверенных врачей.
Кто-то задумается об отдыхе на курорте и профилактике организма. Кто-то скажет, что нужно просто заниматься своим здоровьем, регулярно обследоваться, а также лечиться у проверенных врачей.
Наше здоровье во многом зависит от состояния иммунной системы. Именно она вырабатывает средства защиты, необходимые для эффективного противостояния многим болезням.
Иммунитет бывает врожденным и приобретенным. Поэтому люди, от природы получившие слабый механизм защиты своего организма, с помощью определенных средств и методик могут заметно укрепить его.
Как повысить иммунитет взрослому человеку? В медицине изучению иммунных процессов, а также разнообразных нарушений работы иммунной системы посвящен целый раздел, называемый иммунологией. Получить общие рекомендации, а также скорректировать свой образ жизни и рацион можно во время консультации у терапевтов Rixos Prykarpattya. Если ситуация со здоровьем достаточно серьезная, стоит обратиться к иммунологу.
Что такое иммунитет человекаХотите узнать подробнее, что такое иммунитет человека, и как узнать его уровень? Это огромный комплекс специфических механизмов защиты. Его основная цель — нейтрализовать либо минимизировать воздействие негативных внешних факторов, попадающих в организм из окружающей среды (из воздуха, воды, вместе с продуктами питания и т.п.). Это могут быть не только инородные вещества, но и всевозможные вирусы и бактерии, способные стать причиной множества болезней.
На состояние иммунной системы влияет огромный ряд факторов. Это зависит от режима сна, образа жизни и физической активности, качества питания и питьевой воды, экологической обстановки в районе постоянного проживания и т.п.
Врач может сделать заключение о текущем состоянии иммунной системы, выполнив:
- Устный опрос пациента о состоянии здоровья и самочувствии.
- Визуальный осмотр.
- Изучение анамнеза (сколько раз и с каким интервалом были пневмонии, простудные заболевания и т.
 п.).
п.). - Расшифровку лабораторных анализов.
- Оценку иммунного статуса (с помощью специальных исследований — на иммуноглобулины, B-и T-лимфоциты, супрессоры и др.)
Ослабление иммунной системы, вызванное различными причинами, способно привести к ухудшению здоровья. Поэтому медики призывают тщательно следить за своим самочувствием, и не игнорировать тревожные сигналы, посылаемые нашим организмом.
Зная, что такое ослабленный иммунитет, а также своевременно предпринимая меры по его укреплению, можно снизить риск развития серьезных болезней, а также продлить жизнь.
Важно знать: Вы резко набрали или сбросили вес без явных причин? Развилась аллергия, проявляющая себя в виде насморка или кожных высыпаний? Кожа на лице пересыхает и шелушится, а на руках — краснеет и трескается? Вполне вероятно, что причиной этому стало резкое снижение иммунитета. Вместо того, чтобы глотать таблетки, стоит обратиться к врачу, пройти обследование и восстановить иммунную систему.
Как поднять иммунитет взрослого человека? Укреплять его можно в любое время года, во время работы и на отдыхе. Главное — действовать целенаправленно и методично, соблюдая все рекомендации врача. Не стоит самостоятельно ставить диагноз и делать преждевременные выводы о текущем состоянии иммунной системы. Только специалисты знают, как правильно оценить состояние здоровья пациента, и какие следует провести исследований (лабораторный анализ крови, первичный скрининг для тестирования иммунных функций, аллергопробы и т.п.).
Скрупулезно изучив все факторы и текущее состояние здоровья пациента, врач даст ряд советов, как повысить иммунитет у взрослого человека. Все они просты и доступны, не требуют больших затрат и особых усилий.
Признаки ослабленного иммунитетаВот самые распространенные симптомы ослабленного иммунитета, которые можно заметить еще до визита к врачу:
- Сильная утомляемость, снижение работоспособности.

- Сонливость, вялость, апатия. При этом сонливое состояние, присутствующее в течение всего дня, может сменяться бессонницей по ночам, что выбивает человека из колеи.
- Отсутствие аппетита.
- Снижение остроты зрения.
- Нарушение координации движений.
- Изменение цвета и состояния кожного покрова (сыпь на губах, прыщи на лице, «заеды» в уголках губ и т.п.).
- Высокая подверженность простудным заболеваниям. Малейшее переохлаждение — и вам приходится лечить насморк или кашель.
Большая часть взрослых людей отмечает, что ослабление иммунной системы приходится на осенне-зимний сезон. Вот наиболее частые причины ослабленного иммунитета, по мнению медиков:
- Нехватка витаминов и микроэлементов, представляющих особую ценность для организма.
- Недостаток кислорода и солнечного света.
- Снижение подвижности.
- Употребление рафинированных продуктов.
- Сбои в работе внутренних органов.
- Скопление шлаков и токсинов внутри организма.
- Недостаток полноценного отдыха.
- Частые стрессы и «выгорание» на работе.
- Недостаточная терморегуляция, и т.д.
Вот несколько типовых ситуаций, демонстрирующих причины снижения иммунитета:
- Человек не занимает своевременным лечением зубов. Из-за этого ухудшается процесс пережевывания пищи. При попадании в желудок она плохо расщепляется и медленно переваривается. Как следствие – нарушение обмена веществ, проблемы с желудком и кишечником, а также снижения иммунитета.
- Человек живет в жестком графике. Ранний подъем, сборы на работу в ускоренном темпе, ненормированный рабочий день, параллельное решение множества личных и семейных проблем. Плюс нерациональное питание и изнурительные тренировки в спортзале («для поддержания формы»). Физическая активность достаточно высока, но она приводит к перегрузкам, на фоне чего иммунитет снижается, и человек становится уязвим для болезней.

Опытные врачи RP подскажут, как быстро поднять иммунитет взрослому, и какие средства для этого потребуются. Это будет полезно не только тем, кто хочет сохранить здоровье, но и людям, недавно оправившимся от серьезных заболеваний.
Основные враги вашего здоровья, или от чего снижается иммунитетХотите выяснить, от чего слабеет иммунитет? Зная основные причины, приводящие к его снижению, можно предупредить заранее многие сезонные обострения хронических болезней.
Вот основные враги вашего здоровья, способны привести к ослаблению иммунитета взрослых людей:
- Хронический недосып. Жизнь в бешеном ритме ведет не только к ослаблению иммунитета, но и к другим проблемам: например, к ускоренному набору веса.
- Злоупотребление сахаром. Речь идет о белом сахаре, содержащем в огромном количестве углеводы, а также о выпечке и кондитерских изделиях. Организму сладкоежки приходится пережить своеобразный «стресс» после превышения суточной нормы (100 г) сахара. В последующие несколько часов сопротивляемость вирусам и бактериям падает почти вдвое. Чтобы пресечь такую тенденцию, диетологи рекомендуют пересмотреть свое меню, заменив белый сахар коричневым, а также использовать натуральный мед и сухофрукты.
- Обезвоженность. Нехватка жидкости вызывает чувство сильной усталости, а также негативно влияет на состояние иммунной системы.
- Пересыхание слизистой оболочки носоглотки. Одна из распространенных причин слабого иммунитета в зимний сезон, когда на улице и внутри помещений ощущается недостаток влаги. Бактерии, попавшие на сухую слизистую носа или горла, быстрее проникают в кровь. Поэтому в холодное время года люди чаще болеют простудными заболеваниями.
- Затяжные стрессы. В таких условиях организм вынужден работать на пределе, что ослабляет иммунную систему.
Полезно знать: многие путают закаливание с укреплением иммунитета. На самом деле это разные вещи. Закаливание помогает организму привыкнуть к резкому перепаду температур, и выработать стойкость к холоду. Рекомендации, как повысить иммунитет взрослого, касаются укрепления защитной системы организма в целом.
Закаливание помогает организму привыкнуть к резкому перепаду температур, и выработать стойкость к холоду. Рекомендации, как повысить иммунитет взрослого, касаются укрепления защитной системы организма в целом.
Чтобы разобраться, как быстро повысить иммунитет у взрослого, важно четко понимать ситуацию. Например, сделать это весной и летом намного проще, поскольку в рационе присутствует много свежих овощей и фруктов, и люди проводят много времени на открытом воздухе. Укрепить иммунную систему у относительно здорового человека будет проще и быстрее, чем после затяжной болезни, и т.п.
Как повысить иммунитет в домашних условияхВот простые и доступные способы, как повысить иммунитет взрослому человеку в домашних условиях. Они будут по силам практически всем:
- Пересмотрете свой распорядок дня. Цель — наладить сон, сохранить высокую работоспособность и улучшить самочувствие. Попробуйте подстроиться под световой режим дня, отправляясь спать чуть раньше обычного. Контролируйте потребление чая и кофе, создайте расслабляющую атмосферу в спальне. Запишитесь на курс общего либо релаксирующего массажа, посетите СПА.
- Проанализируйте, что и когда вы едите. Если это необходимо, посетите диетолога. Большая часть полезных веществ должна поступать в организм вместе с пищей, а не в виде капсул и биодобавок. Покупайте овощи и фрукты по сезону. В осенне-зимний период используйте свежие или замороженные ягоды – это настоящий кладезь витаминов. Можно пить травяные чаи, отвар шиповника, свежевыжатые соки и смузи. Пчеловоды рекомендуют гречаный мед — он укрепляет иммунитет гораздо лучше других сортов. Не забывайте про орехи и сухофрукты, а также про цельнозерновой хлеб и каши. Попробуйте есть небольшими порциями, 4-5 раз в течение дня. Тогда организм перестанет испытывать стресс в ожидании очередной порции пищи, и начнет работать более стабильно.

- Сократите употребление рафинированных сахаров, консервов, а также продуктов, прошедших сложную технологическую обработку. Используйте запекание и варку.
- Вода — это жизнь! В холодное время года хочется согреться чаем или кофе. Но не стоит забывать про обычную чистую воду: она необходима для растворения и выведения токсинов, а также для нормальной жизнедеятельности клеток. Вот почему в санаториях Трускавца практически всем пациентам назначат курс минеральной воды, подобранный индивидуально. Это восполняет нехватку влаги, нормализует водный баланс в организме, а также предупреждает дефицит микроэлементов. Минеральная вода в сочетании со свежим воздухом в RP способны как минимум в 1,5-2 раза усилить иммунитет. Такой полезный эффект сохраняется достаточно долго, на протяжении 3-6 месяцев.
- Следите за работой желудка и кишечника. Как утверждал доктор Майер, прославившийся благодаря своей диете, большинство болезней вызвано именно сбоями в работе ЖКТ. Даже банальный весенний авитаминоз, который мы привыкли списывать на смену сезонов, может быть вызван нехваткой полезной микрофлоры кишечника. Важно, чтобы в организме поддерживался баланс между полезными и вредными бактериями. Первые обитают на слизистых оболочках желудка и кишечника, вторые попадают внутрь вместе с пищей. Для поддержания баланса важно регулярно употреблять в пищу пребиотики и пробиотики. Они продаются в аптеках, в составе специальных комплексов, а также содержатся в самых простых продуктах: квашеной капусте, чесноке, яблоках, бобовых, соленых огурцах (бочковых), моцарелле.
- Контролируйте уровень нагрузок. Одно из самых важных условий, как повысить иммунитет взрослому в домашних условиях. Постарайтесь любыми силами избегать физического переутомления, нервных срывов и стрессов. Если чувствуете, что сильно устали, устраивайте себе «дни отдыха». Отключайте телефон, на время откажитесь от интернета, попросите близки не беспокоить вас по пустякам. Лучше всего провести день в тишине и спокойствии, либо отправиться на прогулку за город.

- Выходите чаще не улицу. Совет актуален для тех, кто работает в офисе или удаленно. Кратковременные пробежки от дома до остановки и на работу, а также походы в супермаркеты — не считаются. В день необходимо гулять именно на открытом воздухе как минимум 30-40 минут. Темп и дистанция подбираются индивидуально. Используйте фитнес-браслеты, чтобы подсчитать количество пройденных шагов и потраченные калории.
Прогулка решает одновременно три вопроса. Это:
- Предупреждение кислородного голодания.
- Нормализация массы тела (снижение веса).
- Улучшение кровоснабжения различных органов.
Физиотерапевты рекомендуют выполнять несложные физические упражнения типа разминки, или заняться несложной работой во дворе дома, если есть такая возможность.
Как повысить иммунитет после болезниТе, кто перенес очередное обострение хронических заболеваний, грипп или ОРВИ, часто интересуются, как повысить иммунитет после болезни. Ведь организм истощен борьбой с недугом, и нуждается в хорошей поддержке.
На помощь приходят витаминно-минеральные препараты. Обычно врачи назначают их в составе комплексного лечения, подбирая по результатам анализов. Но можно дополнительно проконсультироваться у терапевта: возможно, прием кое-каких препаратов придется продлить.
Если вы хотите узнать, как повысить иммунитет взрослому человеку витаминами, обязательно обратитесь к врачу. Самостоятельно подбирать и принимать витамины, ориентируясь по рассказам знакомых или рекламе, не стоит. Вместо пользы они могут принести вред. Например, отличный витаминно-антиоксидантный комплекс с пробиотиками и экстрактом зеленого чая идеально подойдет гипотоникам и людям с нормальным артериальным давлением. А гипертонику может стать плохо уже на 2-3 день приема капсул. Одно из самых удачных сочетаний — витамины С, D и цинк. Они ускоряют процесс выздоровления, но важно точно рассчитать дозировку.
Курс витаминов рекомендуют пропить в таких случаях:
- Острая нехватка определенных веществ в организме.
 Может выступать следствием перенесенной болезни или особенным состоянием пациента (например, при регулярных физических нагрузках необходимы белки и аминокислоты).
Может выступать следствием перенесенной болезни или особенным состоянием пациента (например, при регулярных физических нагрузках необходимы белки и аминокислоты). - Скудное нерегулярное питание. Характерно для женщин, постоянно сидящих на диетах, и стремящихся сбросить лишний вес.
В сочетании с аптечными медикаментами можно обратить внимание на качество питания и средства нетрадиционной (народной медицины). Например, пить чай с имбирем, придающим напитку оригинальный вкус, и положительно отражающемся на состоянии иммунной системы.
Как повысить иммунитет без лекарствХотите узнать, как повысить иммунитет в домашних условиях, не прибегая к помощи лекарств? Рекомендуем посетить диетолога и физиотерапевта Rixos Prykarpattya, получив подробные консультации. Цель – скоординировать режим дня и питание так, чтобы организм получал все необходимые полезные вещества.
Существует ряд продуктов, способных негативно отражаться на состоянии иммунной системы. Среди них:
- Красное мясо (свинина, жирная говядина и т.п.). Его лучше заменить телятиной или мясом птицы.
- Копчености и карбонаты. Они увеличивают вероятность мутаций клеток.
- Фаст-фуд. За счет огромного содержания жира приводят к повышению уровня холестерина, а также истончают клеточную мембрану.
- Кондитерские изделия. Негативно отражаются на работе надпочечников, а также ускоряют развитие воспалительных процессов.
Людям, страдающим анемией, рекомендуют употреблять в профилактических целях красное вино по 50-100 мл в день. Оно усиливает иммунитет, а также улучшает выработку эритроцитов в крови, способствуя повышению гемоглобина.
Врачи RP настоятельно рекомендуют использовать способы укрепления иммунитета в комплексе, а не ограничиваться 1-2 методами. Тогда вы сможете надолго сохранить крепкое здоровье, и избежать множества болезней.
Как повысить иммунитет: витамины и народные средства
Способы укрепления иммунитета и мифы об иммуномодуляторах
Иммунитет — функция организма, которая защищает его от воздействия вредоносных микроорганизмов, вирусов и бактерий. Когда он ослабевает, организм становится более проницаемым для внешних инфекций. В современных условиях во пандемии коронавируса как никогда необходимо позаботиться о своем иммунитете и укреплять его. Самые действенные способы повысить иммунную систему, витамины и народные средства, а также мифы об иммуномодуляторах разбираем в статье.
Когда он ослабевает, организм становится более проницаемым для внешних инфекций. В современных условиях во пандемии коронавируса как никогда необходимо позаботиться о своем иммунитете и укреплять его. Самые действенные способы повысить иммунную систему, витамины и народные средства, а также мифы об иммуномодуляторах разбираем в статье.
Как повысить иммунитет?
Прежде чем начать поднимать иммунитет, необходимо исключить привычки и продукты, которые мешают его нормальной работе. Главные факторы, которые снижают иммунитет:
- сезонный авитаминоз;
- стресс;
- вредные привычки;
- отсутствие режима;
- злоупотребление иммуномодуляторами;
- жесткие диеты.
Известно, что при сильном эмоциональном потрясении и перенапряжении нервной системы страдает иммунитет. Это связано с тем, что вместе со стрессом активно вырабатываются такие гормоны, как норадреналин и кортизол. Интересно, что при небольшом количестве кортизол создает защиту организму, но при его избытке он запускает аутоиммунные процессы. По этой причине невротики болеют чаще и дольше. Важно помнить, что паника и стресс, связанные со страхом заболеть коронавирусом, к хорошему не приведут.
Доказано, что человек, который ложится спать поздно и испытывает недостаток сна, болеет чаще. Ночью во сне вырабатываются полезные вещества, в том числе антитела, которые помогают организму побороть инфекции. Поэтому, чтобы укрепить иммунитет, нужно ложиться спать вовремя и высыпаться.
Жесткие диеты во многом вредны иммунитету тем, что организм недополучает необходимых витаминов и микроэлементов из пищи. Это также может привести к авитаминозу.
Иммуномодуляторы, противовирусные препараты и иммунитет
Иммуномодуляторы — все вещества, которые влияют на иммунитет. Они бывают как снижающими иммунитет, для лечения различных аутоиммунных заболеваний, так и активирующими силу иммунитета. Именно втором типом стараются вылечить ОРВИ или пьют для профилактики.
В то же время в Европе и США иммуностимулирующие препараты практически не используют. Такие препараты не входят в клинические рекомендации врачей.
Противовирусные препараты на самом деле не убивают вирус, так же как и антибиотики. Антибиотик может убить только бактерию. Против вируса он бессилен. Вирус же может погибнуть от высокой температуры, химии и облучения и только вне организма человека.
До сих пор врачи-иммунологи спорят насчет влияния иммуномодуляторов и их эффективности. Некоторые убеждены в том, что одна половина интерферонов — бесполезна, а другая, если и эффективна, то должна очень грамотно подбираться иммунологом, так как большая часть препаратов имеет много побочных эффектов и низкую клиническую изученность.
Также есть мнение, что иммуномодуляторы делают “ленивым” естественный иммунитет. Особенно это касается пациентов, которые бесконтрольно пьют таблетки по любому поводу. Тогда, встретившись с реальным вирусом, иммунная система может с ним не справиться сама.
Все мнения можно подытожить тем, что принимать иммуностимулирующие препараты можно только после консультации и с назначением проверенного врача-иммунолога.
С вирусными инфекциями организм должен бороться самостоятельно, силами собственного иммунитета и прививок. При борьбе ОРВИ чаще всего хватает симптоматического лечения. А таблеток, убивающих вирус, просто не существует!
По этой же причине всем известный коронавирус также лечат симптоматически, воздействуя на имеющиеся симптомы у больного.
Укрепить иммунитет можно, питаясь правильно и создавая все условия для правильной работы организма и всех его систем. Рассмотрим ключевые действия для поднятия иммунитета:
- Нормализовать режим сна;
- Скорректировать питание;
- Избавиться от вредных привычек.
- Употреблять полезные продукты для иммунитета;
- Получать витамины для иммунитета;
- “Долечивать” болезни, не оставлять на самотек.

- Закалять организм.
Продукты, повышающие иммунитет
Главный ключ к хорошему иммунитету — правильное, сбалансированное питание, которое дает организму необходимое количество витаминов и микроэлементов. Более того, многие врачи убеждены, что источник качественной работы иммунитета — кишечник. Именно его правильная работа способна обеспечить наилучшую усвояемость полезных веществ.
Чтобы поднять иммунитет и поддерживать его нормальную функцию, обратите внимание на список этих продуктов. Они богаты необходимыми витаминами и другими полезными для иммунитета веществами. Многие из них могут стать аналогами вредной пищи, которую многие из нас употребляют в течение дня.
Шиповник
Вместо кофе, газировок, соков
Шиповник богат витамином С и обладает антибактериальным эффектом. В нем гораздо больше витамина С, чем в лимоне и смородине. Шиповник рекомендуется употреблять в виде настоя. Ягоды залейте кипятком и настоять в течение нескольких часов. На литр воды примерно 80-100 гр плодов. Стакана в день достаточно. Также вы можете приобрести готовый сироп или настой шиповника в аптеке.
Мед
Вместо сахара
Столовой ложки меда в день достаточно, чтобы поддерживать иммунитет. На основе меда можно также сделать лекарственные смеси, которые также повышают функцию защиты организма в сезоны заболеваемости. Смешивайте мед с чесноком, алоэ, лимоном или имбирем на выбор. Тогда вы получите сильное средство в борьбе с вирусами.
Корень женьшеня
Женьшень повышает способность организма самостоятельно справляться с инфекциями. Тем не менее, его рекомендуется принимать по назначению врача, так как он имеет противопоказания, а превышение дозировки может навредить.
Грецкие орехи
Вместо чипсов на перекус
Этот орех за счет витаминов и масел в своем составе также помогает укрепить иммунитет. Также это, довольно, сытный продукт с высокой питательной ценностью. Однако орех — продукт аллергенный и имеет некоторые противопоказания. Поэтому перед употреблением проконсультируйтесь с врачом и исключите возможные побочные эффекты.
Однако орех — продукт аллергенный и имеет некоторые противопоказания. Поэтому перед употреблением проконсультируйтесь с врачом и исключите возможные побочные эффекты.
Корень имбиря
В имбире содержится масса полезных веществ: витамины С, А, В1, В2, цинк, магний, железо, фосфор, калий, кальций и аминокислоты. Он имеет согревающий эффект и улучшает кровообращение. Добавлять его можно в чай, настои и смеси.
Чеснок
Продукт является естественным антибиотиком, который повышает иммунитет и борется с вредоносными микробами. Одного зубчика чеснока в день хватает для профилактики.
Красное мясо
Постное мясо с минимальным количеством жира — полезный продукт для повышения иммунитета. В нем содержится цинк, которые способствует выработке белых кровяных клеток. Они помогают бороться с вредными бактериями и вирусами. 100 граммов в день достаточно для взрослого человека.
“Полезный чай”
Чай с полезными добавками, в виде лимона, меда, малины, смородины, имбиря — одно из лучших народных средств для повышения иммунитета и профилактики вирусов. Такой чай богат витамином С и антиоксидантами.
Также стоит исключить или снизить количество вредной пищи из рациона, чтобы обеспечить хорошее функционирования кишечника. Вот неполный список продуктов, употребление которых стоит снизить.
— газировка;
— сахар;
— крепкий алкоголь;
— фастфуд;
— консервы;
— колбасы.
Витамины для иммунитета
В современном темпе жизни не всегда удается поддерживать правильное питание. Тогда могут помочь искусственно синтезированные “аптечные” витамины. Обратите на список этих витаминов для иммунитета при выборе витаминного комплекса.
Важно! Здесь указан список витаминов и микроэлементов, необходимых для здорового функционирования организма и их суточная норма. Большую долю витаминов и микроэлементов вы уже получаете из пищи. Поэтому стараться получить все указанное количество из аптечных препаратов нельзя! Постарайтесь внести в свой рацион продукты, богатые этими элементами, а нехватку можете дополнить витаминными комплексами.
Поэтому стараться получить все указанное количество из аптечных препаратов нельзя! Постарайтесь внести в свой рацион продукты, богатые этими элементами, а нехватку можете дополнить витаминными комплексами.
Суточная норма витаминов
— С — до 10 г;
— В1 — 1,5-2 мг;
— В2 — 2-2,5 мг;
— В6 — 2-3 мг;
— В12 — 0,002 мг;
— Р — 25 мг;
— РР — 0,25 мг;
— U — 100-300 мг;
— D — 0,001 мг.
— A — 900 мкг.
Узнать подробнее о витаминах, где они содержатся и что укрепляют, вы можете здесь.
Суточная норма минералов
— цинка — 15 мг;
— железа — 10-15 мг;
— калий — 2-5 г;
— магний — 400 мг;
— фосфор — 1,2 г;
— кальций — 1 г;
— медь — 30 мкг/кг — для взрослых, 80 мкг/кг — для детей раннего возраста, 40 мкг/кг — для детей старшего возраста.
— марганец — 2-3 мг;
— хром — 100-200 мкг;
— селен — 150—200 мкг.
— йод — 200 мкг.
Подбирать витамины рекомендуется вместе с врачом.
Автор
Валерия Кручинина
детских иммунных систем отличаются от взрослых. Вот что это может означать для COVID-19
Когда дело доходит до инфекционных заболеваний, наши тела могут защитить себя только в том случае, если они способны различать «я» и «чужое». И мы не говорим здесь о философии — в иммунологии термины используются для дифференциации наших собственных клеток от чужеродных материалов. Это означает, что для атаки такого вируса, как COVID-19, наша иммунная система должна сначала распознать, что чужеродный захватчик не является одной из наших собственных клеток.
И мы не говорим здесь о философии — в иммунологии термины используются для дифференциации наших собственных клеток от чужеродных материалов. Это означает, что для атаки такого вируса, как COVID-19, наша иммунная система должна сначала распознать, что чужеродный захватчик не является одной из наших собственных клеток.
Но ребенок, растущий в утробе матери, также технически является инородным телом, поскольку он разделяет с матерью только 50 процентов своей ДНК. Салли Пермар, вирусный иммунолог из Университета Дьюка, говорит, что именно поэтому иммунная система плода в основном пассивна. Плод должен преуменьшать свои собственные иммунные реакции, чтобы организм матери не отвергал их.
Тем не менее, как только ребенок рождается, его иммунная система должна быстро реагировать на мир, изобилующий вирусами и бактериями, готовыми заразить своего нового хозяина.Так чем же развивающаяся иммунная система младенцев и детей отличается от взрослых? И могут ли эти биологические различия объяснить, почему они, кажется, лучше справляются с COVID-19, чем взрослые, или насколько они передают его другим?
Адаптируйся и выживай
Наша иммунная система состоит из врожденных реакций, с которыми мы родились, и адаптивных реакций, возникающих в результате накопленного воздействия прошлых патогенов. Как часть этой врожденной реакции, младенцы снабжаются миллионами вновь сгенерированных иммунных воинов, называемых Т-клетками.Каждая из клеток распознает разные патогены и помогает укрепить нашу растущую иммунную систему. Но в детстве эти цифры начинают стремительно уменьшаться.
«К тому времени, когда вы становитесь подростком или молодым взрослым, вы действительно не выкачиваете столько новых Т-клеток, а к сорока годам их почти не остается», — говорит Донна Фарбер, иммунолог. в Колумбийском университете. «Итак, [взрослые] полагаются на все те реакции памяти, которые вы генерировали в детстве».
Фарбер объясняет, что развитие иммунной системы преследует двоякую цель. Во-первых, создайте устойчивый врожденный ответ на все новые инфекции. (Это особенно важно в наши самые уязвимые ранние годы.) Во-вторых, создайте воспоминания — в виде ячеек памяти — для всех патогенов в вашем окружении, чтобы вы могли быть защищены от них в будущем. Фарбер говорит, что если ваше окружение не сильно меняется на протяжении всей вашей жизни, к взрослой жизни вы должны быть идеально адаптированы, чтобы оставаться здоровыми по отношению к большинству токсинов.
Во-первых, создайте устойчивый врожденный ответ на все новые инфекции. (Это особенно важно в наши самые уязвимые ранние годы.) Во-вторых, создайте воспоминания — в виде ячеек памяти — для всех патогенов в вашем окружении, чтобы вы могли быть защищены от них в будущем. Фарбер говорит, что если ваше окружение не сильно меняется на протяжении всей вашей жизни, к взрослой жизни вы должны быть идеально адаптированы, чтобы оставаться здоровыми по отношению к большинству токсинов.
Но Фарбер также отмечает, что этот компромисс между нашими врожденными и адаптивными реакциями может поставить взрослых в невыгодное положение с новым коронавирусом.Ни у детей, ни у взрослых не было Т-клеток памяти на COVID-19 в начале пандемии, поскольку никто еще не подвергался воздействию вируса. Но поскольку у взрослых также меньше наивных Т-клеток, Фарбер говорит, что их врожденной иммунной системе требуется больше времени, чтобы отреагировать. Ситуация становится еще хуже для пожилых людей, поскольку они не могут эффективно избавиться от инфекции и продолжать накапливать повреждения, добавляет она.
Для детей, по словам Фарбера, COVID-19 может быть не такой большой проблемой, потому что люди уже подвержены наиболее инфекционным заболеваниям в детстве, поэтому столкнуться с новым заболеванием не так уж и ненормально.Таким образом, их врожденный иммунный ответ, вероятно, лучше подготовлен к быстрому ответу.
Копаем глубже
Данные лаборатории Фарбера также предполагают, что у детей могут быть более сильные врожденные реакции не только из-за наличия большего количества наивных Т-клеток, но и из-за , где расположены эти клетки. В исследовании 2019 года, опубликованном в журнале Nature Mucosal Immunology , они обнаружили, что у детей больше наивных Т-клеток в определенных участках ткани, а не только в их крови, что может означать усиление иммунных ответов в любой ткани, на которую нацелен вирус.
Пермар отмечает несколько других гипотез, объясняющих, почему дети в целом лучше переносят COVID-19. Например, некоторые исследования показали, что у детей в носу более низкий уровень рецептора, который прикрепляется вирусом, который называется ACE2. Кроме того, дети могут иметь частичную защиту от COVID-19 из-за более частого контакта с другими человеческими коронавирусами по сравнению со взрослыми. Но обе эти гипотезы все еще нуждаются в дополнительных исследованиях, добавляет она.
Например, некоторые исследования показали, что у детей в носу более низкий уровень рецептора, который прикрепляется вирусом, который называется ACE2. Кроме того, дети могут иметь частичную защиту от COVID-19 из-за более частого контакта с другими человеческими коронавирусами по сравнению со взрослыми. Но обе эти гипотезы все еще нуждаются в дополнительных исследованиях, добавляет она.
У детей все еще может быть тяжелая реакция на COVID-19, такая как редкие случаи мультисистемного воспалительного синдрома или MIS-C, который может вызывать воспаление различных частей тела.Но даже тогда лаборатория Фарбера обнаружила, что иммунные реакции у детей отличаются от тяжелых случаев у взрослых. У детей было меньше антител, белков, атакующих патогены, по сравнению со взрослыми. Кроме того, Фарбер говорит, что результаты показывают, что вирус не попадал в их легкие. Они все еще не понимают, почему это так, и почему у некоторых детей вообще возникает такая серьезная реакция.
Tag, You’re It
Ранние отчеты предполагали, что дети не передают вирус другим, в то время как более свежие данные предполагали, что только дети старшего возраста передают вирус так же часто, как взрослые.Но новое исследование, опубликованное в журнале JAMA Pediatrics , показало, что у детей младше пяти лет действительно было наибольшее количество вирусной РНК в мазках из носа.
Тейлор Хилд-Сарджент, специалист по педиатрическим инфекционным заболеваниям из Детской больницы имени Энн и Роберта Х. Лурье в Чикаго и ведущий автор исследования, отмечает, что измерение вирусной РНК — это не то же самое, что определение количества инфекционного вируса, переносимого кем-то. Таким образом, хотя исследование не доказывает, что дети младшего возраста больше распространяют вирус, по ее словам, эти два показателя коррелировали друг с другом.
«Суть в том, что мы должны быть в безопасности, и [наше исследование] развеивает идею о том, что дети обладают иммунитетом и что они не могут заразиться», — говорит она. «Но он не говорит нам, как часто они заражаются, и не говорит нам, как часто они его распространяют».
«Но он не говорит нам, как часто они заражаются, и не говорит нам, как часто они его распространяют».
Хилд-Сарджент, Фарбер и Пермар подчеркивают, что все еще необходимы более масштабные исследования, чтобы по-настоящему оценить влияние коронавируса на детей — и контролировать продолжительность и качество их иммунных реакций, особенно для тех, у кого симптомы более легкие за пределами больниц.Но Пермар также отмечает, что пока мы знаем, что дети менее подвержены серьезному заболеванию. Кроме того, данные о передаче свидетельствуют о том, что дети младшего возраста не распространяют вирус в такой степени, как дети старшего возраста и взрослые.
Еще один фактор, о котором мы пока не знаем, — говорит Пермар, — это то, в каком возрасте лучше всего вакцинировать младенцев и детей, когда они станут доступны. Она упоминает о возможности того, что, как и в случае с вакцинами от других вирусов, самые молодые из нас могут на самом деле проявить наилучшие реакции, которые обеспечат защиту на всю жизнь.В конце концов, это хорошо сочетается с объяснением Фарбера о том, как работает развивающаяся иммунная система: выжить, а затем вспомнить, как выжить снова.
Коморбидность является лучшим показателем нарушения иммунитета, чем хронологический возраст у пожилых людей
Цели: Определить, может ли высокий уровень сопутствующей патологии, измеренный с помощью стандартизованного инструмента, предсказать нарушение иммунитета у пожилых людей.
Параметр: Гериатрическая амбулаторная клиника и отделение по уходу за ветеранами в системе здравоохранения Большого Лос-Анджелеса.
Участники: Пятнадцать мужчин в возрасте от 51 до 95 лет с различной степенью хронических заболеваний.
Размеры: Бремя заболевания измерялось с использованием шкалы совокупной оценки болезни (CIRS) и иммунитета с использованием пролиферации Т-клеток, индуцированной фитогемагглютинином (ФГА), и продукции интерлейкина (ИЛ) -12, провоспалительного цитокина, который стимулирует Т-хелперный иммунный ответ, и ИЛ-10, цитокин, который ингибирует Т-хелперный иммунный ответ в ответ на митогенную стимуляцию мононуклеарных клеток периферической крови.
Полученные результаты: С увеличением сопутствующей патологии (увеличение показателя CIRS) у пожилых людей происходит пропорциональное снижение иммунного ответа (уменьшение пролиферации Т-клеток и продукции IL-12 и увеличение продукции IL-10 в ответ на стимуляцию PHA). Ни иммунный ответ, ни оценка CIRS не были достоверно коррелированы с хронологическим возрастом в этой выборке пожилых людей с различной степенью хронического заболевания.
Заключение: Это исследование демонстрирует, что уровень сопутствующей патологии коррелирует с величиной иммунного ответа у пожилых людей, и предполагает, что CIRS можно использовать для определения степени нарушения иммунитета у пожилых людей с различными специфическими заболеваниями и разными уровнями тяжести.
Эволюция иммунной системы человека от младенчества до старости
Резюме
В этой статье рассматривается развитие иммунного ответа в неонатальном, младенческом и взрослом возрасте, включая беременность, заканчивающуюся снижением старости.Возникает картина ребенка, рожденного с незрелой, врожденной и адаптивной иммунной системой, которая созревает и приобретает память по мере его роста. Затем в старости он приходит в упадок. Эти изменения рассматриваются наряду с рисками различных типов инфекций, аутоиммунных заболеваний и злокачественных новообразований.
Затем в старости он приходит в упадок. Эти изменения рассматриваются наряду с рисками различных типов инфекций, аутоиммунных заболеваний и злокачественных новообразований.
Ключевые слова: адаптивный иммунитет, врожденный иммунитет, инфекции
1. Введение
И один человек в свое время играет много ролей,
Его деяниям семь возрастов.
Более 1600 генов участвуют в врожденных и адаптивных иммунных ответах [1]. Эти гены имеют большое значение для поддержания жизни во враждебной среде. Тем не менее, иммунная система является относительно незрелой при рождении и должна развиваться в течение жизни, подвергаясь воздействию множества внешних проблем в детстве, в молодом и зрелом возрасте (включая беременность), до упадка старости ().
( a ) Семь возрастов женщины. ( b ) Схематический график дополнительных смертей от сезонного или пандемического гриппа на протяжении жизни человека, представленный как число смертей на 1000 человек (адаптировано из [2]).Обратите внимание, что хотя беременность увеличивает риск тяжелого гриппа, во время тяжелых пандемий, таких как 1918/1919 гг., Также наблюдались избыточные смертельные случаи среди ранее здоровых молодых людей, которые не были беременными. ( c ) Схематический график различных звеньев иммунного ответа на грипп на протяжении жизни человека.
2. Онтогенез иммунной системы в молодом возрасте
Сначала младенец,
Мычание и рвота в руках медсестры.
In utero среда плода требует, чтобы иммунная система оставалась толерантной к материнским аллоантигенам.После рождения внезапное колоссальное воздействие антигенов окружающей среды, многие из которых происходят из кишечных комменсальных бактерий, требует быстрых изменений, чтобы вызвать определенные иммунные реакции, соответствующие раннему возрасту.
(a) Врожденная иммунная система
Врожденная иммунная система обеспечивает раннюю первую линию защиты от вторжения патогенов. Вовлеченные клетки — нейтрофилы, моноциты, макрофаги и дендритные клетки, которые все взаимодействуют с адаптивной иммунной системой. Эти клетки развиваются и созревают в течение жизни плода, но в разное время, и функция всех компонентов врожденного иммунитета у новорожденных слабее по сравнению с более поздней жизнью.
Вовлеченные клетки — нейтрофилы, моноциты, макрофаги и дендритные клетки, которые все взаимодействуют с адаптивной иммунной системой. Эти клетки развиваются и созревают в течение жизни плода, но в разное время, и функция всех компонентов врожденного иммунитета у новорожденных слабее по сравнению с более поздней жизнью.
Зрелые нейтрофилы присутствуют в конце первого триместра и резко увеличиваются в количестве, стимулируемые гранулоцитарно-колониестимулирующим фактором, незадолго до рождения. Затем их количество возвращается к стабильному уровню в течение нескольких дней, но они демонстрируют слабую бактерицидную функцию, слабую реакцию на воспалительные стимулы, снижение адгезии к эндотелиальным клеткам и уменьшение хемотаксиса [3]. Эти дефициты более заметны у недоношенных детей, у которых также ниже сывороточный IgG и комплемент. Следовательно, новорожденные, и особенно недоношенные, имеют нарушенные функции нейтрофилов [4], что подвергает ребенка риску бактериальных инфекций.
У недоношенных и новорожденных классические моноциты и макрофаги также являются незрелыми. У них снижена экспрессия TLR4 [5] с нарушением врожденных сигнальных путей [6-8], что приводит к снижению цитокиновых ответов по сравнению со взрослыми. Следовательно, происходит плохое восстановление тканей, нарушенный фагоцитоз потенциальных патогенов и плохая секреция биоактивных молекул. Однако, хотя частота макрофагов в легких у недоношенных и доношенных детей снижается, уровни этих клеток у взрослых достигаются в течение нескольких дней после рождения [9].
По сравнению с кровью детей или взрослых, пуповинная кровь содержит меньше дендритных клеток миелоидного типа (mDC). Они экспрессируют более низкие уровни HLA класса II, CD80 и CD86 на клеточной поверхности, чем взрослые mDC [10]. Они секретируют низкие концентрации IL-12p70 в ответ на активацию врожденных стимулов [11]. Таким образом, праймирование Т-клеточных ответов Th2 и CD8 снижено по сравнению со взрослыми, что коррелирует с повышенной восприимчивостью к инфекциям, вызываемым вирусами Mycobacterium tuberculosis и Salmonella spp . Напротив, новорожденные mDC, стимулированные с помощью TLR4, секретируют подобные взрослым концентрации провоспалительных цитокинов [12], которые способствуют иммунным ответам Th27.
Напротив, новорожденные mDC, стимулированные с помощью TLR4, секретируют подобные взрослым концентрации провоспалительных цитокинов [12], которые способствуют иммунным ответам Th27.
Плазмацитоидные дендритные клетки (pDC) выделяют высокие концентрации интерферона I типа (IFN) в ответ на стимуляцию TLR7 и TLR9 у взрослых. Однако новорожденные pDC строго ограничены в секрете интерферона α / β при воздействии различных вирусов, несмотря на то, что уровни экспрессии TLR7 и TLR9 аналогичны взрослым [13]. Следовательно, врожденные иммунные ответы на вирусы, такие как респираторно-синцитиальный вирус, вирус простого герпеса и цитомегаловирус, являются слабыми по сравнению с более поздними периодами жизни.
Естественные киллерные (NK) клетки у взрослых сдерживают репликацию и распространение вируса до установления адаптивного иммунитета [14]. Они регулируются ингибирующими рецепторами, которые распознают HLA-A, B, C и E, и, следовательно, способствуют самотолерантности. На ранних сроках беременности NK-клетки гипочувствительны к клеткам-мишеням, лишенным молекул класса I главного комплекса гистосовместимости (MHC) (таких как трофобласт [15]), и очень чувствительны к подавлению иммунитета за счет трансформирующего фактора роста-β (TGF-β).Цитолитическая функция NK увеличивается во время беременности, но при рождении все еще составляет лишь половину от взрослого уровня. Новорожденные NK-клетки менее чувствительны к активации IL-2 и IL-15 и продуцируют ограниченные концентрации IFN-γ. Однако порог активации клеток ниже, что обеспечивает некоторую противовирусную защиту [15].
Три независимых пути, которые активируют систему комплемента, имеют решающее значение для защиты хозяина и воспаления. Компоненты комплемента способствуют опсонизации, являются хемоаттрактантами для врожденных клеток, опосредуют лизис клеток и влияют на выработку антител.Концентрация почти всех циркулирующих компонентов в сыворотке новорожденных на 10–80% ниже, чем у взрослых [16], при пониженной биологической активности. Уровни комплемента повышаются после рождения, при этом некоторые сывороточные факторы достигают концентрации у взрослых в течение месяца (например, фактор B), но другие развиваются медленнее [16]. Поскольку у младенцев низкая концентрация иммуноглобулина, эффекторные функции комплемента зависят от альтернативных путей активации и лектин-связывающей активации, запускаемых полисахаридами и эндотоксинами.
Уровни комплемента повышаются после рождения, при этом некоторые сывороточные факторы достигают концентрации у взрослых в течение месяца (например, фактор B), но другие развиваются медленнее [16]. Поскольку у младенцев низкая концентрация иммуноглобулина, эффекторные функции комплемента зависят от альтернативных путей активации и лектин-связывающей активации, запускаемых полисахаридами и эндотоксинами.
В целом, врожденная иммунная система при рождении приглушена, цена, вероятно, заплачена плодом не только за переносимость необщих материнских антигенов, но и за игнорирование значительного стресса и ремоделирования, которые происходят во время развития.Это делает новорожденного, особенно недоношенного, относительно восприимчивым к бактериальным и вирусным инфекциям.
(b) Адаптивная иммунная система
Т-клетки развиваются в тимусе, который является самым большим при рождении и в течение первых лет жизни. Зрелые единичные CD4 + и CD8 + положительные Т-клетки впервые обнаруживаются в тимусе на 15 неделе и в большом количестве на периферии задолго до рождения [17,18]. Однако неонатальные Т-клетки значительно отличаются от взрослых клеток, отражая жизнь плода, где воздействие чужеродных антигенов в значительной степени ограничивается ненаследственными материнскими аллоантигенами.Функция ранних Т-клеток отличается от взрослых Т-клеток. Например, хотя наивные CD4 + Т-клетки плода сильно реагируют на аллоантигены, они имеют тенденцию развиваться в направлении Foxp3 + CD25 + регуляторных Т-клеток (T reg ) под влиянием TGF-β [19], и таким образом активно продвигают терпимость к себе. Периферические Т reg составляют около 3% от общего количества CD4 + Т-клеток при рождении [20], и эти клетки сохраняются в течение длительного периода времени [21], придавая иммунному ответу в раннем возрасте противовоспалительный профиль [22 ].
Активация чужеродным антигеном поздних эмбриональных или неонатальных Т-клеток приводит к ответу, искаженному в сторону иммунитета Th3 [23], который усиливается неонатальными дендритными клетками и эпигенетическими особенностями [24,25]. Таким образом, очень ранний адаптивный Т-клеточный иммунитет характеризуется толерогенной реактивностью, сниженным распознаванием алло-антигена и слабыми ответами на чужеродные антигены.
Таким образом, очень ранний адаптивный Т-клеточный иммунитет характеризуется толерогенной реактивностью, сниженным распознаванием алло-антигена и слабыми ответами на чужеродные антигены.
У новорожденных, помимо обычных Т-клеток, которые распознают пептидные антигены в контексте классических молекул MHC, существуют популяции γδ Т-клеточных рецепторов (TCR) -позитивных и врожденных-подобных αβ-TCR-позитивных Т-клеток.К ним относятся функционально компетентные клетки iNKT, которые быстро продуцируют IFN, ассоциированные со слизистой оболочкой инвариантные Т-клетки (MAIT) [26] и недавно описанные интерлейкин-8 (CXCL8) -секретирующие наивные Т-клетки, которые связывают врожденный и адаптивный иммунитет [27]. Клетки MAIT развиваются в тимусе, но их созревание может происходить в тканях слизистой оболочки плода до микробной колонизации. Т-клетки, продуцирующие CXCL8, производят важные эффекторные функции у новорожденных людей, поскольку они обладают потенциалом активации антимикробных нейтрофилов и γδ Т-клеток.Они, по-видимому, особенно активны на барьерах слизистой оболочки недоношенных и доношенных детей, хотя их частота уменьшается с возрастом. В отличие от взрослой крови, где репертуар γδ TCR ограничен, γδ T-клетки неонатальной крови обнаруживают множество комбинаций рецепторных цепей, которые меняются с беременностью [27]. γδ Т-клетки могут продуцировать значительные количества IFN-γ после кратковременной поликлональной стимуляции, компенсируя незрелость более классического ответа Т-клеток Th2-типа на неонатальные инфекции [28,29].
Два типа В-клеток возникают через разные пути развития [30]. Клетки B1 спонтанно секретируют низкоаффинный IgM с ограниченным диапазоном антигенной специфичности (включая обычные бактериальные полисахариды), имеют меньше соматических мутаций и служат первой линией защиты [31]. Клетки B1 секретируют IL-10 и TGF-β и, таким образом, способствуют ответу Th3. При рождении B1-клетки составляют 40% B-клеток периферической крови, и эта частота остается высокой в течение нескольких месяцев [32]. Обычные В-клетки (обозначенные как клетки В2) происходят из многолинейного общего лимфоидного предшественника CD34 + и генерируют широкий репертуар иммуноглобулиновой специфичности благодаря экспрессии терминальной дезоксинуклеотидилтрансферазы, которая увеличивает разнообразие в присоединении сегментов гена иммуноглобулина V-D-J.В-клетки обычно присутствуют во вторичных лимфоидных органах и в костном мозге, где они вносят вклад в гуморальный ответ адаптивной иммунной системы.
Обычные В-клетки (обозначенные как клетки В2) происходят из многолинейного общего лимфоидного предшественника CD34 + и генерируют широкий репертуар иммуноглобулиновой специфичности благодаря экспрессии терминальной дезоксинуклеотидилтрансферазы, которая увеличивает разнообразие в присоединении сегментов гена иммуноглобулина V-D-J.В-клетки обычно присутствуют во вторичных лимфоидных органах и в костном мозге, где они вносят вклад в гуморальный ответ адаптивной иммунной системы.
Большинство ответов антител, в том числе на бактериальные белки, бактериальные полисахариды и на полисахаридно-белковые конъюгированные вакцины, зависят от помощи Т-клеток. Они полагаются на взаимодействие между TCR и участие корецепторов, включая CD28 и лиганд CD40, на Th3 или фолликулярных Т-хелперных клетках с их соответствующими партнерами по связыванию HLA-пептидом, CD80 / 86 и CD40 на антиген-специфических В-клетках.Однако неонатальные В-клетки экспрессируют низкие уровни этих корецепторов, что ограничивает их способность отвечать [33]. Более того, низкие уровни рецептора для фрагмента C3d комплемента (CD21) препятствуют ответам на комплексы полисахарид-комплемент [34]. Вместе эти особенности вносят вклад в притупление гуморальных иммунных ответов с неполным переключением классов иммуноглобулинов [35], хотя генерируются В-клетки памяти [36]. В-клетки новорожденных и младенцев в возрасте до 2 месяцев демонстрируют снижение соматической гипермутации по сравнению со взрослыми, что ограничивает созревание аффинности антител [37].Наконец, стромальные клетки костного мозга в раннем возрасте не способны поддерживать долгосрочную выживаемость плазмобластов и дифференцировку в плазматические клетки, так что любые антитела IgG, вырабатываемые после иммунизации, быстро снижаются, в отличие от детей старшего возраста и взрослых [38]. Следовательно, эффективность адаптивной иммунной системы по раннему ответу на Т-клеточно-зависимые антигены заметно снижена у новорожденных по сравнению с детьми старшего возраста и взрослыми. Это физиологическое поведение особенно актуально для программ вакцинации.Вместе с нарушением врожденного иммунитета слабый ответ Th2 и антител хорошо объясняет, почему неонатальная смертность может быть высокой в условиях повышенного воздействия патогенов.
Это физиологическое поведение особенно актуально для программ вакцинации.Вместе с нарушением врожденного иммунитета слабый ответ Th2 и антител хорошо объясняет, почему неонатальная смертность может быть высокой в условиях повышенного воздействия патогенов.
3. Из детства во взрослую жизнь
Потом нытье школьник с сумкой
И сияющее утреннее лицо, ползет как улитка
В школу нехотя.
Маленький человеческий ребенок, даже когда врожденная и адаптивная иммунные системы начинают созревать, подвергается риску заражения многими патогенными вирусами, бактериями, грибами и паразитами.Тем не менее, у него или нее есть хорошие шансы выжить в развитых странах. До того, как появилось хорошее питание, гигиена и комплексная вакцинация, младенцы и дети младшего возраста страдали от высокой смертности. В 1900 году коэффициент младенческой смертности в Великобритании составлял 140 на 1000, а к 2000 году упал до 7 на 1000 [39]. Это снижение смертности было пропорционально больше у младенцев и детей по сравнению с другими возрастными группами [40]. На лучшую профилактику и контроль инфекций приходится большая часть этой осени. Однако во многих странах уровень младенческой смертности по-прежнему превышает 50 на 1000, что указывает на эволюционное давление, которое должно было привести к выбору работающей защитной иммунной системы.Кроме того, такое давление выбрало крайний генетический полиморфизм в MHC, который благодаря презентации пептидов Т-клеткам и NK-клеткам является ключевым регулятором почти всех иммунных ответов.
В младенчестве иммунная система постепенно созревает. Критически важная ранняя защита от многих инфекционных заболеваний, ранее перенесенных матерью, обеспечивается пассивными антителами IgG, передаваемыми от матери трансплацентарно и с молоком. Как только это исчезнет, маленькие дети станут более уязвимыми к инфекциям, хотя к тому времени они будут лучше вооружены созревающей врожденной и адаптивной иммунной системой. В настоящее время риски значительно снижаются за счет вакцинации, которая стимулирует защитные иммунные реакции в созревающей иммунной системе. Тем не менее, дети все еще могут заразиться вирусными, бактериальными и паразитарными инфекциями, с которыми необходимо бороться и контролировать иммунные реакции. Такая стимуляция антигеном не только способствует выздоровлению, но и приводит к иммунологической памяти [41,42]. Таким образом, со временем защита, обеспечиваемая иммунным ответом, увеличивается, и молодые люди реже страдают от инфекций. Это накопление иммунологической памяти является развивающейся особенностью адаптивного иммунного ответа.Память сохраняется до старости [41], но затем может исчезнуть.
В настоящее время риски значительно снижаются за счет вакцинации, которая стимулирует защитные иммунные реакции в созревающей иммунной системе. Тем не менее, дети все еще могут заразиться вирусными, бактериальными и паразитарными инфекциями, с которыми необходимо бороться и контролировать иммунные реакции. Такая стимуляция антигеном не только способствует выздоровлению, но и приводит к иммунологической памяти [41,42]. Таким образом, со временем защита, обеспечиваемая иммунным ответом, увеличивается, и молодые люди реже страдают от инфекций. Это накопление иммунологической памяти является развивающейся особенностью адаптивного иммунного ответа.Память сохраняется до старости [41], но затем может исчезнуть.
Помимо явных инфекций и прививок, новорожденный подвергается воздействию других антигенов. Он или она происходит из относительно стерильной среды in utero и затем быстро подвергается воздействию множества микробов [43]. Первый серьезный контакт с бактериями происходит во время прохождения через родовые пути, а затем, как только он / она вступает в оральный, кожный и респираторный контакт с окружающей средой. С этого момента воздействие микроорганизмов продолжается.Многие бактерии, колонизирующие кишечник и другие участки слизистой оболочки, необходимы для здорового образа жизни, включая переваривание пищи и получение жизненно важных питательных веществ. Они также влияют на развитие иммунной системы [44].
Примерно 20% всех лимфоцитов находятся в кишечнике [45], подвергаясь воздействию многих возможных чужеродных иммуногенов. Иммунные клетки кишечника контролируют границу с потенциально опасным источником инфекций. Кишечные бактерии влияют на развитие клеток Th27 [46], клеток T reg [47] и Т-клеток памяти [48–50].При рождении почти все Т-клетки несут гликопротеин CD45RA, типичный для наивных Т-клеток, которые никогда не сталкивались с чужеродным антигеном. Кроме того, в CD45RA-негативных CD4 Т-клетках имеется относительно большое количество regs Т . В детстве количество клеток T reg снижается, а клетки памяти Th2, Th27 и Th3 постепенно увеличиваются, чтобы сравняться с количеством наивных Т-клеток [51]. Хотя некоторые из этих Т-клеток памяти могли быть стимулированы инфекциями определенными патогенами и вакцинацией, многие из них могут быть активированы микробиомом не только в кишечнике, но также в дыхательных путях и коже.Эти примированные Т-клетки памяти могут отвечать на последующие инфекции посредством перекрестных реакций [48, 52, 53]. Например, взрослые, которые никогда не контактировали с ВИЧ-1, имеют в своем репертуаре Т-клетки памяти, которые реагируют с пептидами ВИЧ, представленными на клеточной поверхности белками HLA; эти Т-клетки, вероятно, снова пробудятся при возникновении ВИЧ-инфекции [48,50], как и другие микробы [52]. Перекрестная реактивность возникает из-за дискретных коротких (8-15 аминокислот) пептидов (эпитопов), которые входят в пептид-связывающие бороздки на молекулах HLA класса I или II на поверхности клетки и затем распознаются Т-клетками.Внутри последовательностей микробиома существует множество идеальных и почти идеальных совпадений с известными вирусными пептидными эпитопами, например, из ВИЧ-1 [48,50]. Они легко могут быть ответственны за создание Т-клеток памяти, специфичных для эпитопов патогенов, с которыми человек никогда не сталкивался.
В детстве количество клеток T reg снижается, а клетки памяти Th2, Th27 и Th3 постепенно увеличиваются, чтобы сравняться с количеством наивных Т-клеток [51]. Хотя некоторые из этих Т-клеток памяти могли быть стимулированы инфекциями определенными патогенами и вакцинацией, многие из них могут быть активированы микробиомом не только в кишечнике, но также в дыхательных путях и коже.Эти примированные Т-клетки памяти могут отвечать на последующие инфекции посредством перекрестных реакций [48, 52, 53]. Например, взрослые, которые никогда не контактировали с ВИЧ-1, имеют в своем репертуаре Т-клетки памяти, которые реагируют с пептидами ВИЧ, представленными на клеточной поверхности белками HLA; эти Т-клетки, вероятно, снова пробудятся при возникновении ВИЧ-инфекции [48,50], как и другие микробы [52]. Перекрестная реактивность возникает из-за дискретных коротких (8-15 аминокислот) пептидов (эпитопов), которые входят в пептид-связывающие бороздки на молекулах HLA класса I или II на поверхности клетки и затем распознаются Т-клетками.Внутри последовательностей микробиома существует множество идеальных и почти идеальных совпадений с известными вирусными пептидными эпитопами, например, из ВИЧ-1 [48,50]. Они легко могут быть ответственны за создание Т-клеток памяти, специфичных для эпитопов патогенов, с которыми человек никогда не сталкивался.
Сегментированные нитчатые бактерии в кишечнике необходимы для развития клеток Th27 [47] и Clostridium spp. индуцируют клетки T reg толстой кишки [54,55]. У здоровых мышей наблюдаются иммунологические дефекты, в том числе меньшее количество пейеровских бляшек, более мелкие лимфоидные фолликулы и аномальные зародышевые центры в лимфоидной ткани тонкого кишечника [56].Этот иммунодефицит можно скорректировать за несколько дней, добавив одну мышь с нормальной кишечной флорой в клетку с стерильными животными [56,57]. Таким образом, данные на животных подтверждают мнение о том, что микробиом формирует развитие как Т-, так и В-клеток памяти.
Подобные события происходят и для В-клеток. Углеводные антигены групп крови ABO перекрестно реагируют с бактериальными антигенами кишечника и стимулируют ответы антител IgM. Антитела к белку gp41 ВИЧ-1 могут происходить из В-клеток, рецепторы антител которых перекрестно реагируют с белком Escherichia coli [58].
По мере роста ребенка иммунный репертуар также формируется интеркуррентными инфекциями и вакцинациями [59]. Патогенные инфекции могут быть задокументированы по симптоматическим заболеваниям, перенесенным ребенком или взрослым, но для многих вирусов, таких как грипп, инфекция может быть субклинической, но все же достаточной для стимуляции или усиления иммунного ответа [60]. Как правило, защита, обеспечиваемая иммунным ответом, как антителами, так и Т-клетками, очень эффективна. Большинство детских инфекций случаются только один раз, и тогда защита длится всю жизнь.
Поддержание долговременной B-клеточной памяти примечательно, учитывая, что иммуноглобулин IgG имеет период полураспада in vivo около 25 дней [61]. Плазматические клетки, продуцирующие антитела, которые развиваются во время иммунного ответа, мигрируют в костный мозг, где они живут очень долго. Кроме того, может происходить непрерывная регенерация В-клеток памяти, контактирующих с персистирующим антигеном и Т-хелперами. Антигены в виде частиц годами сохраняются в лимфатических узлах, удерживаемых фолликулярными дендритными клетками [62].Персистенция антигена и перекрестно-реактивные антигены, вероятно, помогают поддерживать жизнь этих В-клеток, время от времени делящихся и секретируя антитела.
Примечательно, что мать может передать достаточно антител, чтобы защитить своего ребенка, когда он был инфицирован 20–30 лет назад. Передача защитных антител от матери к ее ребенку чрезвычайно важна, особенно в средах, где 15% или более младенцев и детей умирают от инфекции. Парадоксально, но мать, которая избежала опасной детской инфекции благодаря коллективному иммунитету, может фактически подвергнуть своего ребенка риску, будучи неспособной передавать специфические защитные антитела.
Существует большое количество бессимптомных хронических инфекций, в основном вирусных, которые вызывают иммунные реакции. Примерами являются цитомегаловирус (ЦМВ), вирус Эпштейна-Барра (ВЭБ) и Mycobacterium tubercolosis ( Mtb ), но полный список длинный и продолжает расти [63]. EBV, CMV и Mtb вызывают очень сильные Т-клеточные ответы CD4 и CD8 у людей. ЦМВ-специфический ответ Т-лимфоцитов CD8 может привести к разрастанию олигоклональных Т-клеток, достигающих более 10% циркулирующих Т-лимфоцитов CD8.Эти Т-клетки важны, потому что они контролируют вирус, и их истощение, например, с помощью иммуносупрессивной терапии, может активировать инфекцию (например, Mtb, , EBV, CMV) с разрушительными последствиями.
Эволюция ответов антител в В-лимфоцитах подробно рассмотрена в другом месте [64]. Короче говоря, наивные В-клетки с рецепторами антител, специфическими для иммуногена, связывают антиген в зародышевом центре лимфатических узлов и получают частичный сигнал. Связанный антиген интернализируется и переваривается в лизосомах.Несколько образующихся пептидов связываются с молекулами HLA класса II этой клетки и затем представляются на поверхности клетки, где Т-фолликулярные хелперные клетки с соответствующими Т-клеточными рецепторами отвечают и доставляют дополнительные сигналы, включая IL-21, к В-клетке. Эти сигналы запускают деление В-клеток, переключение классов генов антител и соматическую гипермутацию. В этом случае предпочтение отдается В-клеткам, которые экспрессируют мутировавшие антитела, связывающие иммуноген с более высокой аффинностью. Отбор антител с лучшим связыванием продолжается в течение месяцев, что в конечном итоге приводит к получению антител с высоким сродством из сильно мутировавших генов зародышевой линии.Антитела с высоким сродством более эффективны при нейтрализации или опсонизации вторгшихся микробов и их патогенных продуктов.
Процесс соматической гипермутации не происходит в Т-клетках, даже если они имеют антителоподобные гены рецепторов Т-клеток, потому что наличие высокоаффинного Т-клеточного рецептора не дает никаких преимуществ. Связывание рецептора Т-клетки с комплексом пептид-HLA на антигенпрезентирующих клетках имеет низкое сродство. Он усиливается несколькими парами корецептор-лиганд, которые не являются антиген-специфическими, давая Т-клетке сигнал делиться и функционировать.
Связывание рецептора Т-клетки с комплексом пептид-HLA на антигенпрезентирующих клетках имеет низкое сродство. Он усиливается несколькими парами корецептор-лиганд, которые не являются антиген-специфическими, давая Т-клетке сигнал делиться и функционировать.
В результате иммунного заражения отвечающие Т- и В-клетки могут временно увеличиваться до очень больших количеств [65], иногда более 10% от всех циркулирующих Т-клеток, но они быстро сокращаются в результате активации клеток, индуцированных активацией. смерть и истощение в течение более длительного периода времени. Таким образом, когда патоген контролируется и исчезает, некоторые Т- и В-клетки памяти сохраняются в течение длительного времени в количестве, которое намного превышает количество наивных Т-клеток и Т-клеток «наивной памяти», которые были там до заражения.
По мере того, как человек становится старше, он или она развивает расширяющийся репертуар, включающий Т- и В-клетки памяти, вызванные предыдущими инфекциями и вакцинациями, а также репертуар наивной памяти, сформированный воздействием микробиома, пищевых антигенов и вдыхаемых антигенов. Учитывая большую сложность репертуаров Т- и В-клеток и большой стохастический элемент в выборе того, какие клетки будут реагировать на данный стимул, а также соматические мутации в В-клетках, точный состав будет отличаться у каждого человека, даже у монозиготных близнецов [ 66].Добавьте к этому значительную генетическую изменчивость в реакции людей, определяемую высокополиморфными генами HLA [67] и генами врожденного иммунитета, и неудивительно, что иммунные ответы любого взрослого человека значительно различаются.
(a) Беременность
Подробное изучение иммунологии беременности выходит за рамки настоящего обзора (см. [68,69]). Однако успешное размножение имеет центральное значение в эволюции и имеет иммунологические проблемы.Как новорожденный сохраняет механизмы, с помощью которых плод сводит к минимуму свои иммунные реакции на мать, обсуждалось выше. Еще большей загадкой является то, как мать переносит полуаллогенный трансплантат, не отвергая его и без иммуносупрессии, необходимой для принятия трансплантата органа [70]. На материнском интерфейсе трофобласта в месте первоначальной имплантации и в плаценте есть особенности, которые нарушают нормальный иммунный ответ отторжения трансплантата. К ним относятся экспрессия только неполиморфных неклассических антигенов HLA на трофобласте [71], локальное подавление иммунитета, опосредованное инфильтрацией NK-клеток [72], моноцитов и регуляторных Т-клеток [69,73], а также ингибирование активации Т-клеток. катаболизмом триптофана [74].Примерно во время имплантации местная воспалительная реакция создает стабильный участок плаценты [68]. Есть данные, что мать изменяет баланс своих Т-клеточных ответов на Th3, а не на Th2 [68]. Таким образом, у беременных женщин могут наблюдаться ремиссии аутоиммунного заболевания [75], и они более подвержены тяжелым осложнениям гриппа [76] и некоторых других инфекций. Эта иммунная модуляция, необходимая для благополучия плода, иногда может быть вредной для матери.
Еще большей загадкой является то, как мать переносит полуаллогенный трансплантат, не отвергая его и без иммуносупрессии, необходимой для принятия трансплантата органа [70]. На материнском интерфейсе трофобласта в месте первоначальной имплантации и в плаценте есть особенности, которые нарушают нормальный иммунный ответ отторжения трансплантата. К ним относятся экспрессия только неполиморфных неклассических антигенов HLA на трофобласте [71], локальное подавление иммунитета, опосредованное инфильтрацией NK-клеток [72], моноцитов и регуляторных Т-клеток [69,73], а также ингибирование активации Т-клеток. катаболизмом триптофана [74].Примерно во время имплантации местная воспалительная реакция создает стабильный участок плаценты [68]. Есть данные, что мать изменяет баланс своих Т-клеточных ответов на Th3, а не на Th2 [68]. Таким образом, у беременных женщин могут наблюдаться ремиссии аутоиммунного заболевания [75], и они более подвержены тяжелым осложнениям гриппа [76] и некоторых других инфекций. Эта иммунная модуляция, необходимая для благополучия плода, иногда может быть вредной для матери.
(b) Злокачественные новообразования и аутоиммунитет
Основная роль иммунной системы, вероятно, состоит в защите от инфекций.Другие роли, такие как разрушение мутировавших клеток, могут быть очень важны, но в большей степени в старости после размножения. Многие опухоли отключают Т-клетки, специфичные для опухолевых антигенов, путем связывания с рецепторами «контрольной точки», такими как PD-1 или CTLA4, и новые методы лечения, которые блокируют эти взаимодействия рецептор-лиганд, имеют большой терапевтический потенциал [77,78]. Однако побочные эффекты такой терапии и пассивного переноса противораковых Т-клеток включают аутоиммунные реакции, предполагающие баланс между реакциями против собственного иммунитета, предотвращающими рак и вызывающими аутоиммунитет [79].Во взрослой жизни баланс обычно работает, но у одной трети западных людей развивается рак, обычно в более позднем возрасте, в то время как у 5–10% развивается клиническое аутоиммунное заболевание, поэтому баланс точно установлен и со временем может измениться. Ослабление иммунной системы в пожилом возрасте (см. Ниже) может улучшить аутоиммунитет, но за счет повышенного риска рака.
Ослабление иммунной системы в пожилом возрасте (см. Ниже) может улучшить аутоиммунитет, но за счет повышенного риска рака.
Микроорганизмы вызывают около четверти всех видов рака (например, ВЭБ, вирусы гепатита В и С, вирус папилломы человека и Helicobacter pylori ).Специфические Т-клеточные реакции обычно сдерживают эти микробы. Однако, если иммунитет нарушен в результате старения (см. Ниже), иммуносупрессивной терапии или определенных инфекций, особенно ВИЧ-1, эти виды рака возникают [80].
Таким образом, если в раннем детстве развился полностью эффективный иммунный ответ, он созревает по мере накопления памяти и поддерживает здоровье человека в критические периоды жизни, включая деторождение. Он не только защищает от потенциально смертельных инфекций, но также контролирует ряд устойчивых инфекций, некоторые из которых могут вызвать рак.Он также может иметь дело с мутантными клетками, которые могут стать злокачественными. Он может быть чрезмерно реактивным и вызывать аутоиммунное заболевание или аллергию, что является платой за общую пользу.
4. Снижение иммунитета с возрастом
Последняя сцена из всех,
На этом заканчивается эта странная, насыщенная событиями история,
Это второе ребячество и простое забвение,
Без зубов, без глаз, без вкуса , без всего.
С возрастом иммунная система подвергается глубокому ремоделированию и ухудшению, что существенно влияет на здоровье и выживаемость [81,82].Это иммунное старение предрасполагает пожилых людей к более высокому риску острых вирусных и бактериальных инфекций. Более того, уровень смертности от этих инфекций в три раза выше среди пожилых пациентов по сравнению с более молодыми взрослыми пациентами [83]. Инфекционные заболевания по-прежнему являются четвертой по частоте причиной смерти пожилых людей в развитом мире. Кроме того, аберрантные иммунные ответы у пожилых людей могут усугублять воспаление, возможно, способствуя возникновению других бедствий старости: рака, сердечно-сосудистых заболеваний, инсульта, болезни Альцгеймера и деменции [84].
Во время обычного сезона гриппа около 90% дополнительных смертей происходит среди людей старше 65 лет. Более того, слабый иммунный ответ является причиной снижения эффективности вакцин [82,85]. Иммунное старение также приводит к реактивации латентных вирусов, таких как вирус ветряной оспы, вызывая опоясывающий лишай и хроническую невралгию.
Ухудшение иммунной системы с возрастом может нарушить гомеостатическое равновесие между микробиотой и хозяином. Таким образом, снижение бактериального разнообразия в кишечнике коррелирует с диареей, связанной с Clostridium difficile, , основным осложнением для пожилых людей в больницах [86].Более того, отклонения от профиля кишечной микробиоты, установленного в молодости, связаны с воспалительными заболеваниями кишечника [87]. Увеличение с возрастом количества провоспалительных патобионтов и уменьшение количества иммуномодулирующих видов может способствовать развитию воспалительных заболеваний и поддерживать их [86].
В то же время стареющая иммунная система не может поддерживать полную толерантность к аутоантигенам, что приводит к увеличению числа аутоиммунных заболеваний. [88]. Вероятно, это связано с лимфопенией, возникающей с возрастом, что приводит к избыточной гомеостатической пролиферации лимфоцитов [89], а также к снижению регуляторной функции Т-клеток и уменьшению клиренса апоптотических клеток макрофагами [81].
Рак чаще всего встречается у пожилых людей; средний возраст для диагностики рака в промышленно развитых странах приближается к 70 годам. Основная причина, очевидно, в накоплении клеточных и генетических повреждений на протяжении всей жизни; однако, учитывая роль иммунного ответа в борьбе с раком, снижение иммунных функций у пожилых людей должно способствовать более высокому риску [90]. Это иммунное нарушение явно противоречит увеличению аутоиммунитета, поскольку противоопухолевые реакции могут быть направлены против самого себя; однако, вероятно, преобладает общий упадок иммунной системы, и опухоли больше не отторгаются столь же эффективно. Более того, усиление воспаления, обнаруживаемое с возрастом, способствует возникновению рака.
Более того, усиление воспаления, обнаруживаемое с возрастом, способствует возникновению рака.
Повышенная заболеваемость из-за ослабления иммунной системы является прямым следствием нарушения регуляции адаптивного иммунитета у пожилых людей. Низкое количество наивных Т-лимфоцитов по сравнению с Т-лимфоцитами [41,42] является следствием сниженного выхода тимуса из инволютивного тимуса. Вследствие этой возрастной лимфопении Т-клетки пролиферируют и увеличивают объем «виртуальной памяти» [91], но в то же время способность устанавливать иммунологическую память в ответ на антигены de novo снижается, что ставит под угрозу вакцинацию.Нарушаются такие функции, как продукция цитокинов Т-клетками CD4 и CD8, изменяется экспрессия ключевых поверхностных маркеров, и соотношение CD4 + к CD8 + Т-клеток инвертируется [81]. Расширенные ответы Т-клеток, которые удерживают под контролем латентные вирусы, такие как ВЭБ и ЦМВ, сокращают пространство для Т-клеток CD8 + , специфичных для других потенциально летальных вирусов [92], усугубляемых снижением выработки наивных Т-клеток тимуса.
Хотя количество периферических В-клеток не уменьшается с возрастом, состав этого компартмента меняется.Подобно Т-клеткам, наивные В-клетки заменяются клетками памяти, испытавшими антиген, некоторые из которых «истощены» (CD19 + IgD — CD27 — ), и они демонстрируют пониженное созревание аффинности и переключение изотипа [81 ].
В целом изменения в компартментах Т- и В-клеток препятствуют адекватному иммунному ответу на новые острые и латентные вирусные инфекции и вакцинации.
Врожденный иммунный ответ также снижается с возрастом. Наблюдаются изменения в количестве врожденных клеток со смещением гематопоэза в сторону миелоидных клонов [93,94].Старые нейтрофилы менее функциональны с пониженной фагоцитарной способностью и выработкой супероксида, отчасти из-за снижения экспрессии рецептора Fc γ [95]. Точно так же у стареющих макрофагов снижается респираторный выброс. Вместе с DC они обнаруживают сниженную фагоцитарную функцию и экспрессию HLA II [81]. Таким образом, иммунологическое «молчаливое» удаление апоптозных и возрастающих количеств стареющих клеток ставится под угрозу и может способствовать провоспалительному фенотипу. Действительно, когда у старых мышей искусственно удаляли стареющие клетки, животные жили дольше и были здоровее [96].
Точно так же у стареющих макрофагов снижается респираторный выброс. Вместе с DC они обнаруживают сниженную фагоцитарную функцию и экспрессию HLA II [81]. Таким образом, иммунологическое «молчаливое» удаление апоптозных и возрастающих количеств стареющих клеток ставится под угрозу и может способствовать провоспалительному фенотипу. Действительно, когда у старых мышей искусственно удаляли стареющие клетки, животные жили дольше и были здоровее [96].
Возможно, наиболее важным изменением в стареющей врожденной иммунной системе является увеличение провоспалительных цитокинов IL-1β, IL-6, IL-18 и TNFα [97]. Возникающее в результате воспаление низкой степени, вероятно, способствует атеросклерозу, деменции и раку, неразрывно связывая воспаление и старение других тканей [84,98].
Клеточные и молекулярные основы иммунного старения еще недостаточно изучены. Три фенотипа характеризуют стареющие клетки: истощение теломер, сопровождающее каждый раунд пролиферации, ведущее к остановке деления клеток или «репликативному старению»; повышенная митохондриальная нагрузка / дисфункция и активные формы кислорода; и секреторный фенотип, связанный со старением (SASP), определяемый как секреция провоспалительных цитокинов, хемокинов и протеаз стареющими клетками [99].Хотя большинство данных было получено на фибробластах, стареющие иммунные клетки, вероятно, обладают схожими характеристиками. Эти свойства влияют на митотически активные клетки путем истощения или остановки деления (например, гемопоэтические стволовые клетки — HSC или Т-клетки), а также на постмитотические иммунные клетки, вызывая клеточную дисфункцию (например, нейтрофилов).
Истощение теломер является защитным механизмом против рака, так как каждый раунд пролиферации может вносить мутации [100]. Только эпителиальные лимфоциты и стволовые клетки, включая гемопоэтические (HSC), экспрессируют удлиняющий теломеры фермент теломеразу у взрослых [101], что требует тщательного баланса с риском рака.Как Т-клетки памяти, так и HSC обычно делятся редко, чтобы минимизировать истощение теломер, но надежно либо в ответ на инфекцию (лимфоциты памяти), либо для обновления тканей (стволовые клетки) на протяжении всей жизни. На конечной стадии стареющие CD27 — CD28 — Т-клетки имеют самые короткие теломеры и демонстрируют сниженную пролиферацию после активации, но тем не менее обладают мощными эффекторными функциями. Эти клетки накапливаются в пожилом возрасте и у пациентов с аутоиммунными заболеваниями и хроническими вирусными инфекциями [102].Вторая характеристика старых клеток — усиление митохондриальной дисфункции и, как следствие, окислительное повреждение белков и ДНК. Функция DC у старых мышей может быть восстановлена путем введения антиоксидантов [103]. Окислительный стресс вызывает разрывы ДНК и может быть причиной истощения теломер, которое связывает первые две причины старения. Накопление окислительного повреждения может быть связано со снижением лизосомальной функции и аутофагии [104]. Аутофагия, разрушающая объем цитоплазматического материала путем доставки его к лизосомам, снижается с возрастом, в том числе в человеческих CD8 + Т-клетках [105].Мыши без аутофагии в их кроветворной системе обнаруживают преждевременно состарившуюся кроветворную систему [106]. Отсутствие реакции Т-клеток памяти на вакцинацию против гриппа, наблюдаемую у пожилых людей, можно восстановить с помощью соединения, индуцирующего аутофагию [107]. Третьим более недавним дополнением к этим фундаментальным изменениям старых клеток является приобретение SASP, способствующего повышенной секреции провоспалительных цитокинов и слабому воспалению [99].
На конечной стадии стареющие CD27 — CD28 — Т-клетки имеют самые короткие теломеры и демонстрируют сниженную пролиферацию после активации, но тем не менее обладают мощными эффекторными функциями. Эти клетки накапливаются в пожилом возрасте и у пациентов с аутоиммунными заболеваниями и хроническими вирусными инфекциями [102].Вторая характеристика старых клеток — усиление митохондриальной дисфункции и, как следствие, окислительное повреждение белков и ДНК. Функция DC у старых мышей может быть восстановлена путем введения антиоксидантов [103]. Окислительный стресс вызывает разрывы ДНК и может быть причиной истощения теломер, которое связывает первые две причины старения. Накопление окислительного повреждения может быть связано со снижением лизосомальной функции и аутофагии [104]. Аутофагия, разрушающая объем цитоплазматического материала путем доставки его к лизосомам, снижается с возрастом, в том числе в человеческих CD8 + Т-клетках [105].Мыши без аутофагии в их кроветворной системе обнаруживают преждевременно состарившуюся кроветворную систему [106]. Отсутствие реакции Т-клеток памяти на вакцинацию против гриппа, наблюдаемую у пожилых людей, можно восстановить с помощью соединения, индуцирующего аутофагию [107]. Третьим более недавним дополнением к этим фундаментальным изменениям старых клеток является приобретение SASP, способствующего повышенной секреции провоспалительных цитокинов и слабому воспалению [99].
5. Эволюция иммунной системы человека
Будучи долгоживущими видами, люди развили механизмы врожденного иммунитета и иммунологической памяти, чтобы выжить при повторных инфекциях.Однако на протяжении жизни человека эти иммунные механизмы изменяются, сначала для адаптации к переходу от плода к младенцу, а затем к созреванию и расширению во время роста, слегка изменяясь во время беременности и, наконец, уменьшаясь в процессе старения. Выход наивных лимфоидных клеток и способность формировать новую иммунологическую память становятся все менее важными, поскольку пожилой человек столкнется и установит банк памяти для многих патогенов в течение своей жизни.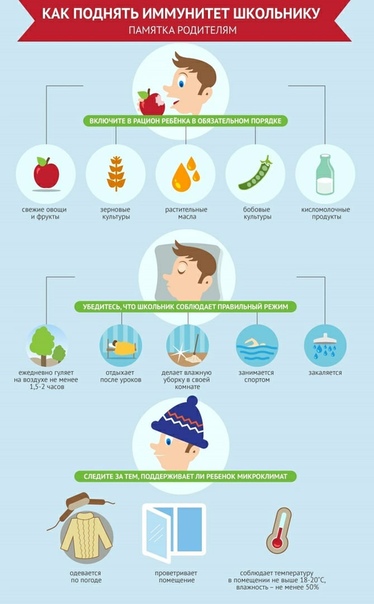 Существует вероятность того, что миелоидный сдвиг и повышенная секреция провоспалительных цитокинов во время старения важны для улучшения фагоцитоза увеличивающегося числа стареющих клеток, что поднимает вопрос о том, могут ли изменения в стареющей иммунной системе служить цели.
Существует вероятность того, что миелоидный сдвиг и повышенная секреция провоспалительных цитокинов во время старения важны для улучшения фагоцитоза увеличивающегося числа стареющих клеток, что поднимает вопрос о том, могут ли изменения в стареющей иммунной системе служить цели.
Иммунная система была в первую очередь сформирована эволюцией, чтобы эффективно реагировать на острые инфекции у молодых людей, адаптироваться к беременности и передавать защиту младенцам, а также адаптирована для борьбы со многими хроническими инфекциями, длящимися десятилетиями. Помимо борьбы с вирусами, бактериями, грибками и паразитами, иммунная система также берет на себя другие функции, такие как восстановление тканей, заживление ран, удаление мертвых и раковых клеток и формирование здоровой микробиоты кишечника. Предполагая отсутствие серьезного избирательного давления на людей старше репродуктивного возраста, нам, возможно, придется платить за генетические черты, выбранные для обеспечения приспособленности в раннем возрасте, за счет более позднего развития иммунологических фенотипов, таких как хроническое воспаление.Массовое старение и повышенная долговечность — это недавние явления, происходящие в оптимизированной среде. Как предположил Хейфлик [108], старение может быть артефактом цивилизации, и, следовательно, изменения в стареющей иммунной системе могут быть просто следствием эволюционного непредсказуемого воздействия антигена на протяжении всей жизни человека.
В некоторых аспектах иммунная система пожилого организма напоминает иммунную систему новорожденного, со сниженной антимикробной активностью нейтрофилов и макрофагов, сниженной презентацией антигена DC и уменьшенным уничтожением NK, а также несколько нарушенными адаптивными ответами лимфоцитов.Таким образом, как очень молодая, так и старая иммунная система одинаково подвержены риску справиться с типичной вирусной инфекцией, такой как грипп, тогда как молодой (небеременный) взрослый организм, по-видимому, идеально подходит для этой задачи (). Эволюция иммунной системы внутри индивидуума, возможно, отражает центральную роль молодого взрослого человека в выживании вида благодаря его репродуктивному потенциалу.
Эволюция иммунной системы внутри индивидуума, возможно, отражает центральную роль молодого взрослого человека в выживании вида благодаря его репродуктивному потенциалу.
Эволюция иммунной системы человека от младенчества до старости
Резюме
В этой статье рассматривается развитие иммунного ответа в неонатальном, младенческом и взрослом возрасте, включая беременность, заканчивающуюся спадом в пожилом возрасте.Возникает картина ребенка, рожденного с незрелой, врожденной и адаптивной иммунной системой, которая созревает и приобретает память по мере его роста. Затем в старости он приходит в упадок. Эти изменения рассматриваются наряду с рисками различных типов инфекций, аутоиммунных заболеваний и злокачественных новообразований.
Ключевые слова: адаптивный иммунитет, врожденный иммунитет, инфекции
1. Введение
И один человек в свое время играет много ролей,
Его деяниям семь возрастов.
Более 1600 генов участвуют в врожденных и адаптивных иммунных ответах [1]. Эти гены имеют большое значение для поддержания жизни во враждебной среде. Тем не менее, иммунная система является относительно незрелой при рождении и должна развиваться в течение жизни, подвергаясь воздействию множества внешних проблем в детстве, в молодом и зрелом возрасте (включая беременность), до упадка старости ().
( a ) Семь возрастов женщины. ( b ) Схематический график дополнительных смертей от сезонного или пандемического гриппа на протяжении жизни человека, представленный как число смертей на 1000 человек (адаптировано из [2]).Обратите внимание, что хотя беременность увеличивает риск тяжелого гриппа, во время тяжелых пандемий, таких как 1918/1919 гг., Также наблюдались избыточные смертельные случаи среди ранее здоровых молодых людей, которые не были беременными. ( c ) Схематический график различных звеньев иммунного ответа на грипп на протяжении жизни человека.
2. Онтогенез иммунной системы в молодом возрасте
Сначала младенец,
Мычание и рвота в руках медсестры.
In utero среда плода требует, чтобы иммунная система оставалась толерантной к материнским аллоантигенам.После рождения внезапное колоссальное воздействие антигенов окружающей среды, многие из которых происходят из кишечных комменсальных бактерий, требует быстрых изменений, чтобы вызвать определенные иммунные реакции, соответствующие раннему возрасту.
(a) Врожденная иммунная система
Врожденная иммунная система обеспечивает раннюю первую линию защиты от вторжения патогенов. Вовлеченные клетки — нейтрофилы, моноциты, макрофаги и дендритные клетки, которые все взаимодействуют с адаптивной иммунной системой. Эти клетки развиваются и созревают в течение жизни плода, но в разное время, и функция всех компонентов врожденного иммунитета у новорожденных слабее по сравнению с более поздней жизнью.
Зрелые нейтрофилы присутствуют в конце первого триместра и резко увеличиваются в количестве, стимулируемые гранулоцитарно-колониестимулирующим фактором, незадолго до рождения. Затем их количество возвращается к стабильному уровню в течение нескольких дней, но они демонстрируют слабую бактерицидную функцию, слабую реакцию на воспалительные стимулы, снижение адгезии к эндотелиальным клеткам и уменьшение хемотаксиса [3]. Эти дефициты более заметны у недоношенных детей, у которых также ниже сывороточный IgG и комплемент. Следовательно, новорожденные, и особенно недоношенные, имеют нарушенные функции нейтрофилов [4], что подвергает ребенка риску бактериальных инфекций.
У недоношенных и новорожденных классические моноциты и макрофаги также являются незрелыми. У них снижена экспрессия TLR4 [5] с нарушением врожденных сигнальных путей [6-8], что приводит к снижению цитокиновых ответов по сравнению со взрослыми. Следовательно, происходит плохое восстановление тканей, нарушенный фагоцитоз потенциальных патогенов и плохая секреция биоактивных молекул. Однако, хотя частота макрофагов в легких у недоношенных и доношенных детей снижается, уровни этих клеток у взрослых достигаются в течение нескольких дней после рождения [9].
Однако, хотя частота макрофагов в легких у недоношенных и доношенных детей снижается, уровни этих клеток у взрослых достигаются в течение нескольких дней после рождения [9].
По сравнению с кровью детей или взрослых, пуповинная кровь содержит меньше дендритных клеток миелоидного типа (mDC). Они экспрессируют более низкие уровни HLA класса II, CD80 и CD86 на клеточной поверхности, чем взрослые mDC [10]. Они секретируют низкие концентрации IL-12p70 в ответ на активацию врожденных стимулов [11]. Таким образом, праймирование Т-клеточных ответов Th2 и CD8 снижено по сравнению со взрослыми, что коррелирует с повышенной восприимчивостью к инфекциям, вызываемым вирусами Mycobacterium tuberculosis и Salmonella spp . Напротив, новорожденные mDC, стимулированные с помощью TLR4, секретируют подобные взрослым концентрации провоспалительных цитокинов [12], которые способствуют иммунным ответам Th27.
Плазмацитоидные дендритные клетки (pDC) выделяют высокие концентрации интерферона I типа (IFN) в ответ на стимуляцию TLR7 и TLR9 у взрослых. Однако новорожденные pDC строго ограничены в секрете интерферона α / β при воздействии различных вирусов, несмотря на то, что уровни экспрессии TLR7 и TLR9 аналогичны взрослым [13]. Следовательно, врожденные иммунные ответы на вирусы, такие как респираторно-синцитиальный вирус, вирус простого герпеса и цитомегаловирус, являются слабыми по сравнению с более поздними периодами жизни.
Естественные киллерные (NK) клетки у взрослых сдерживают репликацию и распространение вируса до установления адаптивного иммунитета [14]. Они регулируются ингибирующими рецепторами, которые распознают HLA-A, B, C и E, и, следовательно, способствуют самотолерантности. На ранних сроках беременности NK-клетки гипочувствительны к клеткам-мишеням, лишенным молекул класса I главного комплекса гистосовместимости (MHC) (таких как трофобласт [15]), и очень чувствительны к подавлению иммунитета за счет трансформирующего фактора роста-β (TGF-β). Цитолитическая функция NK увеличивается во время беременности, но при рождении все еще составляет лишь половину от взрослого уровня. Новорожденные NK-клетки менее чувствительны к активации IL-2 и IL-15 и продуцируют ограниченные концентрации IFN-γ. Однако порог активации клеток ниже, что обеспечивает некоторую противовирусную защиту [15].
Цитолитическая функция NK увеличивается во время беременности, но при рождении все еще составляет лишь половину от взрослого уровня. Новорожденные NK-клетки менее чувствительны к активации IL-2 и IL-15 и продуцируют ограниченные концентрации IFN-γ. Однако порог активации клеток ниже, что обеспечивает некоторую противовирусную защиту [15].
Три независимых пути, которые активируют систему комплемента, имеют решающее значение для защиты хозяина и воспаления. Компоненты комплемента способствуют опсонизации, являются хемоаттрактантами для врожденных клеток, опосредуют лизис клеток и влияют на выработку антител.Концентрация почти всех циркулирующих компонентов в сыворотке новорожденных на 10–80% ниже, чем у взрослых [16], при пониженной биологической активности. Уровни комплемента повышаются после рождения, при этом некоторые сывороточные факторы достигают концентрации у взрослых в течение месяца (например, фактор B), но другие развиваются медленнее [16]. Поскольку у младенцев низкая концентрация иммуноглобулина, эффекторные функции комплемента зависят от альтернативных путей активации и лектин-связывающей активации, запускаемых полисахаридами и эндотоксинами.
В целом, врожденная иммунная система при рождении приглушена, цена, вероятно, заплачена плодом не только за переносимость необщих материнских антигенов, но и за игнорирование значительного стресса и ремоделирования, которые происходят во время развития.Это делает новорожденного, особенно недоношенного, относительно восприимчивым к бактериальным и вирусным инфекциям.
(b) Адаптивная иммунная система
Т-клетки развиваются в тимусе, который является самым большим при рождении и в течение первых лет жизни. Зрелые единичные CD4 + и CD8 + положительные Т-клетки впервые обнаруживаются в тимусе на 15 неделе и в большом количестве на периферии задолго до рождения [17,18]. Однако неонатальные Т-клетки значительно отличаются от взрослых клеток, отражая жизнь плода, где воздействие чужеродных антигенов в значительной степени ограничивается ненаследственными материнскими аллоантигенами. Функция ранних Т-клеток отличается от взрослых Т-клеток. Например, хотя наивные CD4 + Т-клетки плода сильно реагируют на аллоантигены, они имеют тенденцию развиваться в направлении Foxp3 + CD25 + регуляторных Т-клеток (T reg ) под влиянием TGF-β [19], и таким образом активно продвигают терпимость к себе. Периферические Т reg составляют около 3% от общего количества CD4 + Т-клеток при рождении [20], и эти клетки сохраняются в течение длительного периода времени [21], придавая иммунному ответу в раннем возрасте противовоспалительный профиль [22 ].
Функция ранних Т-клеток отличается от взрослых Т-клеток. Например, хотя наивные CD4 + Т-клетки плода сильно реагируют на аллоантигены, они имеют тенденцию развиваться в направлении Foxp3 + CD25 + регуляторных Т-клеток (T reg ) под влиянием TGF-β [19], и таким образом активно продвигают терпимость к себе. Периферические Т reg составляют около 3% от общего количества CD4 + Т-клеток при рождении [20], и эти клетки сохраняются в течение длительного периода времени [21], придавая иммунному ответу в раннем возрасте противовоспалительный профиль [22 ].
Активация чужеродным антигеном поздних эмбриональных или неонатальных Т-клеток приводит к ответу, искаженному в сторону иммунитета Th3 [23], который усиливается неонатальными дендритными клетками и эпигенетическими особенностями [24,25]. Таким образом, очень ранний адаптивный Т-клеточный иммунитет характеризуется толерогенной реактивностью, сниженным распознаванием алло-антигена и слабыми ответами на чужеродные антигены.
У новорожденных, помимо обычных Т-клеток, которые распознают пептидные антигены в контексте классических молекул MHC, существуют популяции γδ Т-клеточных рецепторов (TCR) -позитивных и врожденных-подобных αβ-TCR-позитивных Т-клеток.К ним относятся функционально компетентные клетки iNKT, которые быстро продуцируют IFN, ассоциированные со слизистой оболочкой инвариантные Т-клетки (MAIT) [26] и недавно описанные интерлейкин-8 (CXCL8) -секретирующие наивные Т-клетки, которые связывают врожденный и адаптивный иммунитет [27]. Клетки MAIT развиваются в тимусе, но их созревание может происходить в тканях слизистой оболочки плода до микробной колонизации. Т-клетки, продуцирующие CXCL8, производят важные эффекторные функции у новорожденных людей, поскольку они обладают потенциалом активации антимикробных нейтрофилов и γδ Т-клеток.Они, по-видимому, особенно активны на барьерах слизистой оболочки недоношенных и доношенных детей, хотя их частота уменьшается с возрастом. В отличие от взрослой крови, где репертуар γδ TCR ограничен, γδ T-клетки неонатальной крови обнаруживают множество комбинаций рецепторных цепей, которые меняются с беременностью [27]. γδ Т-клетки могут продуцировать значительные количества IFN-γ после кратковременной поликлональной стимуляции, компенсируя незрелость более классического ответа Т-клеток Th2-типа на неонатальные инфекции [28,29].
В отличие от взрослой крови, где репертуар γδ TCR ограничен, γδ T-клетки неонатальной крови обнаруживают множество комбинаций рецепторных цепей, которые меняются с беременностью [27]. γδ Т-клетки могут продуцировать значительные количества IFN-γ после кратковременной поликлональной стимуляции, компенсируя незрелость более классического ответа Т-клеток Th2-типа на неонатальные инфекции [28,29].
Два типа В-клеток возникают через разные пути развития [30]. Клетки B1 спонтанно секретируют низкоаффинный IgM с ограниченным диапазоном антигенной специфичности (включая обычные бактериальные полисахариды), имеют меньше соматических мутаций и служат первой линией защиты [31]. Клетки B1 секретируют IL-10 и TGF-β и, таким образом, способствуют ответу Th3. При рождении B1-клетки составляют 40% B-клеток периферической крови, и эта частота остается высокой в течение нескольких месяцев [32]. Обычные В-клетки (обозначенные как клетки В2) происходят из многолинейного общего лимфоидного предшественника CD34 + и генерируют широкий репертуар иммуноглобулиновой специфичности благодаря экспрессии терминальной дезоксинуклеотидилтрансферазы, которая увеличивает разнообразие в присоединении сегментов гена иммуноглобулина V-D-J.В-клетки обычно присутствуют во вторичных лимфоидных органах и в костном мозге, где они вносят вклад в гуморальный ответ адаптивной иммунной системы.
Большинство ответов антител, в том числе на бактериальные белки, бактериальные полисахариды и на полисахаридно-белковые конъюгированные вакцины, зависят от помощи Т-клеток. Они полагаются на взаимодействие между TCR и участие корецепторов, включая CD28 и лиганд CD40, на Th3 или фолликулярных Т-хелперных клетках с их соответствующими партнерами по связыванию HLA-пептидом, CD80 / 86 и CD40 на антиген-специфических В-клетках.Однако неонатальные В-клетки экспрессируют низкие уровни этих корецепторов, что ограничивает их способность отвечать [33]. Более того, низкие уровни рецептора для фрагмента C3d комплемента (CD21) препятствуют ответам на комплексы полисахарид-комплемент [34]. Вместе эти особенности вносят вклад в притупление гуморальных иммунных ответов с неполным переключением классов иммуноглобулинов [35], хотя генерируются В-клетки памяти [36]. В-клетки новорожденных и младенцев в возрасте до 2 месяцев демонстрируют снижение соматической гипермутации по сравнению со взрослыми, что ограничивает созревание аффинности антител [37].Наконец, стромальные клетки костного мозга в раннем возрасте не способны поддерживать долгосрочную выживаемость плазмобластов и дифференцировку в плазматические клетки, так что любые антитела IgG, вырабатываемые после иммунизации, быстро снижаются, в отличие от детей старшего возраста и взрослых [38]. Следовательно, эффективность адаптивной иммунной системы по раннему ответу на Т-клеточно-зависимые антигены заметно снижена у новорожденных по сравнению с детьми старшего возраста и взрослыми. Это физиологическое поведение особенно актуально для программ вакцинации.Вместе с нарушением врожденного иммунитета слабый ответ Th2 и антител хорошо объясняет, почему неонатальная смертность может быть высокой в условиях повышенного воздействия патогенов.
Вместе эти особенности вносят вклад в притупление гуморальных иммунных ответов с неполным переключением классов иммуноглобулинов [35], хотя генерируются В-клетки памяти [36]. В-клетки новорожденных и младенцев в возрасте до 2 месяцев демонстрируют снижение соматической гипермутации по сравнению со взрослыми, что ограничивает созревание аффинности антител [37].Наконец, стромальные клетки костного мозга в раннем возрасте не способны поддерживать долгосрочную выживаемость плазмобластов и дифференцировку в плазматические клетки, так что любые антитела IgG, вырабатываемые после иммунизации, быстро снижаются, в отличие от детей старшего возраста и взрослых [38]. Следовательно, эффективность адаптивной иммунной системы по раннему ответу на Т-клеточно-зависимые антигены заметно снижена у новорожденных по сравнению с детьми старшего возраста и взрослыми. Это физиологическое поведение особенно актуально для программ вакцинации.Вместе с нарушением врожденного иммунитета слабый ответ Th2 и антител хорошо объясняет, почему неонатальная смертность может быть высокой в условиях повышенного воздействия патогенов.
3. Из детства во взрослую жизнь
Потом нытье школьник с сумкой
И сияющее утреннее лицо, ползет как улитка
В школу нехотя.
Маленький человеческий ребенок, даже когда врожденная и адаптивная иммунные системы начинают созревать, подвергается риску заражения многими патогенными вирусами, бактериями, грибами и паразитами.Тем не менее, у него или нее есть хорошие шансы выжить в развитых странах. До того, как появилось хорошее питание, гигиена и комплексная вакцинация, младенцы и дети младшего возраста страдали от высокой смертности. В 1900 году коэффициент младенческой смертности в Великобритании составлял 140 на 1000, а к 2000 году упал до 7 на 1000 [39]. Это снижение смертности было пропорционально больше у младенцев и детей по сравнению с другими возрастными группами [40]. На лучшую профилактику и контроль инфекций приходится большая часть этой осени. Однако во многих странах уровень младенческой смертности по-прежнему превышает 50 на 1000, что указывает на эволюционное давление, которое должно было привести к выбору работающей защитной иммунной системы.Кроме того, такое давление выбрало крайний генетический полиморфизм в MHC, который благодаря презентации пептидов Т-клеткам и NK-клеткам является ключевым регулятором почти всех иммунных ответов.
На лучшую профилактику и контроль инфекций приходится большая часть этой осени. Однако во многих странах уровень младенческой смертности по-прежнему превышает 50 на 1000, что указывает на эволюционное давление, которое должно было привести к выбору работающей защитной иммунной системы.Кроме того, такое давление выбрало крайний генетический полиморфизм в MHC, который благодаря презентации пептидов Т-клеткам и NK-клеткам является ключевым регулятором почти всех иммунных ответов.
В младенчестве иммунная система постепенно созревает. Критически важная ранняя защита от многих инфекционных заболеваний, ранее перенесенных матерью, обеспечивается пассивными антителами IgG, передаваемыми от матери трансплацентарно и с молоком. Как только это исчезнет, маленькие дети станут более уязвимыми к инфекциям, хотя к тому времени они будут лучше вооружены созревающей врожденной и адаптивной иммунной системой.В настоящее время риски значительно снижаются за счет вакцинации, которая стимулирует защитные иммунные реакции в созревающей иммунной системе. Тем не менее, дети все еще могут заразиться вирусными, бактериальными и паразитарными инфекциями, с которыми необходимо бороться и контролировать иммунные реакции. Такая стимуляция антигеном не только способствует выздоровлению, но и приводит к иммунологической памяти [41,42]. Таким образом, со временем защита, обеспечиваемая иммунным ответом, увеличивается, и молодые люди реже страдают от инфекций. Это накопление иммунологической памяти является развивающейся особенностью адаптивного иммунного ответа.Память сохраняется до старости [41], но затем может исчезнуть.
Помимо явных инфекций и прививок, новорожденный подвергается воздействию других антигенов. Он или она происходит из относительно стерильной среды in utero и затем быстро подвергается воздействию множества микробов [43]. Первый серьезный контакт с бактериями происходит во время прохождения через родовые пути, а затем, как только он / она вступает в оральный, кожный и респираторный контакт с окружающей средой.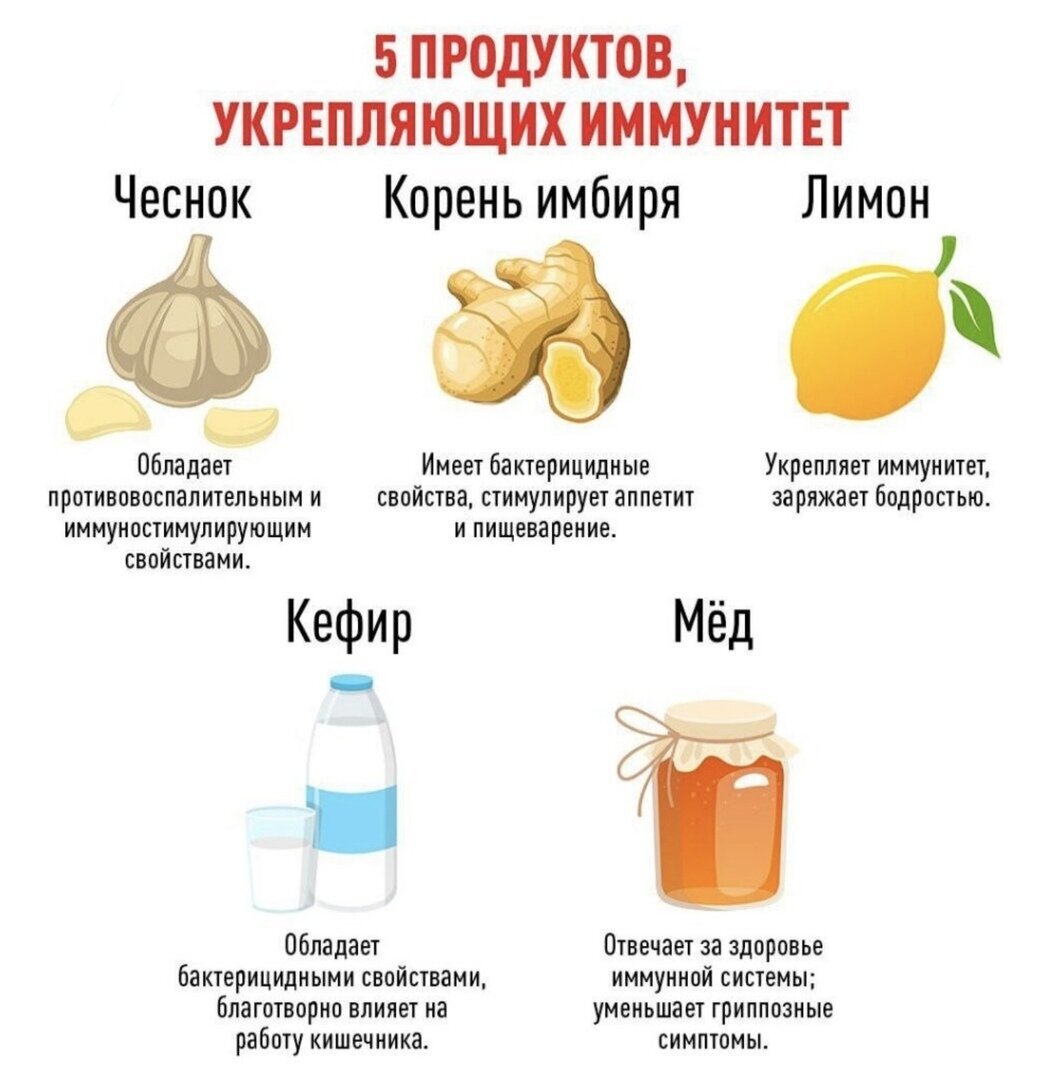 С этого момента воздействие микроорганизмов продолжается.Многие бактерии, колонизирующие кишечник и другие участки слизистой оболочки, необходимы для здорового образа жизни, включая переваривание пищи и получение жизненно важных питательных веществ. Они также влияют на развитие иммунной системы [44].
С этого момента воздействие микроорганизмов продолжается.Многие бактерии, колонизирующие кишечник и другие участки слизистой оболочки, необходимы для здорового образа жизни, включая переваривание пищи и получение жизненно важных питательных веществ. Они также влияют на развитие иммунной системы [44].
Примерно 20% всех лимфоцитов находятся в кишечнике [45], подвергаясь воздействию многих возможных чужеродных иммуногенов. Иммунные клетки кишечника контролируют границу с потенциально опасным источником инфекций. Кишечные бактерии влияют на развитие клеток Th27 [46], клеток T reg [47] и Т-клеток памяти [48–50].При рождении почти все Т-клетки несут гликопротеин CD45RA, типичный для наивных Т-клеток, которые никогда не сталкивались с чужеродным антигеном. Кроме того, в CD45RA-негативных CD4 Т-клетках имеется относительно большое количество regs Т . В детстве количество клеток T reg снижается, а клетки памяти Th2, Th27 и Th3 постепенно увеличиваются, чтобы сравняться с количеством наивных Т-клеток [51]. Хотя некоторые из этих Т-клеток памяти могли быть стимулированы инфекциями определенными патогенами и вакцинацией, многие из них могут быть активированы микробиомом не только в кишечнике, но также в дыхательных путях и коже.Эти примированные Т-клетки памяти могут отвечать на последующие инфекции посредством перекрестных реакций [48, 52, 53]. Например, взрослые, которые никогда не контактировали с ВИЧ-1, имеют в своем репертуаре Т-клетки памяти, которые реагируют с пептидами ВИЧ, представленными на клеточной поверхности белками HLA; эти Т-клетки, вероятно, снова пробудятся при возникновении ВИЧ-инфекции [48,50], как и другие микробы [52]. Перекрестная реактивность возникает из-за дискретных коротких (8-15 аминокислот) пептидов (эпитопов), которые входят в пептид-связывающие бороздки на молекулах HLA класса I или II на поверхности клетки и затем распознаются Т-клетками.Внутри последовательностей микробиома существует множество идеальных и почти идеальных совпадений с известными вирусными пептидными эпитопами, например, из ВИЧ-1 [48,50]. Они легко могут быть ответственны за создание Т-клеток памяти, специфичных для эпитопов патогенов, с которыми человек никогда не сталкивался.
Они легко могут быть ответственны за создание Т-клеток памяти, специфичных для эпитопов патогенов, с которыми человек никогда не сталкивался.
Сегментированные нитчатые бактерии в кишечнике необходимы для развития клеток Th27 [47] и Clostridium spp. индуцируют клетки T reg толстой кишки [54,55]. У здоровых мышей наблюдаются иммунологические дефекты, в том числе меньшее количество пейеровских бляшек, более мелкие лимфоидные фолликулы и аномальные зародышевые центры в лимфоидной ткани тонкого кишечника [56].Этот иммунодефицит можно скорректировать за несколько дней, добавив одну мышь с нормальной кишечной флорой в клетку с стерильными животными [56,57]. Таким образом, данные на животных подтверждают мнение о том, что микробиом формирует развитие как Т-, так и В-клеток памяти.
Подобные события происходят и для В-клеток. Углеводные антигены групп крови ABO перекрестно реагируют с бактериальными антигенами кишечника и стимулируют ответы антител IgM. Антитела к белку gp41 ВИЧ-1 могут происходить из В-клеток, рецепторы антител которых перекрестно реагируют с белком Escherichia coli [58].
По мере роста ребенка иммунный репертуар также формируется интеркуррентными инфекциями и вакцинациями [59]. Патогенные инфекции могут быть задокументированы по симптоматическим заболеваниям, перенесенным ребенком или взрослым, но для многих вирусов, таких как грипп, инфекция может быть субклинической, но все же достаточной для стимуляции или усиления иммунного ответа [60]. Как правило, защита, обеспечиваемая иммунным ответом, как антителами, так и Т-клетками, очень эффективна. Большинство детских инфекций случаются только один раз, и тогда защита длится всю жизнь.
Поддержание долговременной B-клеточной памяти примечательно, учитывая, что иммуноглобулин IgG имеет период полураспада in vivo около 25 дней [61]. Плазматические клетки, продуцирующие антитела, которые развиваются во время иммунного ответа, мигрируют в костный мозг, где они живут очень долго. Кроме того, может происходить непрерывная регенерация В-клеток памяти, контактирующих с персистирующим антигеном и Т-хелперами. Антигены в виде частиц годами сохраняются в лимфатических узлах, удерживаемых фолликулярными дендритными клетками [62].Персистенция антигена и перекрестно-реактивные антигены, вероятно, помогают поддерживать жизнь этих В-клеток, время от времени делящихся и секретируя антитела.
Примечательно, что мать может передать достаточно антител, чтобы защитить своего ребенка, когда он был инфицирован 20–30 лет назад. Передача защитных антител от матери к ее ребенку чрезвычайно важна, особенно в средах, где 15% или более младенцев и детей умирают от инфекции. Парадоксально, но мать, которая избежала опасной детской инфекции благодаря коллективному иммунитету, может фактически подвергнуть своего ребенка риску, будучи неспособной передавать специфические защитные антитела.
Существует большое количество бессимптомных хронических инфекций, в основном вирусных, которые вызывают иммунные реакции. Примерами являются цитомегаловирус (ЦМВ), вирус Эпштейна-Барра (ВЭБ) и Mycobacterium tubercolosis ( Mtb ), но полный список длинный и продолжает расти [63]. EBV, CMV и Mtb вызывают очень сильные Т-клеточные ответы CD4 и CD8 у людей. ЦМВ-специфический ответ Т-лимфоцитов CD8 может привести к разрастанию олигоклональных Т-клеток, достигающих более 10% циркулирующих Т-лимфоцитов CD8.Эти Т-клетки важны, потому что они контролируют вирус, и их истощение, например, с помощью иммуносупрессивной терапии, может активировать инфекцию (например, Mtb, , EBV, CMV) с разрушительными последствиями.
Эволюция ответов антител в В-лимфоцитах подробно рассмотрена в другом месте [64]. Короче говоря, наивные В-клетки с рецепторами антител, специфическими для иммуногена, связывают антиген в зародышевом центре лимфатических узлов и получают частичный сигнал. Связанный антиген интернализируется и переваривается в лизосомах.Несколько образующихся пептидов связываются с молекулами HLA класса II этой клетки и затем представляются на поверхности клетки, где Т-фолликулярные хелперные клетки с соответствующими Т-клеточными рецепторами отвечают и доставляют дополнительные сигналы, включая IL-21, к В-клетке. Эти сигналы запускают деление В-клеток, переключение классов генов антител и соматическую гипермутацию. В этом случае предпочтение отдается В-клеткам, которые экспрессируют мутировавшие антитела, связывающие иммуноген с более высокой аффинностью. Отбор антител с лучшим связыванием продолжается в течение месяцев, что в конечном итоге приводит к получению антител с высоким сродством из сильно мутировавших генов зародышевой линии.Антитела с высоким сродством более эффективны при нейтрализации или опсонизации вторгшихся микробов и их патогенных продуктов.
Процесс соматической гипермутации не происходит в Т-клетках, даже если они имеют антителоподобные гены рецепторов Т-клеток, потому что наличие высокоаффинного Т-клеточного рецептора не дает никаких преимуществ. Связывание рецептора Т-клетки с комплексом пептид-HLA на антигенпрезентирующих клетках имеет низкое сродство. Он усиливается несколькими парами корецептор-лиганд, которые не являются антиген-специфическими, давая Т-клетке сигнал делиться и функционировать.
В результате иммунного заражения отвечающие Т- и В-клетки могут временно увеличиваться до очень больших количеств [65], иногда более 10% от всех циркулирующих Т-клеток, но они быстро сокращаются в результате активации клеток, индуцированных активацией. смерть и истощение в течение более длительного периода времени. Таким образом, когда патоген контролируется и исчезает, некоторые Т- и В-клетки памяти сохраняются в течение длительного времени в количестве, которое намного превышает количество наивных Т-клеток и Т-клеток «наивной памяти», которые были там до заражения.
По мере того, как человек становится старше, он или она развивает расширяющийся репертуар, включающий Т- и В-клетки памяти, вызванные предыдущими инфекциями и вакцинациями, а также репертуар наивной памяти, сформированный воздействием микробиома, пищевых антигенов и вдыхаемых антигенов. Учитывая большую сложность репертуаров Т- и В-клеток и большой стохастический элемент в выборе того, какие клетки будут реагировать на данный стимул, а также соматические мутации в В-клетках, точный состав будет отличаться у каждого человека, даже у монозиготных близнецов [ 66].Добавьте к этому значительную генетическую изменчивость в реакции людей, определяемую высокополиморфными генами HLA [67] и генами врожденного иммунитета, и неудивительно, что иммунные ответы любого взрослого человека значительно различаются.
(a) Беременность
Подробное изучение иммунологии беременности выходит за рамки настоящего обзора (см. [68,69]). Однако успешное размножение имеет центральное значение в эволюции и имеет иммунологические проблемы.Как новорожденный сохраняет механизмы, с помощью которых плод сводит к минимуму свои иммунные реакции на мать, обсуждалось выше. Еще большей загадкой является то, как мать переносит полуаллогенный трансплантат, не отвергая его и без иммуносупрессии, необходимой для принятия трансплантата органа [70]. На материнском интерфейсе трофобласта в месте первоначальной имплантации и в плаценте есть особенности, которые нарушают нормальный иммунный ответ отторжения трансплантата. К ним относятся экспрессия только неполиморфных неклассических антигенов HLA на трофобласте [71], локальное подавление иммунитета, опосредованное инфильтрацией NK-клеток [72], моноцитов и регуляторных Т-клеток [69,73], а также ингибирование активации Т-клеток. катаболизмом триптофана [74].Примерно во время имплантации местная воспалительная реакция создает стабильный участок плаценты [68]. Есть данные, что мать изменяет баланс своих Т-клеточных ответов на Th3, а не на Th2 [68]. Таким образом, у беременных женщин могут наблюдаться ремиссии аутоиммунного заболевания [75], и они более подвержены тяжелым осложнениям гриппа [76] и некоторых других инфекций. Эта иммунная модуляция, необходимая для благополучия плода, иногда может быть вредной для матери.
(b) Злокачественные новообразования и аутоиммунитет
Основная роль иммунной системы, вероятно, состоит в защите от инфекций.Другие роли, такие как разрушение мутировавших клеток, могут быть очень важны, но в большей степени в старости после размножения. Многие опухоли отключают Т-клетки, специфичные для опухолевых антигенов, путем связывания с рецепторами «контрольной точки», такими как PD-1 или CTLA4, и новые методы лечения, которые блокируют эти взаимодействия рецептор-лиганд, имеют большой терапевтический потенциал [77,78]. Однако побочные эффекты такой терапии и пассивного переноса противораковых Т-клеток включают аутоиммунные реакции, предполагающие баланс между реакциями против собственного иммунитета, предотвращающими рак и вызывающими аутоиммунитет [79].Во взрослой жизни баланс обычно работает, но у одной трети западных людей развивается рак, обычно в более позднем возрасте, в то время как у 5–10% развивается клиническое аутоиммунное заболевание, поэтому баланс точно установлен и со временем может измениться. Ослабление иммунной системы в пожилом возрасте (см. Ниже) может улучшить аутоиммунитет, но за счет повышенного риска рака.
Микроорганизмы вызывают около четверти всех видов рака (например, ВЭБ, вирусы гепатита В и С, вирус папилломы человека и Helicobacter pylori ).Специфические Т-клеточные реакции обычно сдерживают эти микробы. Однако, если иммунитет нарушен в результате старения (см. Ниже), иммуносупрессивной терапии или определенных инфекций, особенно ВИЧ-1, эти виды рака возникают [80].
Таким образом, если в раннем детстве развился полностью эффективный иммунный ответ, он созревает по мере накопления памяти и поддерживает здоровье человека в критические периоды жизни, включая деторождение. Он не только защищает от потенциально смертельных инфекций, но также контролирует ряд устойчивых инфекций, некоторые из которых могут вызвать рак.Он также может иметь дело с мутантными клетками, которые могут стать злокачественными. Он может быть чрезмерно реактивным и вызывать аутоиммунное заболевание или аллергию, что является платой за общую пользу.
4. Снижение иммунитета с возрастом
Последняя сцена из всех,
На этом заканчивается эта странная, насыщенная событиями история,
Это второе ребячество и простое забвение,
Без зубов, без глаз, без вкуса , без всего.
С возрастом иммунная система подвергается глубокому ремоделированию и ухудшению, что существенно влияет на здоровье и выживаемость [81,82].Это иммунное старение предрасполагает пожилых людей к более высокому риску острых вирусных и бактериальных инфекций. Более того, уровень смертности от этих инфекций в три раза выше среди пожилых пациентов по сравнению с более молодыми взрослыми пациентами [83]. Инфекционные заболевания по-прежнему являются четвертой по частоте причиной смерти пожилых людей в развитом мире. Кроме того, аберрантные иммунные ответы у пожилых людей могут усугублять воспаление, возможно, способствуя возникновению других бедствий старости: рака, сердечно-сосудистых заболеваний, инсульта, болезни Альцгеймера и деменции [84].
Во время обычного сезона гриппа около 90% дополнительных смертей происходит среди людей старше 65 лет. Более того, слабый иммунный ответ является причиной снижения эффективности вакцин [82,85]. Иммунное старение также приводит к реактивации латентных вирусов, таких как вирус ветряной оспы, вызывая опоясывающий лишай и хроническую невралгию.
Ухудшение иммунной системы с возрастом может нарушить гомеостатическое равновесие между микробиотой и хозяином. Таким образом, снижение бактериального разнообразия в кишечнике коррелирует с диареей, связанной с Clostridium difficile, , основным осложнением для пожилых людей в больницах [86].Более того, отклонения от профиля кишечной микробиоты, установленного в молодости, связаны с воспалительными заболеваниями кишечника [87]. Увеличение с возрастом количества провоспалительных патобионтов и уменьшение количества иммуномодулирующих видов может способствовать развитию воспалительных заболеваний и поддерживать их [86].
В то же время стареющая иммунная система не может поддерживать полную толерантность к аутоантигенам, что приводит к увеличению числа аутоиммунных заболеваний. [88]. Вероятно, это связано с лимфопенией, возникающей с возрастом, что приводит к избыточной гомеостатической пролиферации лимфоцитов [89], а также к снижению регуляторной функции Т-клеток и уменьшению клиренса апоптотических клеток макрофагами [81].
Рак чаще всего встречается у пожилых людей; средний возраст для диагностики рака в промышленно развитых странах приближается к 70 годам. Основная причина, очевидно, в накоплении клеточных и генетических повреждений на протяжении всей жизни; однако, учитывая роль иммунного ответа в борьбе с раком, снижение иммунных функций у пожилых людей должно способствовать более высокому риску [90]. Это иммунное нарушение явно противоречит увеличению аутоиммунитета, поскольку противоопухолевые реакции могут быть направлены против самого себя; однако, вероятно, преобладает общий упадок иммунной системы, и опухоли больше не отторгаются столь же эффективно.Более того, усиление воспаления, обнаруживаемое с возрастом, способствует возникновению рака.
Повышенная заболеваемость из-за ослабления иммунной системы является прямым следствием нарушения регуляции адаптивного иммунитета у пожилых людей. Низкое количество наивных Т-лимфоцитов по сравнению с Т-лимфоцитами [41,42] является следствием сниженного выхода тимуса из инволютивного тимуса. Вследствие этой возрастной лимфопении Т-клетки пролиферируют и увеличивают объем «виртуальной памяти» [91], но в то же время способность устанавливать иммунологическую память в ответ на антигены de novo снижается, что ставит под угрозу вакцинацию.Нарушаются такие функции, как продукция цитокинов Т-клетками CD4 и CD8, изменяется экспрессия ключевых поверхностных маркеров, и соотношение CD4 + к CD8 + Т-клеток инвертируется [81]. Расширенные ответы Т-клеток, которые удерживают под контролем латентные вирусы, такие как ВЭБ и ЦМВ, сокращают пространство для Т-клеток CD8 + , специфичных для других потенциально летальных вирусов [92], усугубляемых снижением выработки наивных Т-клеток тимуса.
Хотя количество периферических В-клеток не уменьшается с возрастом, состав этого компартмента меняется.Подобно Т-клеткам, наивные В-клетки заменяются клетками памяти, испытавшими антиген, некоторые из которых «истощены» (CD19 + IgD — CD27 — ), и они демонстрируют пониженное созревание аффинности и переключение изотипа [81 ].
В целом изменения в компартментах Т- и В-клеток препятствуют адекватному иммунному ответу на новые острые и латентные вирусные инфекции и вакцинации.
Врожденный иммунный ответ также снижается с возрастом. Наблюдаются изменения в количестве врожденных клеток со смещением гематопоэза в сторону миелоидных клонов [93,94].Старые нейтрофилы менее функциональны с пониженной фагоцитарной способностью и выработкой супероксида, отчасти из-за снижения экспрессии рецептора Fc γ [95]. Точно так же у стареющих макрофагов снижается респираторный выброс. Вместе с DC они обнаруживают сниженную фагоцитарную функцию и экспрессию HLA II [81]. Таким образом, иммунологическое «молчаливое» удаление апоптозных и возрастающих количеств стареющих клеток ставится под угрозу и может способствовать провоспалительному фенотипу. Действительно, когда у старых мышей искусственно удаляли стареющие клетки, животные жили дольше и были здоровее [96].
Возможно, наиболее важным изменением в стареющей врожденной иммунной системе является увеличение провоспалительных цитокинов IL-1β, IL-6, IL-18 и TNFα [97]. Возникающее в результате воспаление низкой степени, вероятно, способствует атеросклерозу, деменции и раку, неразрывно связывая воспаление и старение других тканей [84,98].
Клеточные и молекулярные основы иммунного старения еще недостаточно изучены. Три фенотипа характеризуют стареющие клетки: истощение теломер, сопровождающее каждый раунд пролиферации, ведущее к остановке деления клеток или «репликативному старению»; повышенная митохондриальная нагрузка / дисфункция и активные формы кислорода; и секреторный фенотип, связанный со старением (SASP), определяемый как секреция провоспалительных цитокинов, хемокинов и протеаз стареющими клетками [99].Хотя большинство данных было получено на фибробластах, стареющие иммунные клетки, вероятно, обладают схожими характеристиками. Эти свойства влияют на митотически активные клетки путем истощения или остановки деления (например, гемопоэтические стволовые клетки — HSC или Т-клетки), а также на постмитотические иммунные клетки, вызывая клеточную дисфункцию (например, нейтрофилов).
Истощение теломер является защитным механизмом против рака, так как каждый раунд пролиферации может вносить мутации [100]. Только эпителиальные лимфоциты и стволовые клетки, включая гемопоэтические (HSC), экспрессируют удлиняющий теломеры фермент теломеразу у взрослых [101], что требует тщательного баланса с риском рака.Как Т-клетки памяти, так и HSC обычно делятся редко, чтобы минимизировать истощение теломер, но надежно либо в ответ на инфекцию (лимфоциты памяти), либо для обновления тканей (стволовые клетки) на протяжении всей жизни. На конечной стадии стареющие CD27 — CD28 — Т-клетки имеют самые короткие теломеры и демонстрируют сниженную пролиферацию после активации, но тем не менее обладают мощными эффекторными функциями. Эти клетки накапливаются в пожилом возрасте и у пациентов с аутоиммунными заболеваниями и хроническими вирусными инфекциями [102].Вторая характеристика старых клеток — усиление митохондриальной дисфункции и, как следствие, окислительное повреждение белков и ДНК. Функция DC у старых мышей может быть восстановлена путем введения антиоксидантов [103]. Окислительный стресс вызывает разрывы ДНК и может быть причиной истощения теломер, которое связывает первые две причины старения. Накопление окислительного повреждения может быть связано со снижением лизосомальной функции и аутофагии [104]. Аутофагия, разрушающая объем цитоплазматического материала путем доставки его к лизосомам, снижается с возрастом, в том числе в человеческих CD8 + Т-клетках [105].Мыши без аутофагии в их кроветворной системе обнаруживают преждевременно состарившуюся кроветворную систему [106]. Отсутствие реакции Т-клеток памяти на вакцинацию против гриппа, наблюдаемую у пожилых людей, можно восстановить с помощью соединения, индуцирующего аутофагию [107]. Третьим более недавним дополнением к этим фундаментальным изменениям старых клеток является приобретение SASP, способствующего повышенной секреции провоспалительных цитокинов и слабому воспалению [99].
5. Эволюция иммунной системы человека
Будучи долгоживущими видами, люди развили механизмы врожденного иммунитета и иммунологической памяти, чтобы выжить при повторных инфекциях.Однако на протяжении жизни человека эти иммунные механизмы изменяются, сначала для адаптации к переходу от плода к младенцу, а затем к созреванию и расширению во время роста, слегка изменяясь во время беременности и, наконец, уменьшаясь в процессе старения. Выход наивных лимфоидных клеток и способность формировать новую иммунологическую память становятся все менее важными, поскольку пожилой человек столкнется и установит банк памяти для многих патогенов в течение своей жизни. Существует вероятность того, что миелоидный сдвиг и повышенная секреция провоспалительных цитокинов во время старения важны для улучшения фагоцитоза увеличивающегося числа стареющих клеток, что поднимает вопрос о том, могут ли изменения в стареющей иммунной системе служить цели.
Иммунная система была в первую очередь сформирована эволюцией, чтобы эффективно реагировать на острые инфекции у молодых людей, адаптироваться к беременности и передавать защиту младенцам, а также адаптирована для борьбы со многими хроническими инфекциями, длящимися десятилетиями. Помимо борьбы с вирусами, бактериями, грибками и паразитами, иммунная система также берет на себя другие функции, такие как восстановление тканей, заживление ран, удаление мертвых и раковых клеток и формирование здоровой микробиоты кишечника. Предполагая отсутствие серьезного избирательного давления на людей старше репродуктивного возраста, нам, возможно, придется платить за генетические черты, выбранные для обеспечения приспособленности в раннем возрасте, за счет более позднего развития иммунологических фенотипов, таких как хроническое воспаление.Массовое старение и повышенная долговечность — это недавние явления, происходящие в оптимизированной среде. Как предположил Хейфлик [108], старение может быть артефактом цивилизации, и, следовательно, изменения в стареющей иммунной системе могут быть просто следствием эволюционного непредсказуемого воздействия антигена на протяжении всей жизни человека.
В некоторых аспектах иммунная система пожилого организма напоминает иммунную систему новорожденного, со сниженной антимикробной активностью нейтрофилов и макрофагов, сниженной презентацией антигена DC и уменьшенным уничтожением NK, а также несколько нарушенными адаптивными ответами лимфоцитов.Таким образом, как очень молодая, так и старая иммунная система одинаково подвержены риску справиться с типичной вирусной инфекцией, такой как грипп, тогда как молодой (небеременный) взрослый организм, по-видимому, идеально подходит для этой задачи (). Эволюция иммунной системы внутри индивидуума, возможно, отражает центральную роль молодого взрослого человека в выживании вида благодаря его репродуктивному потенциалу.
Эволюция иммунной системы человека от младенчества до старости
Резюме
В этой статье рассматривается развитие иммунного ответа в неонатальном, младенческом и взрослом возрасте, включая беременность, заканчивающуюся спадом в пожилом возрасте.Возникает картина ребенка, рожденного с незрелой, врожденной и адаптивной иммунной системой, которая созревает и приобретает память по мере его роста. Затем в старости он приходит в упадок. Эти изменения рассматриваются наряду с рисками различных типов инфекций, аутоиммунных заболеваний и злокачественных новообразований.
Ключевые слова: адаптивный иммунитет, врожденный иммунитет, инфекции
1. Введение
И один человек в свое время играет много ролей,
Его деяниям семь возрастов.
Более 1600 генов участвуют в врожденных и адаптивных иммунных ответах [1]. Эти гены имеют большое значение для поддержания жизни во враждебной среде. Тем не менее, иммунная система является относительно незрелой при рождении и должна развиваться в течение жизни, подвергаясь воздействию множества внешних проблем в детстве, в молодом и зрелом возрасте (включая беременность), до упадка старости ().
( a ) Семь возрастов женщины. ( b ) Схематический график дополнительных смертей от сезонного или пандемического гриппа на протяжении жизни человека, представленный как число смертей на 1000 человек (адаптировано из [2]).Обратите внимание, что хотя беременность увеличивает риск тяжелого гриппа, во время тяжелых пандемий, таких как 1918/1919 гг., Также наблюдались избыточные смертельные случаи среди ранее здоровых молодых людей, которые не были беременными. ( c ) Схематический график различных звеньев иммунного ответа на грипп на протяжении жизни человека.
2. Онтогенез иммунной системы в молодом возрасте
Сначала младенец,
Мычание и рвота в руках медсестры.
In utero среда плода требует, чтобы иммунная система оставалась толерантной к материнским аллоантигенам.После рождения внезапное колоссальное воздействие антигенов окружающей среды, многие из которых происходят из кишечных комменсальных бактерий, требует быстрых изменений, чтобы вызвать определенные иммунные реакции, соответствующие раннему возрасту.
(a) Врожденная иммунная система
Врожденная иммунная система обеспечивает раннюю первую линию защиты от вторжения патогенов. Вовлеченные клетки — нейтрофилы, моноциты, макрофаги и дендритные клетки, которые все взаимодействуют с адаптивной иммунной системой. Эти клетки развиваются и созревают в течение жизни плода, но в разное время, и функция всех компонентов врожденного иммунитета у новорожденных слабее по сравнению с более поздней жизнью.
Зрелые нейтрофилы присутствуют в конце первого триместра и резко увеличиваются в количестве, стимулируемые гранулоцитарно-колониестимулирующим фактором, незадолго до рождения. Затем их количество возвращается к стабильному уровню в течение нескольких дней, но они демонстрируют слабую бактерицидную функцию, слабую реакцию на воспалительные стимулы, снижение адгезии к эндотелиальным клеткам и уменьшение хемотаксиса [3]. Эти дефициты более заметны у недоношенных детей, у которых также ниже сывороточный IgG и комплемент. Следовательно, новорожденные, и особенно недоношенные, имеют нарушенные функции нейтрофилов [4], что подвергает ребенка риску бактериальных инфекций.
У недоношенных и новорожденных классические моноциты и макрофаги также являются незрелыми. У них снижена экспрессия TLR4 [5] с нарушением врожденных сигнальных путей [6-8], что приводит к снижению цитокиновых ответов по сравнению со взрослыми. Следовательно, происходит плохое восстановление тканей, нарушенный фагоцитоз потенциальных патогенов и плохая секреция биоактивных молекул. Однако, хотя частота макрофагов в легких у недоношенных и доношенных детей снижается, уровни этих клеток у взрослых достигаются в течение нескольких дней после рождения [9].
По сравнению с кровью детей или взрослых, пуповинная кровь содержит меньше дендритных клеток миелоидного типа (mDC). Они экспрессируют более низкие уровни HLA класса II, CD80 и CD86 на клеточной поверхности, чем взрослые mDC [10]. Они секретируют низкие концентрации IL-12p70 в ответ на активацию врожденных стимулов [11]. Таким образом, праймирование Т-клеточных ответов Th2 и CD8 снижено по сравнению со взрослыми, что коррелирует с повышенной восприимчивостью к инфекциям, вызываемым вирусами Mycobacterium tuberculosis и Salmonella spp . Напротив, новорожденные mDC, стимулированные с помощью TLR4, секретируют подобные взрослым концентрации провоспалительных цитокинов [12], которые способствуют иммунным ответам Th27.
Плазмацитоидные дендритные клетки (pDC) выделяют высокие концентрации интерферона I типа (IFN) в ответ на стимуляцию TLR7 и TLR9 у взрослых. Однако новорожденные pDC строго ограничены в секрете интерферона α / β при воздействии различных вирусов, несмотря на то, что уровни экспрессии TLR7 и TLR9 аналогичны взрослым [13]. Следовательно, врожденные иммунные ответы на вирусы, такие как респираторно-синцитиальный вирус, вирус простого герпеса и цитомегаловирус, являются слабыми по сравнению с более поздними периодами жизни.
Естественные киллерные (NK) клетки у взрослых сдерживают репликацию и распространение вируса до установления адаптивного иммунитета [14]. Они регулируются ингибирующими рецепторами, которые распознают HLA-A, B, C и E, и, следовательно, способствуют самотолерантности. На ранних сроках беременности NK-клетки гипочувствительны к клеткам-мишеням, лишенным молекул класса I главного комплекса гистосовместимости (MHC) (таких как трофобласт [15]), и очень чувствительны к подавлению иммунитета за счет трансформирующего фактора роста-β (TGF-β).Цитолитическая функция NK увеличивается во время беременности, но при рождении все еще составляет лишь половину от взрослого уровня. Новорожденные NK-клетки менее чувствительны к активации IL-2 и IL-15 и продуцируют ограниченные концентрации IFN-γ. Однако порог активации клеток ниже, что обеспечивает некоторую противовирусную защиту [15].
Три независимых пути, которые активируют систему комплемента, имеют решающее значение для защиты хозяина и воспаления. Компоненты комплемента способствуют опсонизации, являются хемоаттрактантами для врожденных клеток, опосредуют лизис клеток и влияют на выработку антител.Концентрация почти всех циркулирующих компонентов в сыворотке новорожденных на 10–80% ниже, чем у взрослых [16], при пониженной биологической активности. Уровни комплемента повышаются после рождения, при этом некоторые сывороточные факторы достигают концентрации у взрослых в течение месяца (например, фактор B), но другие развиваются медленнее [16]. Поскольку у младенцев низкая концентрация иммуноглобулина, эффекторные функции комплемента зависят от альтернативных путей активации и лектин-связывающей активации, запускаемых полисахаридами и эндотоксинами.
В целом, врожденная иммунная система при рождении приглушена, цена, вероятно, заплачена плодом не только за переносимость необщих материнских антигенов, но и за игнорирование значительного стресса и ремоделирования, которые происходят во время развития.Это делает новорожденного, особенно недоношенного, относительно восприимчивым к бактериальным и вирусным инфекциям.
(b) Адаптивная иммунная система
Т-клетки развиваются в тимусе, который является самым большим при рождении и в течение первых лет жизни. Зрелые единичные CD4 + и CD8 + положительные Т-клетки впервые обнаруживаются в тимусе на 15 неделе и в большом количестве на периферии задолго до рождения [17,18]. Однако неонатальные Т-клетки значительно отличаются от взрослых клеток, отражая жизнь плода, где воздействие чужеродных антигенов в значительной степени ограничивается ненаследственными материнскими аллоантигенами.Функция ранних Т-клеток отличается от взрослых Т-клеток. Например, хотя наивные CD4 + Т-клетки плода сильно реагируют на аллоантигены, они имеют тенденцию развиваться в направлении Foxp3 + CD25 + регуляторных Т-клеток (T reg ) под влиянием TGF-β [19], и таким образом активно продвигают терпимость к себе. Периферические Т reg составляют около 3% от общего количества CD4 + Т-клеток при рождении [20], и эти клетки сохраняются в течение длительного периода времени [21], придавая иммунному ответу в раннем возрасте противовоспалительный профиль [22 ].
Активация чужеродным антигеном поздних эмбриональных или неонатальных Т-клеток приводит к ответу, искаженному в сторону иммунитета Th3 [23], который усиливается неонатальными дендритными клетками и эпигенетическими особенностями [24,25]. Таким образом, очень ранний адаптивный Т-клеточный иммунитет характеризуется толерогенной реактивностью, сниженным распознаванием алло-антигена и слабыми ответами на чужеродные антигены.
У новорожденных, помимо обычных Т-клеток, которые распознают пептидные антигены в контексте классических молекул MHC, существуют популяции γδ Т-клеточных рецепторов (TCR) -позитивных и врожденных-подобных αβ-TCR-позитивных Т-клеток.К ним относятся функционально компетентные клетки iNKT, которые быстро продуцируют IFN, ассоциированные со слизистой оболочкой инвариантные Т-клетки (MAIT) [26] и недавно описанные интерлейкин-8 (CXCL8) -секретирующие наивные Т-клетки, которые связывают врожденный и адаптивный иммунитет [27]. Клетки MAIT развиваются в тимусе, но их созревание может происходить в тканях слизистой оболочки плода до микробной колонизации. Т-клетки, продуцирующие CXCL8, производят важные эффекторные функции у новорожденных людей, поскольку они обладают потенциалом активации антимикробных нейтрофилов и γδ Т-клеток.Они, по-видимому, особенно активны на барьерах слизистой оболочки недоношенных и доношенных детей, хотя их частота уменьшается с возрастом. В отличие от взрослой крови, где репертуар γδ TCR ограничен, γδ T-клетки неонатальной крови обнаруживают множество комбинаций рецепторных цепей, которые меняются с беременностью [27]. γδ Т-клетки могут продуцировать значительные количества IFN-γ после кратковременной поликлональной стимуляции, компенсируя незрелость более классического ответа Т-клеток Th2-типа на неонатальные инфекции [28,29].
Два типа В-клеток возникают через разные пути развития [30]. Клетки B1 спонтанно секретируют низкоаффинный IgM с ограниченным диапазоном антигенной специфичности (включая обычные бактериальные полисахариды), имеют меньше соматических мутаций и служат первой линией защиты [31]. Клетки B1 секретируют IL-10 и TGF-β и, таким образом, способствуют ответу Th3. При рождении B1-клетки составляют 40% B-клеток периферической крови, и эта частота остается высокой в течение нескольких месяцев [32]. Обычные В-клетки (обозначенные как клетки В2) происходят из многолинейного общего лимфоидного предшественника CD34 + и генерируют широкий репертуар иммуноглобулиновой специфичности благодаря экспрессии терминальной дезоксинуклеотидилтрансферазы, которая увеличивает разнообразие в присоединении сегментов гена иммуноглобулина V-D-J.В-клетки обычно присутствуют во вторичных лимфоидных органах и в костном мозге, где они вносят вклад в гуморальный ответ адаптивной иммунной системы.
Большинство ответов антител, в том числе на бактериальные белки, бактериальные полисахариды и на полисахаридно-белковые конъюгированные вакцины, зависят от помощи Т-клеток. Они полагаются на взаимодействие между TCR и участие корецепторов, включая CD28 и лиганд CD40, на Th3 или фолликулярных Т-хелперных клетках с их соответствующими партнерами по связыванию HLA-пептидом, CD80 / 86 и CD40 на антиген-специфических В-клетках.Однако неонатальные В-клетки экспрессируют низкие уровни этих корецепторов, что ограничивает их способность отвечать [33]. Более того, низкие уровни рецептора для фрагмента C3d комплемента (CD21) препятствуют ответам на комплексы полисахарид-комплемент [34]. Вместе эти особенности вносят вклад в притупление гуморальных иммунных ответов с неполным переключением классов иммуноглобулинов [35], хотя генерируются В-клетки памяти [36]. В-клетки новорожденных и младенцев в возрасте до 2 месяцев демонстрируют снижение соматической гипермутации по сравнению со взрослыми, что ограничивает созревание аффинности антител [37].Наконец, стромальные клетки костного мозга в раннем возрасте не способны поддерживать долгосрочную выживаемость плазмобластов и дифференцировку в плазматические клетки, так что любые антитела IgG, вырабатываемые после иммунизации, быстро снижаются, в отличие от детей старшего возраста и взрослых [38]. Следовательно, эффективность адаптивной иммунной системы по раннему ответу на Т-клеточно-зависимые антигены заметно снижена у новорожденных по сравнению с детьми старшего возраста и взрослыми. Это физиологическое поведение особенно актуально для программ вакцинации.Вместе с нарушением врожденного иммунитета слабый ответ Th2 и антител хорошо объясняет, почему неонатальная смертность может быть высокой в условиях повышенного воздействия патогенов.
3. Из детства во взрослую жизнь
Потом нытье школьник с сумкой
И сияющее утреннее лицо, ползет как улитка
В школу нехотя.
Маленький человеческий ребенок, даже когда врожденная и адаптивная иммунные системы начинают созревать, подвергается риску заражения многими патогенными вирусами, бактериями, грибами и паразитами.Тем не менее, у него или нее есть хорошие шансы выжить в развитых странах. До того, как появилось хорошее питание, гигиена и комплексная вакцинация, младенцы и дети младшего возраста страдали от высокой смертности. В 1900 году коэффициент младенческой смертности в Великобритании составлял 140 на 1000, а к 2000 году упал до 7 на 1000 [39]. Это снижение смертности было пропорционально больше у младенцев и детей по сравнению с другими возрастными группами [40]. На лучшую профилактику и контроль инфекций приходится большая часть этой осени. Однако во многих странах уровень младенческой смертности по-прежнему превышает 50 на 1000, что указывает на эволюционное давление, которое должно было привести к выбору работающей защитной иммунной системы.Кроме того, такое давление выбрало крайний генетический полиморфизм в MHC, который благодаря презентации пептидов Т-клеткам и NK-клеткам является ключевым регулятором почти всех иммунных ответов.
В младенчестве иммунная система постепенно созревает. Критически важная ранняя защита от многих инфекционных заболеваний, ранее перенесенных матерью, обеспечивается пассивными антителами IgG, передаваемыми от матери трансплацентарно и с молоком. Как только это исчезнет, маленькие дети станут более уязвимыми к инфекциям, хотя к тому времени они будут лучше вооружены созревающей врожденной и адаптивной иммунной системой.В настоящее время риски значительно снижаются за счет вакцинации, которая стимулирует защитные иммунные реакции в созревающей иммунной системе. Тем не менее, дети все еще могут заразиться вирусными, бактериальными и паразитарными инфекциями, с которыми необходимо бороться и контролировать иммунные реакции. Такая стимуляция антигеном не только способствует выздоровлению, но и приводит к иммунологической памяти [41,42]. Таким образом, со временем защита, обеспечиваемая иммунным ответом, увеличивается, и молодые люди реже страдают от инфекций. Это накопление иммунологической памяти является развивающейся особенностью адаптивного иммунного ответа.Память сохраняется до старости [41], но затем может исчезнуть.
Помимо явных инфекций и прививок, новорожденный подвергается воздействию других антигенов. Он или она происходит из относительно стерильной среды in utero и затем быстро подвергается воздействию множества микробов [43]. Первый серьезный контакт с бактериями происходит во время прохождения через родовые пути, а затем, как только он / она вступает в оральный, кожный и респираторный контакт с окружающей средой. С этого момента воздействие микроорганизмов продолжается.Многие бактерии, колонизирующие кишечник и другие участки слизистой оболочки, необходимы для здорового образа жизни, включая переваривание пищи и получение жизненно важных питательных веществ. Они также влияют на развитие иммунной системы [44].
Примерно 20% всех лимфоцитов находятся в кишечнике [45], подвергаясь воздействию многих возможных чужеродных иммуногенов. Иммунные клетки кишечника контролируют границу с потенциально опасным источником инфекций. Кишечные бактерии влияют на развитие клеток Th27 [46], клеток T reg [47] и Т-клеток памяти [48–50].При рождении почти все Т-клетки несут гликопротеин CD45RA, типичный для наивных Т-клеток, которые никогда не сталкивались с чужеродным антигеном. Кроме того, в CD45RA-негативных CD4 Т-клетках имеется относительно большое количество regs Т . В детстве количество клеток T reg снижается, а клетки памяти Th2, Th27 и Th3 постепенно увеличиваются, чтобы сравняться с количеством наивных Т-клеток [51]. Хотя некоторые из этих Т-клеток памяти могли быть стимулированы инфекциями определенными патогенами и вакцинацией, многие из них могут быть активированы микробиомом не только в кишечнике, но также в дыхательных путях и коже.Эти примированные Т-клетки памяти могут отвечать на последующие инфекции посредством перекрестных реакций [48, 52, 53]. Например, взрослые, которые никогда не контактировали с ВИЧ-1, имеют в своем репертуаре Т-клетки памяти, которые реагируют с пептидами ВИЧ, представленными на клеточной поверхности белками HLA; эти Т-клетки, вероятно, снова пробудятся при возникновении ВИЧ-инфекции [48,50], как и другие микробы [52]. Перекрестная реактивность возникает из-за дискретных коротких (8-15 аминокислот) пептидов (эпитопов), которые входят в пептид-связывающие бороздки на молекулах HLA класса I или II на поверхности клетки и затем распознаются Т-клетками.Внутри последовательностей микробиома существует множество идеальных и почти идеальных совпадений с известными вирусными пептидными эпитопами, например, из ВИЧ-1 [48,50]. Они легко могут быть ответственны за создание Т-клеток памяти, специфичных для эпитопов патогенов, с которыми человек никогда не сталкивался.
Сегментированные нитчатые бактерии в кишечнике необходимы для развития клеток Th27 [47] и Clostridium spp. индуцируют клетки T reg толстой кишки [54,55]. У здоровых мышей наблюдаются иммунологические дефекты, в том числе меньшее количество пейеровских бляшек, более мелкие лимфоидные фолликулы и аномальные зародышевые центры в лимфоидной ткани тонкого кишечника [56].Этот иммунодефицит можно скорректировать за несколько дней, добавив одну мышь с нормальной кишечной флорой в клетку с стерильными животными [56,57]. Таким образом, данные на животных подтверждают мнение о том, что микробиом формирует развитие как Т-, так и В-клеток памяти.
Подобные события происходят и для В-клеток. Углеводные антигены групп крови ABO перекрестно реагируют с бактериальными антигенами кишечника и стимулируют ответы антител IgM. Антитела к белку gp41 ВИЧ-1 могут происходить из В-клеток, рецепторы антител которых перекрестно реагируют с белком Escherichia coli [58].
По мере роста ребенка иммунный репертуар также формируется интеркуррентными инфекциями и вакцинациями [59]. Патогенные инфекции могут быть задокументированы по симптоматическим заболеваниям, перенесенным ребенком или взрослым, но для многих вирусов, таких как грипп, инфекция может быть субклинической, но все же достаточной для стимуляции или усиления иммунного ответа [60]. Как правило, защита, обеспечиваемая иммунным ответом, как антителами, так и Т-клетками, очень эффективна. Большинство детских инфекций случаются только один раз, и тогда защита длится всю жизнь.
Поддержание долговременной B-клеточной памяти примечательно, учитывая, что иммуноглобулин IgG имеет период полураспада in vivo около 25 дней [61]. Плазматические клетки, продуцирующие антитела, которые развиваются во время иммунного ответа, мигрируют в костный мозг, где они живут очень долго. Кроме того, может происходить непрерывная регенерация В-клеток памяти, контактирующих с персистирующим антигеном и Т-хелперами. Антигены в виде частиц годами сохраняются в лимфатических узлах, удерживаемых фолликулярными дендритными клетками [62].Персистенция антигена и перекрестно-реактивные антигены, вероятно, помогают поддерживать жизнь этих В-клеток, время от времени делящихся и секретируя антитела.
Примечательно, что мать может передать достаточно антител, чтобы защитить своего ребенка, когда он был инфицирован 20–30 лет назад. Передача защитных антител от матери к ее ребенку чрезвычайно важна, особенно в средах, где 15% или более младенцев и детей умирают от инфекции. Парадоксально, но мать, которая избежала опасной детской инфекции благодаря коллективному иммунитету, может фактически подвергнуть своего ребенка риску, будучи неспособной передавать специфические защитные антитела.
Существует большое количество бессимптомных хронических инфекций, в основном вирусных, которые вызывают иммунные реакции. Примерами являются цитомегаловирус (ЦМВ), вирус Эпштейна-Барра (ВЭБ) и Mycobacterium tubercolosis ( Mtb ), но полный список длинный и продолжает расти [63]. EBV, CMV и Mtb вызывают очень сильные Т-клеточные ответы CD4 и CD8 у людей. ЦМВ-специфический ответ Т-лимфоцитов CD8 может привести к разрастанию олигоклональных Т-клеток, достигающих более 10% циркулирующих Т-лимфоцитов CD8.Эти Т-клетки важны, потому что они контролируют вирус, и их истощение, например, с помощью иммуносупрессивной терапии, может активировать инфекцию (например, Mtb, , EBV, CMV) с разрушительными последствиями.
Эволюция ответов антител в В-лимфоцитах подробно рассмотрена в другом месте [64]. Короче говоря, наивные В-клетки с рецепторами антител, специфическими для иммуногена, связывают антиген в зародышевом центре лимфатических узлов и получают частичный сигнал. Связанный антиген интернализируется и переваривается в лизосомах.Несколько образующихся пептидов связываются с молекулами HLA класса II этой клетки и затем представляются на поверхности клетки, где Т-фолликулярные хелперные клетки с соответствующими Т-клеточными рецепторами отвечают и доставляют дополнительные сигналы, включая IL-21, к В-клетке. Эти сигналы запускают деление В-клеток, переключение классов генов антител и соматическую гипермутацию. В этом случае предпочтение отдается В-клеткам, которые экспрессируют мутировавшие антитела, связывающие иммуноген с более высокой аффинностью. Отбор антител с лучшим связыванием продолжается в течение месяцев, что в конечном итоге приводит к получению антител с высоким сродством из сильно мутировавших генов зародышевой линии.Антитела с высоким сродством более эффективны при нейтрализации или опсонизации вторгшихся микробов и их патогенных продуктов.
Процесс соматической гипермутации не происходит в Т-клетках, даже если они имеют антителоподобные гены рецепторов Т-клеток, потому что наличие высокоаффинного Т-клеточного рецептора не дает никаких преимуществ. Связывание рецептора Т-клетки с комплексом пептид-HLA на антигенпрезентирующих клетках имеет низкое сродство. Он усиливается несколькими парами корецептор-лиганд, которые не являются антиген-специфическими, давая Т-клетке сигнал делиться и функционировать.
В результате иммунного заражения отвечающие Т- и В-клетки могут временно увеличиваться до очень больших количеств [65], иногда более 10% от всех циркулирующих Т-клеток, но они быстро сокращаются в результате активации клеток, индуцированных активацией. смерть и истощение в течение более длительного периода времени. Таким образом, когда патоген контролируется и исчезает, некоторые Т- и В-клетки памяти сохраняются в течение длительного времени в количестве, которое намного превышает количество наивных Т-клеток и Т-клеток «наивной памяти», которые были там до заражения.
По мере того, как человек становится старше, он или она развивает расширяющийся репертуар, включающий Т- и В-клетки памяти, вызванные предыдущими инфекциями и вакцинациями, а также репертуар наивной памяти, сформированный воздействием микробиома, пищевых антигенов и вдыхаемых антигенов. Учитывая большую сложность репертуаров Т- и В-клеток и большой стохастический элемент в выборе того, какие клетки будут реагировать на данный стимул, а также соматические мутации в В-клетках, точный состав будет отличаться у каждого человека, даже у монозиготных близнецов [ 66].Добавьте к этому значительную генетическую изменчивость в реакции людей, определяемую высокополиморфными генами HLA [67] и генами врожденного иммунитета, и неудивительно, что иммунные ответы любого взрослого человека значительно различаются.
(a) Беременность
Подробное изучение иммунологии беременности выходит за рамки настоящего обзора (см. [68,69]). Однако успешное размножение имеет центральное значение в эволюции и имеет иммунологические проблемы.Как новорожденный сохраняет механизмы, с помощью которых плод сводит к минимуму свои иммунные реакции на мать, обсуждалось выше. Еще большей загадкой является то, как мать переносит полуаллогенный трансплантат, не отвергая его и без иммуносупрессии, необходимой для принятия трансплантата органа [70]. На материнском интерфейсе трофобласта в месте первоначальной имплантации и в плаценте есть особенности, которые нарушают нормальный иммунный ответ отторжения трансплантата. К ним относятся экспрессия только неполиморфных неклассических антигенов HLA на трофобласте [71], локальное подавление иммунитета, опосредованное инфильтрацией NK-клеток [72], моноцитов и регуляторных Т-клеток [69,73], а также ингибирование активации Т-клеток. катаболизмом триптофана [74].Примерно во время имплантации местная воспалительная реакция создает стабильный участок плаценты [68]. Есть данные, что мать изменяет баланс своих Т-клеточных ответов на Th3, а не на Th2 [68]. Таким образом, у беременных женщин могут наблюдаться ремиссии аутоиммунного заболевания [75], и они более подвержены тяжелым осложнениям гриппа [76] и некоторых других инфекций. Эта иммунная модуляция, необходимая для благополучия плода, иногда может быть вредной для матери.
(b) Злокачественные новообразования и аутоиммунитет
Основная роль иммунной системы, вероятно, состоит в защите от инфекций.Другие роли, такие как разрушение мутировавших клеток, могут быть очень важны, но в большей степени в старости после размножения. Многие опухоли отключают Т-клетки, специфичные для опухолевых антигенов, путем связывания с рецепторами «контрольной точки», такими как PD-1 или CTLA4, и новые методы лечения, которые блокируют эти взаимодействия рецептор-лиганд, имеют большой терапевтический потенциал [77,78]. Однако побочные эффекты такой терапии и пассивного переноса противораковых Т-клеток включают аутоиммунные реакции, предполагающие баланс между реакциями против собственного иммунитета, предотвращающими рак и вызывающими аутоиммунитет [79].Во взрослой жизни баланс обычно работает, но у одной трети западных людей развивается рак, обычно в более позднем возрасте, в то время как у 5–10% развивается клиническое аутоиммунное заболевание, поэтому баланс точно установлен и со временем может измениться. Ослабление иммунной системы в пожилом возрасте (см. Ниже) может улучшить аутоиммунитет, но за счет повышенного риска рака.
Микроорганизмы вызывают около четверти всех видов рака (например, ВЭБ, вирусы гепатита В и С, вирус папилломы человека и Helicobacter pylori ).Специфические Т-клеточные реакции обычно сдерживают эти микробы. Однако, если иммунитет нарушен в результате старения (см. Ниже), иммуносупрессивной терапии или определенных инфекций, особенно ВИЧ-1, эти виды рака возникают [80].
Таким образом, если в раннем детстве развился полностью эффективный иммунный ответ, он созревает по мере накопления памяти и поддерживает здоровье человека в критические периоды жизни, включая деторождение. Он не только защищает от потенциально смертельных инфекций, но также контролирует ряд устойчивых инфекций, некоторые из которых могут вызвать рак.Он также может иметь дело с мутантными клетками, которые могут стать злокачественными. Он может быть чрезмерно реактивным и вызывать аутоиммунное заболевание или аллергию, что является платой за общую пользу.
4. Снижение иммунитета с возрастом
Последняя сцена из всех,
На этом заканчивается эта странная, насыщенная событиями история,
Это второе ребячество и простое забвение,
Без зубов, без глаз, без вкуса , без всего.
С возрастом иммунная система подвергается глубокому ремоделированию и ухудшению, что существенно влияет на здоровье и выживаемость [81,82].Это иммунное старение предрасполагает пожилых людей к более высокому риску острых вирусных и бактериальных инфекций. Более того, уровень смертности от этих инфекций в три раза выше среди пожилых пациентов по сравнению с более молодыми взрослыми пациентами [83]. Инфекционные заболевания по-прежнему являются четвертой по частоте причиной смерти пожилых людей в развитом мире. Кроме того, аберрантные иммунные ответы у пожилых людей могут усугублять воспаление, возможно, способствуя возникновению других бедствий старости: рака, сердечно-сосудистых заболеваний, инсульта, болезни Альцгеймера и деменции [84].
Во время обычного сезона гриппа около 90% дополнительных смертей происходит среди людей старше 65 лет. Более того, слабый иммунный ответ является причиной снижения эффективности вакцин [82,85]. Иммунное старение также приводит к реактивации латентных вирусов, таких как вирус ветряной оспы, вызывая опоясывающий лишай и хроническую невралгию.
Ухудшение иммунной системы с возрастом может нарушить гомеостатическое равновесие между микробиотой и хозяином. Таким образом, снижение бактериального разнообразия в кишечнике коррелирует с диареей, связанной с Clostridium difficile, , основным осложнением для пожилых людей в больницах [86].Более того, отклонения от профиля кишечной микробиоты, установленного в молодости, связаны с воспалительными заболеваниями кишечника [87]. Увеличение с возрастом количества провоспалительных патобионтов и уменьшение количества иммуномодулирующих видов может способствовать развитию воспалительных заболеваний и поддерживать их [86].
В то же время стареющая иммунная система не может поддерживать полную толерантность к аутоантигенам, что приводит к увеличению числа аутоиммунных заболеваний. [88]. Вероятно, это связано с лимфопенией, возникающей с возрастом, что приводит к избыточной гомеостатической пролиферации лимфоцитов [89], а также к снижению регуляторной функции Т-клеток и уменьшению клиренса апоптотических клеток макрофагами [81].
Рак чаще всего встречается у пожилых людей; средний возраст для диагностики рака в промышленно развитых странах приближается к 70 годам. Основная причина, очевидно, в накоплении клеточных и генетических повреждений на протяжении всей жизни; однако, учитывая роль иммунного ответа в борьбе с раком, снижение иммунных функций у пожилых людей должно способствовать более высокому риску [90]. Это иммунное нарушение явно противоречит увеличению аутоиммунитета, поскольку противоопухолевые реакции могут быть направлены против самого себя; однако, вероятно, преобладает общий упадок иммунной системы, и опухоли больше не отторгаются столь же эффективно.Более того, усиление воспаления, обнаруживаемое с возрастом, способствует возникновению рака.
Повышенная заболеваемость из-за ослабления иммунной системы является прямым следствием нарушения регуляции адаптивного иммунитета у пожилых людей. Низкое количество наивных Т-лимфоцитов по сравнению с Т-лимфоцитами [41,42] является следствием сниженного выхода тимуса из инволютивного тимуса. Вследствие этой возрастной лимфопении Т-клетки пролиферируют и увеличивают объем «виртуальной памяти» [91], но в то же время способность устанавливать иммунологическую память в ответ на антигены de novo снижается, что ставит под угрозу вакцинацию.Нарушаются такие функции, как продукция цитокинов Т-клетками CD4 и CD8, изменяется экспрессия ключевых поверхностных маркеров, и соотношение CD4 + к CD8 + Т-клеток инвертируется [81]. Расширенные ответы Т-клеток, которые удерживают под контролем латентные вирусы, такие как ВЭБ и ЦМВ, сокращают пространство для Т-клеток CD8 + , специфичных для других потенциально летальных вирусов [92], усугубляемых снижением выработки наивных Т-клеток тимуса.
Хотя количество периферических В-клеток не уменьшается с возрастом, состав этого компартмента меняется.Подобно Т-клеткам, наивные В-клетки заменяются клетками памяти, испытавшими антиген, некоторые из которых «истощены» (CD19 + IgD — CD27 — ), и они демонстрируют пониженное созревание аффинности и переключение изотипа [81 ].
В целом изменения в компартментах Т- и В-клеток препятствуют адекватному иммунному ответу на новые острые и латентные вирусные инфекции и вакцинации.
Врожденный иммунный ответ также снижается с возрастом. Наблюдаются изменения в количестве врожденных клеток со смещением гематопоэза в сторону миелоидных клонов [93,94].Старые нейтрофилы менее функциональны с пониженной фагоцитарной способностью и выработкой супероксида, отчасти из-за снижения экспрессии рецептора Fc γ [95]. Точно так же у стареющих макрофагов снижается респираторный выброс. Вместе с DC они обнаруживают сниженную фагоцитарную функцию и экспрессию HLA II [81]. Таким образом, иммунологическое «молчаливое» удаление апоптозных и возрастающих количеств стареющих клеток ставится под угрозу и может способствовать провоспалительному фенотипу. Действительно, когда у старых мышей искусственно удаляли стареющие клетки, животные жили дольше и были здоровее [96].
Возможно, наиболее важным изменением в стареющей врожденной иммунной системе является увеличение провоспалительных цитокинов IL-1β, IL-6, IL-18 и TNFα [97]. Возникающее в результате воспаление низкой степени, вероятно, способствует атеросклерозу, деменции и раку, неразрывно связывая воспаление и старение других тканей [84,98].
Клеточные и молекулярные основы иммунного старения еще недостаточно изучены. Три фенотипа характеризуют стареющие клетки: истощение теломер, сопровождающее каждый раунд пролиферации, ведущее к остановке деления клеток или «репликативному старению»; повышенная митохондриальная нагрузка / дисфункция и активные формы кислорода; и секреторный фенотип, связанный со старением (SASP), определяемый как секреция провоспалительных цитокинов, хемокинов и протеаз стареющими клетками [99].Хотя большинство данных было получено на фибробластах, стареющие иммунные клетки, вероятно, обладают схожими характеристиками. Эти свойства влияют на митотически активные клетки путем истощения или остановки деления (например, гемопоэтические стволовые клетки — HSC или Т-клетки), а также на постмитотические иммунные клетки, вызывая клеточную дисфункцию (например, нейтрофилов).
Истощение теломер является защитным механизмом против рака, так как каждый раунд пролиферации может вносить мутации [100]. Только эпителиальные лимфоциты и стволовые клетки, включая гемопоэтические (HSC), экспрессируют удлиняющий теломеры фермент теломеразу у взрослых [101], что требует тщательного баланса с риском рака.Как Т-клетки памяти, так и HSC обычно делятся редко, чтобы минимизировать истощение теломер, но надежно либо в ответ на инфекцию (лимфоциты памяти), либо для обновления тканей (стволовые клетки) на протяжении всей жизни. На конечной стадии стареющие CD27 — CD28 — Т-клетки имеют самые короткие теломеры и демонстрируют сниженную пролиферацию после активации, но тем не менее обладают мощными эффекторными функциями. Эти клетки накапливаются в пожилом возрасте и у пациентов с аутоиммунными заболеваниями и хроническими вирусными инфекциями [102].Вторая характеристика старых клеток — усиление митохондриальной дисфункции и, как следствие, окислительное повреждение белков и ДНК. Функция DC у старых мышей может быть восстановлена путем введения антиоксидантов [103]. Окислительный стресс вызывает разрывы ДНК и может быть причиной истощения теломер, которое связывает первые две причины старения. Накопление окислительного повреждения может быть связано со снижением лизосомальной функции и аутофагии [104]. Аутофагия, разрушающая объем цитоплазматического материала путем доставки его к лизосомам, снижается с возрастом, в том числе в человеческих CD8 + Т-клетках [105].Мыши без аутофагии в их кроветворной системе обнаруживают преждевременно состарившуюся кроветворную систему [106]. Отсутствие реакции Т-клеток памяти на вакцинацию против гриппа, наблюдаемую у пожилых людей, можно восстановить с помощью соединения, индуцирующего аутофагию [107]. Третьим более недавним дополнением к этим фундаментальным изменениям старых клеток является приобретение SASP, способствующего повышенной секреции провоспалительных цитокинов и слабому воспалению [99].
5. Эволюция иммунной системы человека
Будучи долгоживущими видами, люди развили механизмы врожденного иммунитета и иммунологической памяти, чтобы выжить при повторных инфекциях.Однако на протяжении жизни человека эти иммунные механизмы изменяются, сначала для адаптации к переходу от плода к младенцу, а затем к созреванию и расширению во время роста, слегка изменяясь во время беременности и, наконец, уменьшаясь в процессе старения. Выход наивных лимфоидных клеток и способность формировать новую иммунологическую память становятся все менее важными, поскольку пожилой человек столкнется и установит банк памяти для многих патогенов в течение своей жизни. Существует вероятность того, что миелоидный сдвиг и повышенная секреция провоспалительных цитокинов во время старения важны для улучшения фагоцитоза увеличивающегося числа стареющих клеток, что поднимает вопрос о том, могут ли изменения в стареющей иммунной системе служить цели.
Иммунная система была в первую очередь сформирована эволюцией, чтобы эффективно реагировать на острые инфекции у молодых людей, адаптироваться к беременности и передавать защиту младенцам, а также адаптирована для борьбы со многими хроническими инфекциями, длящимися десятилетиями. Помимо борьбы с вирусами, бактериями, грибками и паразитами, иммунная система также берет на себя другие функции, такие как восстановление тканей, заживление ран, удаление мертвых и раковых клеток и формирование здоровой микробиоты кишечника. Предполагая отсутствие серьезного избирательного давления на людей старше репродуктивного возраста, нам, возможно, придется платить за генетические черты, выбранные для обеспечения приспособленности в раннем возрасте, за счет более позднего развития иммунологических фенотипов, таких как хроническое воспаление.Массовое старение и повышенная долговечность — это недавние явления, происходящие в оптимизированной среде. Как предположил Хейфлик [108], старение может быть артефактом цивилизации, и, следовательно, изменения в стареющей иммунной системе могут быть просто следствием эволюционного непредсказуемого воздействия антигена на протяжении всей жизни человека.
В некоторых аспектах иммунная система пожилого организма напоминает иммунную систему новорожденного, со сниженной антимикробной активностью нейтрофилов и макрофагов, сниженной презентацией антигена DC и уменьшенным уничтожением NK, а также несколько нарушенными адаптивными ответами лимфоцитов.Таким образом, как очень молодая, так и старая иммунная система одинаково подвержены риску справиться с типичной вирусной инфекцией, такой как грипп, тогда как молодой (небеременный) взрослый организм, по-видимому, идеально подходит для этой задачи (). Эволюция иммунной системы внутри индивидуума, возможно, отражает центральную роль молодого взрослого человека в выживании вида благодаря его репродуктивному потенциалу.
Эволюция иммунной системы человека от младенчества до старости
Резюме
В этой статье рассматривается развитие иммунного ответа в неонатальном, младенческом и взрослом возрасте, включая беременность, заканчивающуюся спадом в пожилом возрасте.Возникает картина ребенка, рожденного с незрелой, врожденной и адаптивной иммунной системой, которая созревает и приобретает память по мере его роста. Затем в старости он приходит в упадок. Эти изменения рассматриваются наряду с рисками различных типов инфекций, аутоиммунных заболеваний и злокачественных новообразований.
Ключевые слова: адаптивный иммунитет, врожденный иммунитет, инфекции
1. Введение
И один человек в свое время играет много ролей,
Его деяниям семь возрастов.
Более 1600 генов участвуют в врожденных и адаптивных иммунных ответах [1]. Эти гены имеют большое значение для поддержания жизни во враждебной среде. Тем не менее, иммунная система является относительно незрелой при рождении и должна развиваться в течение жизни, подвергаясь воздействию множества внешних проблем в детстве, в молодом и зрелом возрасте (включая беременность), до упадка старости ().
( a ) Семь возрастов женщины. ( b ) Схематический график дополнительных смертей от сезонного или пандемического гриппа на протяжении жизни человека, представленный как число смертей на 1000 человек (адаптировано из [2]).Обратите внимание, что хотя беременность увеличивает риск тяжелого гриппа, во время тяжелых пандемий, таких как 1918/1919 гг., Также наблюдались избыточные смертельные случаи среди ранее здоровых молодых людей, которые не были беременными. ( c ) Схематический график различных звеньев иммунного ответа на грипп на протяжении жизни человека.
2. Онтогенез иммунной системы в молодом возрасте
Сначала младенец,
Мычание и рвота в руках медсестры.
In utero среда плода требует, чтобы иммунная система оставалась толерантной к материнским аллоантигенам.После рождения внезапное колоссальное воздействие антигенов окружающей среды, многие из которых происходят из кишечных комменсальных бактерий, требует быстрых изменений, чтобы вызвать определенные иммунные реакции, соответствующие раннему возрасту.
(a) Врожденная иммунная система
Врожденная иммунная система обеспечивает раннюю первую линию защиты от вторжения патогенов. Вовлеченные клетки — нейтрофилы, моноциты, макрофаги и дендритные клетки, которые все взаимодействуют с адаптивной иммунной системой. Эти клетки развиваются и созревают в течение жизни плода, но в разное время, и функция всех компонентов врожденного иммунитета у новорожденных слабее по сравнению с более поздней жизнью.
Зрелые нейтрофилы присутствуют в конце первого триместра и резко увеличиваются в количестве, стимулируемые гранулоцитарно-колониестимулирующим фактором, незадолго до рождения. Затем их количество возвращается к стабильному уровню в течение нескольких дней, но они демонстрируют слабую бактерицидную функцию, слабую реакцию на воспалительные стимулы, снижение адгезии к эндотелиальным клеткам и уменьшение хемотаксиса [3]. Эти дефициты более заметны у недоношенных детей, у которых также ниже сывороточный IgG и комплемент. Следовательно, новорожденные, и особенно недоношенные, имеют нарушенные функции нейтрофилов [4], что подвергает ребенка риску бактериальных инфекций.
У недоношенных и новорожденных классические моноциты и макрофаги также являются незрелыми. У них снижена экспрессия TLR4 [5] с нарушением врожденных сигнальных путей [6-8], что приводит к снижению цитокиновых ответов по сравнению со взрослыми. Следовательно, происходит плохое восстановление тканей, нарушенный фагоцитоз потенциальных патогенов и плохая секреция биоактивных молекул. Однако, хотя частота макрофагов в легких у недоношенных и доношенных детей снижается, уровни этих клеток у взрослых достигаются в течение нескольких дней после рождения [9].
По сравнению с кровью детей или взрослых, пуповинная кровь содержит меньше дендритных клеток миелоидного типа (mDC). Они экспрессируют более низкие уровни HLA класса II, CD80 и CD86 на клеточной поверхности, чем взрослые mDC [10]. Они секретируют низкие концентрации IL-12p70 в ответ на активацию врожденных стимулов [11]. Таким образом, праймирование Т-клеточных ответов Th2 и CD8 снижено по сравнению со взрослыми, что коррелирует с повышенной восприимчивостью к инфекциям, вызываемым вирусами Mycobacterium tuberculosis и Salmonella spp . Напротив, новорожденные mDC, стимулированные с помощью TLR4, секретируют подобные взрослым концентрации провоспалительных цитокинов [12], которые способствуют иммунным ответам Th27.
Плазмацитоидные дендритные клетки (pDC) выделяют высокие концентрации интерферона I типа (IFN) в ответ на стимуляцию TLR7 и TLR9 у взрослых. Однако новорожденные pDC строго ограничены в секрете интерферона α / β при воздействии различных вирусов, несмотря на то, что уровни экспрессии TLR7 и TLR9 аналогичны взрослым [13]. Следовательно, врожденные иммунные ответы на вирусы, такие как респираторно-синцитиальный вирус, вирус простого герпеса и цитомегаловирус, являются слабыми по сравнению с более поздними периодами жизни.
Естественные киллерные (NK) клетки у взрослых сдерживают репликацию и распространение вируса до установления адаптивного иммунитета [14]. Они регулируются ингибирующими рецепторами, которые распознают HLA-A, B, C и E, и, следовательно, способствуют самотолерантности. На ранних сроках беременности NK-клетки гипочувствительны к клеткам-мишеням, лишенным молекул класса I главного комплекса гистосовместимости (MHC) (таких как трофобласт [15]), и очень чувствительны к подавлению иммунитета за счет трансформирующего фактора роста-β (TGF-β).Цитолитическая функция NK увеличивается во время беременности, но при рождении все еще составляет лишь половину от взрослого уровня. Новорожденные NK-клетки менее чувствительны к активации IL-2 и IL-15 и продуцируют ограниченные концентрации IFN-γ. Однако порог активации клеток ниже, что обеспечивает некоторую противовирусную защиту [15].
Три независимых пути, которые активируют систему комплемента, имеют решающее значение для защиты хозяина и воспаления. Компоненты комплемента способствуют опсонизации, являются хемоаттрактантами для врожденных клеток, опосредуют лизис клеток и влияют на выработку антител.Концентрация почти всех циркулирующих компонентов в сыворотке новорожденных на 10–80% ниже, чем у взрослых [16], при пониженной биологической активности. Уровни комплемента повышаются после рождения, при этом некоторые сывороточные факторы достигают концентрации у взрослых в течение месяца (например, фактор B), но другие развиваются медленнее [16]. Поскольку у младенцев низкая концентрация иммуноглобулина, эффекторные функции комплемента зависят от альтернативных путей активации и лектин-связывающей активации, запускаемых полисахаридами и эндотоксинами.
В целом, врожденная иммунная система при рождении приглушена, цена, вероятно, заплачена плодом не только за переносимость необщих материнских антигенов, но и за игнорирование значительного стресса и ремоделирования, которые происходят во время развития.Это делает новорожденного, особенно недоношенного, относительно восприимчивым к бактериальным и вирусным инфекциям.
(b) Адаптивная иммунная система
Т-клетки развиваются в тимусе, который является самым большим при рождении и в течение первых лет жизни. Зрелые единичные CD4 + и CD8 + положительные Т-клетки впервые обнаруживаются в тимусе на 15 неделе и в большом количестве на периферии задолго до рождения [17,18]. Однако неонатальные Т-клетки значительно отличаются от взрослых клеток, отражая жизнь плода, где воздействие чужеродных антигенов в значительной степени ограничивается ненаследственными материнскими аллоантигенами.Функция ранних Т-клеток отличается от взрослых Т-клеток. Например, хотя наивные CD4 + Т-клетки плода сильно реагируют на аллоантигены, они имеют тенденцию развиваться в направлении Foxp3 + CD25 + регуляторных Т-клеток (T reg ) под влиянием TGF-β [19], и таким образом активно продвигают терпимость к себе. Периферические Т reg составляют около 3% от общего количества CD4 + Т-клеток при рождении [20], и эти клетки сохраняются в течение длительного периода времени [21], придавая иммунному ответу в раннем возрасте противовоспалительный профиль [22 ].
Активация чужеродным антигеном поздних эмбриональных или неонатальных Т-клеток приводит к ответу, искаженному в сторону иммунитета Th3 [23], который усиливается неонатальными дендритными клетками и эпигенетическими особенностями [24,25]. Таким образом, очень ранний адаптивный Т-клеточный иммунитет характеризуется толерогенной реактивностью, сниженным распознаванием алло-антигена и слабыми ответами на чужеродные антигены.
У новорожденных, помимо обычных Т-клеток, которые распознают пептидные антигены в контексте классических молекул MHC, существуют популяции γδ Т-клеточных рецепторов (TCR) -позитивных и врожденных-подобных αβ-TCR-позитивных Т-клеток.К ним относятся функционально компетентные клетки iNKT, которые быстро продуцируют IFN, ассоциированные со слизистой оболочкой инвариантные Т-клетки (MAIT) [26] и недавно описанные интерлейкин-8 (CXCL8) -секретирующие наивные Т-клетки, которые связывают врожденный и адаптивный иммунитет [27]. Клетки MAIT развиваются в тимусе, но их созревание может происходить в тканях слизистой оболочки плода до микробной колонизации. Т-клетки, продуцирующие CXCL8, производят важные эффекторные функции у новорожденных людей, поскольку они обладают потенциалом активации антимикробных нейтрофилов и γδ Т-клеток.Они, по-видимому, особенно активны на барьерах слизистой оболочки недоношенных и доношенных детей, хотя их частота уменьшается с возрастом. В отличие от взрослой крови, где репертуар γδ TCR ограничен, γδ T-клетки неонатальной крови обнаруживают множество комбинаций рецепторных цепей, которые меняются с беременностью [27]. γδ Т-клетки могут продуцировать значительные количества IFN-γ после кратковременной поликлональной стимуляции, компенсируя незрелость более классического ответа Т-клеток Th2-типа на неонатальные инфекции [28,29].
Два типа В-клеток возникают через разные пути развития [30]. Клетки B1 спонтанно секретируют низкоаффинный IgM с ограниченным диапазоном антигенной специфичности (включая обычные бактериальные полисахариды), имеют меньше соматических мутаций и служат первой линией защиты [31]. Клетки B1 секретируют IL-10 и TGF-β и, таким образом, способствуют ответу Th3. При рождении B1-клетки составляют 40% B-клеток периферической крови, и эта частота остается высокой в течение нескольких месяцев [32]. Обычные В-клетки (обозначенные как клетки В2) происходят из многолинейного общего лимфоидного предшественника CD34 + и генерируют широкий репертуар иммуноглобулиновой специфичности благодаря экспрессии терминальной дезоксинуклеотидилтрансферазы, которая увеличивает разнообразие в присоединении сегментов гена иммуноглобулина V-D-J.В-клетки обычно присутствуют во вторичных лимфоидных органах и в костном мозге, где они вносят вклад в гуморальный ответ адаптивной иммунной системы.
Большинство ответов антител, в том числе на бактериальные белки, бактериальные полисахариды и на полисахаридно-белковые конъюгированные вакцины, зависят от помощи Т-клеток. Они полагаются на взаимодействие между TCR и участие корецепторов, включая CD28 и лиганд CD40, на Th3 или фолликулярных Т-хелперных клетках с их соответствующими партнерами по связыванию HLA-пептидом, CD80 / 86 и CD40 на антиген-специфических В-клетках.Однако неонатальные В-клетки экспрессируют низкие уровни этих корецепторов, что ограничивает их способность отвечать [33]. Более того, низкие уровни рецептора для фрагмента C3d комплемента (CD21) препятствуют ответам на комплексы полисахарид-комплемент [34]. Вместе эти особенности вносят вклад в притупление гуморальных иммунных ответов с неполным переключением классов иммуноглобулинов [35], хотя генерируются В-клетки памяти [36]. В-клетки новорожденных и младенцев в возрасте до 2 месяцев демонстрируют снижение соматической гипермутации по сравнению со взрослыми, что ограничивает созревание аффинности антител [37].Наконец, стромальные клетки костного мозга в раннем возрасте не способны поддерживать долгосрочную выживаемость плазмобластов и дифференцировку в плазматические клетки, так что любые антитела IgG, вырабатываемые после иммунизации, быстро снижаются, в отличие от детей старшего возраста и взрослых [38]. Следовательно, эффективность адаптивной иммунной системы по раннему ответу на Т-клеточно-зависимые антигены заметно снижена у новорожденных по сравнению с детьми старшего возраста и взрослыми. Это физиологическое поведение особенно актуально для программ вакцинации.Вместе с нарушением врожденного иммунитета слабый ответ Th2 и антител хорошо объясняет, почему неонатальная смертность может быть высокой в условиях повышенного воздействия патогенов.
3. Из детства во взрослую жизнь
Потом нытье школьник с сумкой
И сияющее утреннее лицо, ползет как улитка
В школу нехотя.
Маленький человеческий ребенок, даже когда врожденная и адаптивная иммунные системы начинают созревать, подвергается риску заражения многими патогенными вирусами, бактериями, грибами и паразитами.Тем не менее, у него или нее есть хорошие шансы выжить в развитых странах. До того, как появилось хорошее питание, гигиена и комплексная вакцинация, младенцы и дети младшего возраста страдали от высокой смертности. В 1900 году коэффициент младенческой смертности в Великобритании составлял 140 на 1000, а к 2000 году упал до 7 на 1000 [39]. Это снижение смертности было пропорционально больше у младенцев и детей по сравнению с другими возрастными группами [40]. На лучшую профилактику и контроль инфекций приходится большая часть этой осени. Однако во многих странах уровень младенческой смертности по-прежнему превышает 50 на 1000, что указывает на эволюционное давление, которое должно было привести к выбору работающей защитной иммунной системы.Кроме того, такое давление выбрало крайний генетический полиморфизм в MHC, который благодаря презентации пептидов Т-клеткам и NK-клеткам является ключевым регулятором почти всех иммунных ответов.
В младенчестве иммунная система постепенно созревает. Критически важная ранняя защита от многих инфекционных заболеваний, ранее перенесенных матерью, обеспечивается пассивными антителами IgG, передаваемыми от матери трансплацентарно и с молоком. Как только это исчезнет, маленькие дети станут более уязвимыми к инфекциям, хотя к тому времени они будут лучше вооружены созревающей врожденной и адаптивной иммунной системой.В настоящее время риски значительно снижаются за счет вакцинации, которая стимулирует защитные иммунные реакции в созревающей иммунной системе. Тем не менее, дети все еще могут заразиться вирусными, бактериальными и паразитарными инфекциями, с которыми необходимо бороться и контролировать иммунные реакции. Такая стимуляция антигеном не только способствует выздоровлению, но и приводит к иммунологической памяти [41,42]. Таким образом, со временем защита, обеспечиваемая иммунным ответом, увеличивается, и молодые люди реже страдают от инфекций. Это накопление иммунологической памяти является развивающейся особенностью адаптивного иммунного ответа.Память сохраняется до старости [41], но затем может исчезнуть.
Помимо явных инфекций и прививок, новорожденный подвергается воздействию других антигенов. Он или она происходит из относительно стерильной среды in utero и затем быстро подвергается воздействию множества микробов [43]. Первый серьезный контакт с бактериями происходит во время прохождения через родовые пути, а затем, как только он / она вступает в оральный, кожный и респираторный контакт с окружающей средой. С этого момента воздействие микроорганизмов продолжается.Многие бактерии, колонизирующие кишечник и другие участки слизистой оболочки, необходимы для здорового образа жизни, включая переваривание пищи и получение жизненно важных питательных веществ. Они также влияют на развитие иммунной системы [44].
Примерно 20% всех лимфоцитов находятся в кишечнике [45], подвергаясь воздействию многих возможных чужеродных иммуногенов. Иммунные клетки кишечника контролируют границу с потенциально опасным источником инфекций. Кишечные бактерии влияют на развитие клеток Th27 [46], клеток T reg [47] и Т-клеток памяти [48–50].При рождении почти все Т-клетки несут гликопротеин CD45RA, типичный для наивных Т-клеток, которые никогда не сталкивались с чужеродным антигеном. Кроме того, в CD45RA-негативных CD4 Т-клетках имеется относительно большое количество regs Т . В детстве количество клеток T reg снижается, а клетки памяти Th2, Th27 и Th3 постепенно увеличиваются, чтобы сравняться с количеством наивных Т-клеток [51]. Хотя некоторые из этих Т-клеток памяти могли быть стимулированы инфекциями определенными патогенами и вакцинацией, многие из них могут быть активированы микробиомом не только в кишечнике, но также в дыхательных путях и коже.Эти примированные Т-клетки памяти могут отвечать на последующие инфекции посредством перекрестных реакций [48, 52, 53]. Например, взрослые, которые никогда не контактировали с ВИЧ-1, имеют в своем репертуаре Т-клетки памяти, которые реагируют с пептидами ВИЧ, представленными на клеточной поверхности белками HLA; эти Т-клетки, вероятно, снова пробудятся при возникновении ВИЧ-инфекции [48,50], как и другие микробы [52]. Перекрестная реактивность возникает из-за дискретных коротких (8-15 аминокислот) пептидов (эпитопов), которые входят в пептид-связывающие бороздки на молекулах HLA класса I или II на поверхности клетки и затем распознаются Т-клетками.Внутри последовательностей микробиома существует множество идеальных и почти идеальных совпадений с известными вирусными пептидными эпитопами, например, из ВИЧ-1 [48,50]. Они легко могут быть ответственны за создание Т-клеток памяти, специфичных для эпитопов патогенов, с которыми человек никогда не сталкивался.
Сегментированные нитчатые бактерии в кишечнике необходимы для развития клеток Th27 [47] и Clostridium spp. индуцируют клетки T reg толстой кишки [54,55]. У здоровых мышей наблюдаются иммунологические дефекты, в том числе меньшее количество пейеровских бляшек, более мелкие лимфоидные фолликулы и аномальные зародышевые центры в лимфоидной ткани тонкого кишечника [56].Этот иммунодефицит можно скорректировать за несколько дней, добавив одну мышь с нормальной кишечной флорой в клетку с стерильными животными [56,57]. Таким образом, данные на животных подтверждают мнение о том, что микробиом формирует развитие как Т-, так и В-клеток памяти.
Подобные события происходят и для В-клеток. Углеводные антигены групп крови ABO перекрестно реагируют с бактериальными антигенами кишечника и стимулируют ответы антител IgM. Антитела к белку gp41 ВИЧ-1 могут происходить из В-клеток, рецепторы антител которых перекрестно реагируют с белком Escherichia coli [58].
По мере роста ребенка иммунный репертуар также формируется интеркуррентными инфекциями и вакцинациями [59]. Патогенные инфекции могут быть задокументированы по симптоматическим заболеваниям, перенесенным ребенком или взрослым, но для многих вирусов, таких как грипп, инфекция может быть субклинической, но все же достаточной для стимуляции или усиления иммунного ответа [60]. Как правило, защита, обеспечиваемая иммунным ответом, как антителами, так и Т-клетками, очень эффективна. Большинство детских инфекций случаются только один раз, и тогда защита длится всю жизнь.
Поддержание долговременной B-клеточной памяти примечательно, учитывая, что иммуноглобулин IgG имеет период полураспада in vivo около 25 дней [61]. Плазматические клетки, продуцирующие антитела, которые развиваются во время иммунного ответа, мигрируют в костный мозг, где они живут очень долго. Кроме того, может происходить непрерывная регенерация В-клеток памяти, контактирующих с персистирующим антигеном и Т-хелперами. Антигены в виде частиц годами сохраняются в лимфатических узлах, удерживаемых фолликулярными дендритными клетками [62].Персистенция антигена и перекрестно-реактивные антигены, вероятно, помогают поддерживать жизнь этих В-клеток, время от времени делящихся и секретируя антитела.
Примечательно, что мать может передать достаточно антител, чтобы защитить своего ребенка, когда он был инфицирован 20–30 лет назад. Передача защитных антител от матери к ее ребенку чрезвычайно важна, особенно в средах, где 15% или более младенцев и детей умирают от инфекции. Парадоксально, но мать, которая избежала опасной детской инфекции благодаря коллективному иммунитету, может фактически подвергнуть своего ребенка риску, будучи неспособной передавать специфические защитные антитела.
Существует большое количество бессимптомных хронических инфекций, в основном вирусных, которые вызывают иммунные реакции. Примерами являются цитомегаловирус (ЦМВ), вирус Эпштейна-Барра (ВЭБ) и Mycobacterium tubercolosis ( Mtb ), но полный список длинный и продолжает расти [63]. EBV, CMV и Mtb вызывают очень сильные Т-клеточные ответы CD4 и CD8 у людей. ЦМВ-специфический ответ Т-лимфоцитов CD8 может привести к разрастанию олигоклональных Т-клеток, достигающих более 10% циркулирующих Т-лимфоцитов CD8.Эти Т-клетки важны, потому что они контролируют вирус, и их истощение, например, с помощью иммуносупрессивной терапии, может активировать инфекцию (например, Mtb, , EBV, CMV) с разрушительными последствиями.
Эволюция ответов антител в В-лимфоцитах подробно рассмотрена в другом месте [64]. Короче говоря, наивные В-клетки с рецепторами антител, специфическими для иммуногена, связывают антиген в зародышевом центре лимфатических узлов и получают частичный сигнал. Связанный антиген интернализируется и переваривается в лизосомах.Несколько образующихся пептидов связываются с молекулами HLA класса II этой клетки и затем представляются на поверхности клетки, где Т-фолликулярные хелперные клетки с соответствующими Т-клеточными рецепторами отвечают и доставляют дополнительные сигналы, включая IL-21, к В-клетке. Эти сигналы запускают деление В-клеток, переключение классов генов антител и соматическую гипермутацию. В этом случае предпочтение отдается В-клеткам, которые экспрессируют мутировавшие антитела, связывающие иммуноген с более высокой аффинностью. Отбор антител с лучшим связыванием продолжается в течение месяцев, что в конечном итоге приводит к получению антител с высоким сродством из сильно мутировавших генов зародышевой линии.Антитела с высоким сродством более эффективны при нейтрализации или опсонизации вторгшихся микробов и их патогенных продуктов.
Процесс соматической гипермутации не происходит в Т-клетках, даже если они имеют антителоподобные гены рецепторов Т-клеток, потому что наличие высокоаффинного Т-клеточного рецептора не дает никаких преимуществ. Связывание рецептора Т-клетки с комплексом пептид-HLA на антигенпрезентирующих клетках имеет низкое сродство. Он усиливается несколькими парами корецептор-лиганд, которые не являются антиген-специфическими, давая Т-клетке сигнал делиться и функционировать.
В результате иммунного заражения отвечающие Т- и В-клетки могут временно увеличиваться до очень больших количеств [65], иногда более 10% от всех циркулирующих Т-клеток, но они быстро сокращаются в результате активации клеток, индуцированных активацией. смерть и истощение в течение более длительного периода времени. Таким образом, когда патоген контролируется и исчезает, некоторые Т- и В-клетки памяти сохраняются в течение длительного времени в количестве, которое намного превышает количество наивных Т-клеток и Т-клеток «наивной памяти», которые были там до заражения.
По мере того, как человек становится старше, он или она развивает расширяющийся репертуар, включающий Т- и В-клетки памяти, вызванные предыдущими инфекциями и вакцинациями, а также репертуар наивной памяти, сформированный воздействием микробиома, пищевых антигенов и вдыхаемых антигенов. Учитывая большую сложность репертуаров Т- и В-клеток и большой стохастический элемент в выборе того, какие клетки будут реагировать на данный стимул, а также соматические мутации в В-клетках, точный состав будет отличаться у каждого человека, даже у монозиготных близнецов [ 66].Добавьте к этому значительную генетическую изменчивость в реакции людей, определяемую высокополиморфными генами HLA [67] и генами врожденного иммунитета, и неудивительно, что иммунные ответы любого взрослого человека значительно различаются.
(a) Беременность
Подробное изучение иммунологии беременности выходит за рамки настоящего обзора (см. [68,69]). Однако успешное размножение имеет центральное значение в эволюции и имеет иммунологические проблемы.Как новорожденный сохраняет механизмы, с помощью которых плод сводит к минимуму свои иммунные реакции на мать, обсуждалось выше. Еще большей загадкой является то, как мать переносит полуаллогенный трансплантат, не отвергая его и без иммуносупрессии, необходимой для принятия трансплантата органа [70]. На материнском интерфейсе трофобласта в месте первоначальной имплантации и в плаценте есть особенности, которые нарушают нормальный иммунный ответ отторжения трансплантата. К ним относятся экспрессия только неполиморфных неклассических антигенов HLA на трофобласте [71], локальное подавление иммунитета, опосредованное инфильтрацией NK-клеток [72], моноцитов и регуляторных Т-клеток [69,73], а также ингибирование активации Т-клеток. катаболизмом триптофана [74].Примерно во время имплантации местная воспалительная реакция создает стабильный участок плаценты [68]. Есть данные, что мать изменяет баланс своих Т-клеточных ответов на Th3, а не на Th2 [68]. Таким образом, у беременных женщин могут наблюдаться ремиссии аутоиммунного заболевания [75], и они более подвержены тяжелым осложнениям гриппа [76] и некоторых других инфекций. Эта иммунная модуляция, необходимая для благополучия плода, иногда может быть вредной для матери.
(b) Злокачественные новообразования и аутоиммунитет
Основная роль иммунной системы, вероятно, состоит в защите от инфекций.Другие роли, такие как разрушение мутировавших клеток, могут быть очень важны, но в большей степени в старости после размножения. Многие опухоли отключают Т-клетки, специфичные для опухолевых антигенов, путем связывания с рецепторами «контрольной точки», такими как PD-1 или CTLA4, и новые методы лечения, которые блокируют эти взаимодействия рецептор-лиганд, имеют большой терапевтический потенциал [77,78]. Однако побочные эффекты такой терапии и пассивного переноса противораковых Т-клеток включают аутоиммунные реакции, предполагающие баланс между реакциями против собственного иммунитета, предотвращающими рак и вызывающими аутоиммунитет [79].Во взрослой жизни баланс обычно работает, но у одной трети западных людей развивается рак, обычно в более позднем возрасте, в то время как у 5–10% развивается клиническое аутоиммунное заболевание, поэтому баланс точно установлен и со временем может измениться. Ослабление иммунной системы в пожилом возрасте (см. Ниже) может улучшить аутоиммунитет, но за счет повышенного риска рака.
Микроорганизмы вызывают около четверти всех видов рака (например, ВЭБ, вирусы гепатита В и С, вирус папилломы человека и Helicobacter pylori ).Специфические Т-клеточные реакции обычно сдерживают эти микробы. Однако, если иммунитет нарушен в результате старения (см. Ниже), иммуносупрессивной терапии или определенных инфекций, особенно ВИЧ-1, эти виды рака возникают [80].
Таким образом, если в раннем детстве развился полностью эффективный иммунный ответ, он созревает по мере накопления памяти и поддерживает здоровье человека в критические периоды жизни, включая деторождение. Он не только защищает от потенциально смертельных инфекций, но также контролирует ряд устойчивых инфекций, некоторые из которых могут вызвать рак.Он также может иметь дело с мутантными клетками, которые могут стать злокачественными. Он может быть чрезмерно реактивным и вызывать аутоиммунное заболевание или аллергию, что является платой за общую пользу.
4. Снижение иммунитета с возрастом
Последняя сцена из всех,
На этом заканчивается эта странная, насыщенная событиями история,
Это второе ребячество и простое забвение,
Без зубов, без глаз, без вкуса , без всего.
С возрастом иммунная система подвергается глубокому ремоделированию и ухудшению, что существенно влияет на здоровье и выживаемость [81,82].Это иммунное старение предрасполагает пожилых людей к более высокому риску острых вирусных и бактериальных инфекций. Более того, уровень смертности от этих инфекций в три раза выше среди пожилых пациентов по сравнению с более молодыми взрослыми пациентами [83]. Инфекционные заболевания по-прежнему являются четвертой по частоте причиной смерти пожилых людей в развитом мире. Кроме того, аберрантные иммунные ответы у пожилых людей могут усугублять воспаление, возможно, способствуя возникновению других бедствий старости: рака, сердечно-сосудистых заболеваний, инсульта, болезни Альцгеймера и деменции [84].
Во время обычного сезона гриппа около 90% дополнительных смертей происходит среди людей старше 65 лет. Более того, слабый иммунный ответ является причиной снижения эффективности вакцин [82,85]. Иммунное старение также приводит к реактивации латентных вирусов, таких как вирус ветряной оспы, вызывая опоясывающий лишай и хроническую невралгию.
Ухудшение иммунной системы с возрастом может нарушить гомеостатическое равновесие между микробиотой и хозяином. Таким образом, снижение бактериального разнообразия в кишечнике коррелирует с диареей, связанной с Clostridium difficile, , основным осложнением для пожилых людей в больницах [86].Более того, отклонения от профиля кишечной микробиоты, установленного в молодости, связаны с воспалительными заболеваниями кишечника [87]. Увеличение с возрастом количества провоспалительных патобионтов и уменьшение количества иммуномодулирующих видов может способствовать развитию воспалительных заболеваний и поддерживать их [86].
В то же время стареющая иммунная система не может поддерживать полную толерантность к аутоантигенам, что приводит к увеличению числа аутоиммунных заболеваний. [88]. Вероятно, это связано с лимфопенией, возникающей с возрастом, что приводит к избыточной гомеостатической пролиферации лимфоцитов [89], а также к снижению регуляторной функции Т-клеток и уменьшению клиренса апоптотических клеток макрофагами [81].
Рак чаще всего встречается у пожилых людей; средний возраст для диагностики рака в промышленно развитых странах приближается к 70 годам. Основная причина, очевидно, в накоплении клеточных и генетических повреждений на протяжении всей жизни; однако, учитывая роль иммунного ответа в борьбе с раком, снижение иммунных функций у пожилых людей должно способствовать более высокому риску [90]. Это иммунное нарушение явно противоречит увеличению аутоиммунитета, поскольку противоопухолевые реакции могут быть направлены против самого себя; однако, вероятно, преобладает общий упадок иммунной системы, и опухоли больше не отторгаются столь же эффективно.Более того, усиление воспаления, обнаруживаемое с возрастом, способствует возникновению рака.
Повышенная заболеваемость из-за ослабления иммунной системы является прямым следствием нарушения регуляции адаптивного иммунитета у пожилых людей. Низкое количество наивных Т-лимфоцитов по сравнению с Т-лимфоцитами [41,42] является следствием сниженного выхода тимуса из инволютивного тимуса. Вследствие этой возрастной лимфопении Т-клетки пролиферируют и увеличивают объем «виртуальной памяти» [91], но в то же время способность устанавливать иммунологическую память в ответ на антигены de novo снижается, что ставит под угрозу вакцинацию.Нарушаются такие функции, как продукция цитокинов Т-клетками CD4 и CD8, изменяется экспрессия ключевых поверхностных маркеров, и соотношение CD4 + к CD8 + Т-клеток инвертируется [81]. Расширенные ответы Т-клеток, которые удерживают под контролем латентные вирусы, такие как ВЭБ и ЦМВ, сокращают пространство для Т-клеток CD8 + , специфичных для других потенциально летальных вирусов [92], усугубляемых снижением выработки наивных Т-клеток тимуса.
Хотя количество периферических В-клеток не уменьшается с возрастом, состав этого компартмента меняется.Подобно Т-клеткам, наивные В-клетки заменяются клетками памяти, испытавшими антиген, некоторые из которых «истощены» (CD19 + IgD — CD27 — ), и они демонстрируют пониженное созревание аффинности и переключение изотипа [81 ].
В целом изменения в компартментах Т- и В-клеток препятствуют адекватному иммунному ответу на новые острые и латентные вирусные инфекции и вакцинации.
Врожденный иммунный ответ также снижается с возрастом. Наблюдаются изменения в количестве врожденных клеток со смещением гематопоэза в сторону миелоидных клонов [93,94].Старые нейтрофилы менее функциональны с пониженной фагоцитарной способностью и выработкой супероксида, отчасти из-за снижения экспрессии рецептора Fc γ [95]. Точно так же у стареющих макрофагов снижается респираторный выброс. Вместе с DC они обнаруживают сниженную фагоцитарную функцию и экспрессию HLA II [81]. Таким образом, иммунологическое «молчаливое» удаление апоптозных и возрастающих количеств стареющих клеток ставится под угрозу и может способствовать провоспалительному фенотипу. Действительно, когда у старых мышей искусственно удаляли стареющие клетки, животные жили дольше и были здоровее [96].
Возможно, наиболее важным изменением в стареющей врожденной иммунной системе является увеличение провоспалительных цитокинов IL-1β, IL-6, IL-18 и TNFα [97]. Возникающее в результате воспаление низкой степени, вероятно, способствует атеросклерозу, деменции и раку, неразрывно связывая воспаление и старение других тканей [84,98].
Клеточные и молекулярные основы иммунного старения еще недостаточно изучены. Три фенотипа характеризуют стареющие клетки: истощение теломер, сопровождающее каждый раунд пролиферации, ведущее к остановке деления клеток или «репликативному старению»; повышенная митохондриальная нагрузка / дисфункция и активные формы кислорода; и секреторный фенотип, связанный со старением (SASP), определяемый как секреция провоспалительных цитокинов, хемокинов и протеаз стареющими клетками [99].Хотя большинство данных было получено на фибробластах, стареющие иммунные клетки, вероятно, обладают схожими характеристиками. Эти свойства влияют на митотически активные клетки путем истощения или остановки деления (например, гемопоэтические стволовые клетки — HSC или Т-клетки), а также на постмитотические иммунные клетки, вызывая клеточную дисфункцию (например, нейтрофилов).
Истощение теломер является защитным механизмом против рака, так как каждый раунд пролиферации может вносить мутации [100]. Только эпителиальные лимфоциты и стволовые клетки, включая гемопоэтические (HSC), экспрессируют удлиняющий теломеры фермент теломеразу у взрослых [101], что требует тщательного баланса с риском рака.Как Т-клетки памяти, так и HSC обычно делятся редко, чтобы минимизировать истощение теломер, но надежно либо в ответ на инфекцию (лимфоциты памяти), либо для обновления тканей (стволовые клетки) на протяжении всей жизни. На конечной стадии стареющие CD27 — CD28 — Т-клетки имеют самые короткие теломеры и демонстрируют сниженную пролиферацию после активации, но тем не менее обладают мощными эффекторными функциями. Эти клетки накапливаются в пожилом возрасте и у пациентов с аутоиммунными заболеваниями и хроническими вирусными инфекциями [102].Вторая характеристика старых клеток — усиление митохондриальной дисфункции и, как следствие, окислительное повреждение белков и ДНК. Функция DC у старых мышей может быть восстановлена путем введения антиоксидантов [103]. Окислительный стресс вызывает разрывы ДНК и может быть причиной истощения теломер, которое связывает первые две причины старения. Накопление окислительного повреждения может быть связано со снижением лизосомальной функции и аутофагии [104]. Аутофагия, разрушающая объем цитоплазматического материала путем доставки его к лизосомам, снижается с возрастом, в том числе в человеческих CD8 + Т-клетках [105].Мыши без аутофагии в их кроветворной системе обнаруживают преждевременно состарившуюся кроветворную систему [106]. Отсутствие реакции Т-клеток памяти на вакцинацию против гриппа, наблюдаемую у пожилых людей, можно восстановить с помощью соединения, индуцирующего аутофагию [107]. Третьим более недавним дополнением к этим фундаментальным изменениям старых клеток является приобретение SASP, способствующего повышенной секреции провоспалительных цитокинов и слабому воспалению [99].
5. Эволюция иммунной системы человека
Будучи долгоживущими видами, люди развили механизмы врожденного иммунитета и иммунологической памяти, чтобы выжить при повторных инфекциях.Однако на протяжении жизни человека эти иммунные механизмы изменяются, сначала для адаптации к переходу от плода к младенцу, а затем к созреванию и расширению во время роста, слегка изменяясь во время беременности и, наконец, уменьшаясь в процессе старения. Выход наивных лимфоидных клеток и способность формировать новую иммунологическую память становятся все менее важными, поскольку пожилой человек столкнется и установит банк памяти для многих патогенов в течение своей жизни. Существует вероятность того, что миелоидный сдвиг и повышенная секреция провоспалительных цитокинов во время старения важны для улучшения фагоцитоза увеличивающегося числа стареющих клеток, что поднимает вопрос о том, могут ли изменения в стареющей иммунной системе служить цели.
Иммунная система была в первую очередь сформирована эволюцией, чтобы эффективно реагировать на острые инфекции у молодых людей, адаптироваться к беременности и передавать защиту младенцам, а также адаптирована для борьбы со многими хроническими инфекциями, длящимися десятилетиями. Помимо борьбы с вирусами, бактериями, грибками и паразитами, иммунная система также берет на себя другие функции, такие как восстановление тканей, заживление ран, удаление мертвых и раковых клеток и формирование здоровой микробиоты кишечника. Предполагая отсутствие серьезного избирательного давления на людей старше репродуктивного возраста, нам, возможно, придется платить за генетические черты, выбранные для обеспечения приспособленности в раннем возрасте, за счет более позднего развития иммунологических фенотипов, таких как хроническое воспаление.Массовое старение и повышенная долговечность — это недавние явления, происходящие в оптимизированной среде. Как предположил Хейфлик [108], старение может быть артефактом цивилизации, и, следовательно, изменения в стареющей иммунной системе могут быть просто следствием эволюционного непредсказуемого воздействия антигена на протяжении всей жизни человека.
В некоторых аспектах иммунная система пожилого организма напоминает иммунную систему новорожденного, со сниженной антимикробной активностью нейтрофилов и макрофагов, сниженной презентацией антигена DC и уменьшенным уничтожением NK, а также несколько нарушенными адаптивными ответами лимфоцитов.Таким образом, как очень молодая, так и старая иммунная система одинаково подвержены риску справиться с типичной вирусной инфекцией, такой как грипп, тогда как молодой (небеременный) взрослый организм, по-видимому, идеально подходит для этой задачи (). Эволюция иммунной системы внутри индивидуума, возможно, отражает центральную роль молодого взрослого человека в выживании вида благодаря его репродуктивному потенциалу.
У детей иммунная система сильнее, чем у взрослых? — Мануальный терапевт — Парк Ридж, штат Иллинойс,
Исследования показывают, что у молодых людей иммунная система НЕ так эффективна, как у взрослых.Дети могут быть предрасположены к контакту с вирусной инфекцией, и им требуется больше времени, чтобы вылечиться от нее. Это верно по ряду причин. Дети постоянно растут, они едят больше еды, пьют больше воды и дышат большим количеством воздуха, чем взрослые.
Экологические токсиныЦентральная нервная, репродуктивная, пищеварительная и иммунная системы детей все еще находятся в стадии развития. На этой уязвимой стадии определенные токсичные вещества окружающей среды могут нанести непоправимый ущерб. Маленькие дети ползают по земле и полу.Они кладут вещи в рот и без разбора делятся игрушками с другими детьми и домашними животными. Пестициды, другие химические вещества, пыль и отходы могут загрязнить почву во дворе и попасть в ваш дом. Они более восприимчивы к загрязнению воздуха и пассивному курению. Химические вещества и гормоны в пище, которую едят дети, особенно «детские» блюда, такие как хот-доги, макароны с сыром, также могут иметь влияние.
Иммунные системыИммунная система состоит из группы клеток, белков, тканей и органов, которые борются с болезнями, микробами и другими захватчиками.Когда в организм попадает небезопасное вещество, иммунная система срабатывает и атакует. У детей нет полностью развитой иммунной системы до 7-8 лет. Поскольку иммунная система помогает организму бороться с болезнями и инфекциями, у детей повышен риск развития состояний, таких как коклюш, диарея, ушные инфекции, ветряная оспа, круп и пищевая аллергия, по сравнению со взрослыми.
Развитие сильной иммунной системы Младенцы
Младенцы получают выгоду от воздействия материнской иммунной системы через грудное молоко.Исследования показывают, что у детей, находящихся на грудном вскармливании, меньше шансов заболеть инфекциями (особенно легочными, ушными инфекциями и диареей) в течение первого года жизни по сравнению с детьми, которых кормят смесями. Это связано с тем, что грудное молоко матери содержит важные антитела, ферменты, жиры и белки, которые помогают укрепить иммунную систему ребенка.
Малыши и дошкольники <
По мере того, как ваш ребенок становится более уязвимым из-за контакта с другими, вероятность заболевания простудой и вирусами возрастает.Некоторые исследования показывают, что это помогает укрепить иммунную систему вашего ребенка. Однако никто не хочет видеть, как страдают их дети. Практика и обучение правилам гигиены дома наряду с другими методами повышения иммунитета могут уменьшить тяжесть и продолжительность болезни вашего ребенка. Когда ваш ребенок достигает 7-8 лет, большая часть его иммунной системы развивается.
Целостный подход к повышению иммунитета
В своей практике в Active Health мы верим в целостный (целостный) подход к здоровью и благополучию.С этой целью мы считаем, что обучение пациентов является ключом к созданию для наших пациентов здоровой среды для себя и своих семей. Мы перечислили некоторые из наиболее важных вещей, которые вам следует знать, если вы хотите повысить иммунитет своих детей:
Грудное вскармливание Полноценное питание: рекомендуется диета, богатая фруктами и овощами со здоровым балансом белков и жиров. для поддержания сильного организма и иммунной системы.
витаминов и минералов может быть еще одним ключевым фактором в поддержании вашей иммунной системы.При составлении рекомендаций по питанию вашего ребенка следует учитывать витамины, поддерживающие иммунную систему, такие как витамины A, C, E и незаменимые жирные кислоты. Кроме того, в рамках плана здорового питания не следует упускать из виду адекватное потребление минералов, таких как марганец, селен, цинк, медь, железо, сера, магний и германий.

 п.).
п.).



 Может выступать следствием перенесенной болезни или особенным состоянием пациента (например, при регулярных физических нагрузках необходимы белки и аминокислоты).
Может выступать следствием перенесенной болезни или особенным состоянием пациента (например, при регулярных физических нагрузках необходимы белки и аминокислоты).