Восстановление двигательных функций после инсульта: Восстановление двигательных функций после инсульта
Восстановление двигательных функций после инсульта
Реабилитация после инсульта – это наобходимость!
Специальный курс восстановления двигательных функций после инсульта поможет устранить последствия поражения центральной нервной системы и позволит вернуться к полноценной жизни.Верните себе активность — запишитесь на курс!
Инсульт – нарушение мозгового кровообращения, которое приводит к различным последствиям, таким как частичный или полный паралич, потеря речи, памяти, слуха. Причинами развития инсультов могут быть высокое артериальное давление, нарушения ритма сердца, повышенное содержание сахара и холестерина в крови, избыточный вес, нарушение свёртываемости крови, вредные привычки.
Виды инсульта
Геморрагический инсульт
Геморрагический инсульт – в результате высокого давления и истончения стенки кровеносного сосуда происходит его разрыв с кровотечением непосредственно в ткань и/или под оболочки и/или в желудочки головного мозга.
Ишемический инсульт
При данном виде инсульта сохраняется целостность стенок сосудов, но прекращается приток крови, вследствие спазма или закупорки тромбом либо холестериновой бляшкой.
Внимание! Медцентр EVOLIFE оказывает помощь в восстановлении после инсульта на втором позднем восстановительном периоде и третьем периоде отдалённых действий.
Как пройти курс восстановления после инсульта в медцентре EVOLIFE
Записаться на приём врача невролога Программа назначается врачом неврологом (возможен выезд на дом). На первичном приеме врач-невролог изучает историю болезни и сопутствующие показания. Затем проверяет общее состояние пациента, проводит его осмотр и составляет курс лечения с учетом показаний и противопоказаний к лечебным процедурам, устанавливает их параметры и продолжительность.
Что входит в курс реабилитации после инсульта
Кинезиотерапия (ЛФК)
В нашей клинике широко применяются методики физической реабилитации, разработанные для дисфункций и поражения центральной нервной системы в сочетании с физиотерапией и массажем.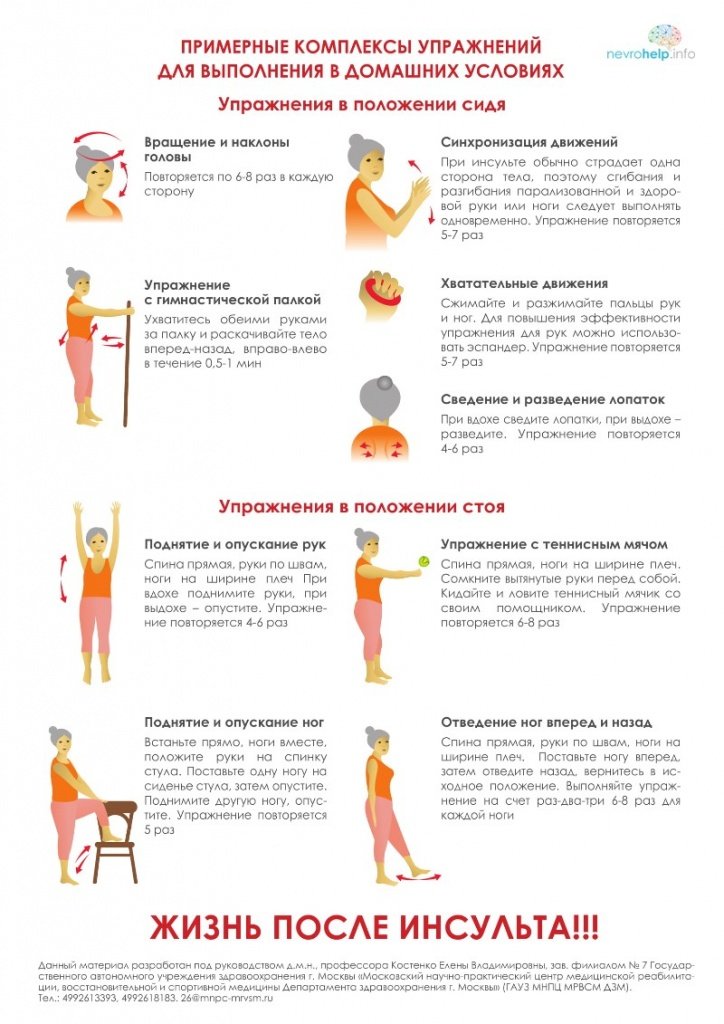 Эффективным методом восстановления двигательных функций в паретичных конечностях является кинезотерапия (ЛФК), физические нагрузки с применением специально разработанных тренажеров.
Эффективным методом восстановления двигательных функций в паретичных конечностях является кинезотерапия (ЛФК), физические нагрузки с применением специально разработанных тренажеров.
Выполнение соответствующих упражнений стимулирует формирование новых межнейронных связей. А также ЛФК способствует более активному восстановлению навыков самообслуживания после инсульта.
Криотерапия, аппаратная кинезиотерапия и электролечение
Чтобы достигнуть более весомых результатов в борьбе со спастичностью мышц и с гипертонусом верхних конечностей используют комплексный подход, включающий применение физиотерапевтических методов (криотерапия, электролечение, аппаратную кинезиотерапию)
Массаж после инсульта
Массаж после инсульта — очень важная часть реабилитационного процесса. Однако целебное воздействие возможно лишь при правильном проведении.
Применять массаж желательно в сочетании с остальными видами лечения: медикаментозным восстановлением, ЛФК и прочей физиотерапией.
В нашем медицинском центре работают специалисты только с медицинским образованием и стажем не менее 8 лет.
Записаться консультацию по восстановлению после инсульта в медцентре EVOLIFE
Чтобы записаться на консультацию, позвоните нам по телефону или оставьте заявку на сайте клиники «Эволайф» в удобное для вас время.
Восстановление после инсульта: этапы реабилитации и сроки
Главная цель реабилитации после инсульта — это восстановление тех навыков, которые потерял человек. Реабилитация не продлевает жизнь, но она способна значительно улучшить качество жизни и избежать второго удара.
В зависимости от тяжести осложнений и способности человека восстанавливаться, подбирается индивидуальная программа восстановления после инсульта.
Когда начинать реабилитацию после инсульта?
При инсульте кровоснабжение мозга нарушается, а нервная ткань в зоне поражения начинает отмирать. Как следствие — нарушение функций, за который определенный участок мозга нес ответственность. Узнать причины инсульта вы можете здесь.
Узнать причины инсульта вы можете здесь.
Нервная система способна заменить погибшие клетки и связи на новые. Этот процесс называется нейропластичностью. Главная задача нейрореабилитации заключается в том, чтобы направить процесс восстановления мозга в правильное русло. Чем быстрее начать процесс восстановления после инсульта, тем выше вероятность восстановить утраченные навыки и способности.
Роль времени в процессе восстановления после инсульта
Первые три месяца после инсульта считаются пиком восстановления. Именно в этот срок можно вернуть более 50% утраченных функций. Тогда как в последующие 3 месяца — не более 30%, а следующие полгода лишь 20%.
Время играет одну из основных ролей в процессе восстановления. Чем раньше начать реабилитацию, тем выше ее эффективность.
Восстановительные периоды:
- Острый этап реабилитации начинается в течение 24-48 часов после инсульта в больнице неотложной помощи.

- Ранний восстановительный период — это первые 6 месяцев после инсульта. Но именно для восстановления двигательных функций очень важно начать лечение в первые 3 месяца. Именно в этот период важно обратиться в реабилитационный центр, чтобы комплексно подойти к восстановлению;
- Поздний период — это период от полугода до 1 года после инсульта. Реабилитацию можно проводить как амбулаторно, так и на дому;
- Резидуальный (отдаленный) период после 1 года проводится как на дому, так и в медучреждении.
Сколько длится восстановление после инсульта?
Скорость восстановления после инсульта зависит от многих факторов:
- типа инсульта, обширности поражения мозга;
- качества и сроков оказания первой помощи;
- срока начала и объема реабилитации;
- профессионализма врачей и реабилитологов;
- эмоционального состояния пациента и его желания быстрее встать на ноги.

Нет стандартных сроков для восстановления, но благодаря правильно составленному плану реабилитации, комплексному подходу реабилитологов, психологов, неврологов и желанию пациента, можно достичь улучшения состояния на каждом этапе реабилитации.
Возможно ли полное восстановление после инсульта?
Полное восстановление всех функций после инсульта вполне возможно, поскольку в процессе реабилитации принимают участие множество специалистов:
- реабилитолог занимается лечением текущих и профилактикой будущих осложнений, медикаментозной терапией;
- физиотерапевт отвечает за восстановление двигательных функций, подбирает индивидуальные методики лечения;
- эрготерапевт восстанавливает социально-бытовой аспект жизни;
- кинезиотерапевт занимается физической реабилитацией пациента с помощью движения;
- логопед работает над восстановлением речи и глотания;
- нейропсихолог помогает справиться с депрессий, апатией, восстанавливает память;
- психологи трудятся над восстановлением поведенческо-когнитивных функций.

Профессиональная команда работает над полным восстановлением утраченных функций пациента, применяя различные методы лечения.
Физическая активность включает:
- Упражнения для моторных навыков;
- Обучение мобильности;
- Контраст-индуцированная терапия;
- Терапия диапазона движений.
Физическая деятельность может включать:
- Функциональная электрическая стимуляция;
- Эрготерапия;
- Кинезиотерапия.
Занятия с психологом и логопедом— терапия когнитивных расстройств, нарушения общения и речи.
Альтернативная медицина: массаж, акупунктура (иглоукалывание) и кислородная терапия.
Где можно пройти реабилитацию после инсульта?
Реабилитация начинается в течение 48 часов после инсульта в больнице. После выписки, вам следует обратиться в реабилитационный центр как можно быстрее, чтобы восстановление прошло с наибольшей эффективностью. Реабилитационный центр “Аксимед” в г. Киев оснащен ультрасовременным оборудованием, новейшими тренажерами и аппаратами. Врачи-неврологи и реабилитологи прошли обучение в Германии.
Реабилитационный центр “Аксимед” в г. Киев оснащен ультрасовременным оборудованием, новейшими тренажерами и аппаратами. Врачи-неврологи и реабилитологи прошли обучение в Германии.
Мультицисциплинарный подход признан лучшей методикой в мире по восстановлению клеток головного мозга после инсульта. В нашем центре восстановление включает в себя двигательную, адаптационно-бытовую и психо-эмоциональную (речевую, когнитивную) реабилитацию.
Для нас важен каждый пациент! Весь коллектив работает, чтобы как можно быстрее вернуть человека к нормальной полноценной жизни после инсульта.
Восстановление после инсульта
ПОКАЗАНИЯ ДЛЯ ПРОВЕДЕНИЯ РЕАБИЛИТАЦИИ ПОСЛЕ ИНСУЛЬТА
- нарушение двигательных функций
- координаторные нарушения
- речевые нарушения
РЕАБИЛИТАЦИЯ ПОСЛЕ ИНСУЛЬТА В РКМЦ
В нашем Центре мы обеспечиваем индивидуальное мультидисциплинарное сопровождение на каждом этапе реабилитации пациентов, перенесших нарушение кровообращение головного мозга.
Инновационный стол-вертиклизатор Erigo Pro (Hocoma, Швейцария) с интегрированным роботизированным устройством и встроенной синхронизированной функцией электростимуляции мышц нижних конечностей обеспечивает поддержание нормальной жизнедеятельности организма лежачего больного. Возможность ранней вертикализации позволяет нормализовать кровообращение, предупредить возникновение пролежней, застойных явлений в легких и пневмоний, тромбоза вен нижних конечностей, мышечной спастики и контрактуры суставов.
Следующая задача — восстановление нарушенных функций и способностей. На каждом этапе восстановления с пациентом работают опытные специалисты по физической реабилитации.
На ранних этапах важно сохранить движения в суставах конечностей, предупредить развитие контрактур. С этой целью проводится пассивная гимнастика, которую сочетают с лечением положением, пассивной имитацией ходьбы, дыхательными упражнениями и массажем конечностей.
С этой целью проводится пассивная гимнастика, которую сочетают с лечением положением, пассивной имитацией ходьбы, дыхательными упражнениями и массажем конечностей.
В дальнейшем приступают к тренировке активных движений, обучению поддержания положения сидя.Устранение двигательных и координаторных нарушений проводится на новейшем оборудовании с применением технологий биологической обратной связи. Уникальные многофункциональные реабилитационные тренажеры Amadeo, Tymo, Pablo (Tyromotion GmbH, Австрия) для оценки и коррекции нарушений моторики верхних и нижних конечностей, туловища. Тренировки осуществляются при помощи интерактивных программ, что обеспечивает поддержание внимания, когнитивных функций и мотивации.
В восстановлении двигательных функций и бытовых навыков мы применяем также такие методы, как эрготерапия и зеркальная терапия.
Важной задачей после инсульта является восстановление навыков ходьбы. Пациенты поэтапно обучаются поддерживать положение стоя, восстанавливать правильную походку. Система с беговой дорожкой для обучения навыкам ходьбы с разгрузкой веса H/P/COSMOS Robowalk expander (HPCOSMOS, Германия) позволяет ускорить процесс восстановления двигательных функций.
Пациенты поэтапно обучаются поддерживать положение стоя, восстанавливать правильную походку. Система с беговой дорожкой для обучения навыкам ходьбы с разгрузкой веса H/P/COSMOS Robowalk expander (HPCOSMOS, Германия) позволяет ускорить процесс восстановления двигательных функций.
Дополнительным эффективным доступным нам методом в реабилитации является кинезиотейпирование. Коррекция мышечного тонуса с помощью эластичных, наклеиваемых на кожу, хлопковых лент способствует восстановлению функции пораженных конечностей.
Не менее важна психологическая и социальная адаптация пациентов, перенесших инсульт. Эту задачу решают опытные психологи, психотерапевты, логопед на каждом реабилитационном этапе.
На поздних сроках реабилитации проводится восстановительная гимнастика в воде. Бассейн в отделении реабилитации и физиотерапии оборудован специальным подъемником для комфорта и безопасности пациентов с ограниченными возможностями, а также водными тренажерами.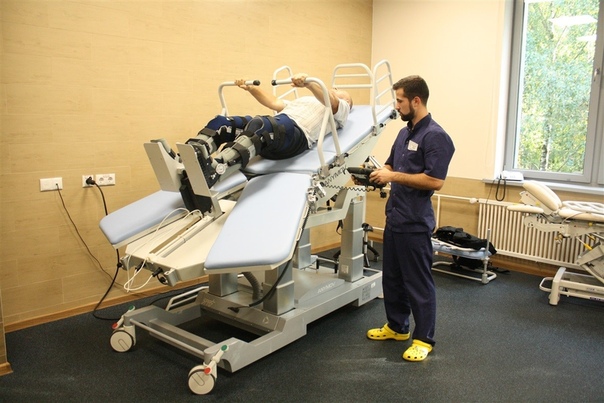
Также в поздние сроки восстановления применяется широкий спектр физиотерапевтического воздействия, бальнеолечения, массаж, рефлексотерапия.
ПРОТИВОПОКАЗАНИЯ
Тяжелое состояние пациента.
КАК ПРОЙТИ РЕАБИЛИТАЦИЮ ПОСЛЕ ИНСУЛЬТА В РКМЦ
С целью восстановительного лечения и реабилитации возможна госпитализация пациентов в стационар нашего Центра. (Госпитализация осуществляется по согласованию с неврологом РКМЦ).
Для этого нужно:
- Позвонить в Контакт-центр для записи на консультацию к врачу-неврологу
- Прийти на прием в назначенное время с имеющимися у вас медицинскими документами.
- В день госпитализации в регистратуре заключить договор на оказание платных услуг
- Оплатить счет в кассе РКМЦ или через ЕРИП
Помощь в восстановлении и реабилитации после инсульта в Москве
Наиболее тяжелыми последствиями инсульта являются нарушения речевых и двигательных функций.:max_bytes(150000):strip_icc()/health-worker-assisting-a-disabled-woman-in-walking-126172526-59c920f9c412440010f8f22b.jpg) Они проявляются по-разному и отмечаются примерно у 70% людей, переживших это заболевание. Утраченные способности со временем, как правило, возвращаются, но риск инвалидности всегда существует и беспокоит пациентов. Восстановить здоровье и вернуться к привычной жизни помогают своевременно оказанная медицинская помощь и правильно организованная реабилитация после инсульта.
Они проявляются по-разному и отмечаются примерно у 70% людей, переживших это заболевание. Утраченные способности со временем, как правило, возвращаются, но риск инвалидности всегда существует и беспокоит пациентов. Восстановить здоровье и вернуться к привычной жизни помогают своевременно оказанная медицинская помощь и правильно организованная реабилитация после инсульта.
Чем опасен инсульт? Возможные осложнения и последствия
Приступ инсульта может продолжаться от 2 до 24 часов. Расстройство мозгового кровообращения приводит к отмиранию нервных клеток, разрыву сосудов, отеку мозга. Эти процессы не протекают бессимптомно. Первые признаки опасной патологии – сильная головная боль, тошнота, рвота. Затем появляются неврологические симптомы:
- расстройства координации;
- трофические и когнитивные нарушения;
- ухудшение зрения и слуха;
- потеря памяти;
-
парезы и парализация разных участков тела.

Некоторые симптомы проходят вскоре после приступа, но начавшееся отмирание клеток мозга уже не остановить. Чем раньше будет оказана медицинская помощь, тем выше шанс сохранить жизнь больному и восстановить его здоровье. После инсульта человек лишается возможности нормально общаться, чувствовать и передвигаться, зачастую страдает психика.
Чтобы избавить больного от опасных осложнений и помочь восстановить здоровье, требуется участие опытных специалистов. Лечиться дома небезопасно. Контролировать процессы, протекающие в организме, и правильно планировать лечебно-восстановительные мероприятия способны только квалифицированные врачи.
В какой помощи нуждаются люди, пережившие инсульт?
Реабилитация после инсульта должна быть комплексной, так как последствия болезни влияют на все системы и функции организма. Коррекция нарушений и восстановление утраченных способностей могут занять длительное время. Сроки зависят от вида инсульта (ишемический, геморрагический), степени поражения головного мозга, возраста больного. Пожилым людям, как правило, требуется больше времени на восстановление, так как обновление клеток идет медленнее, чем в молодости, а имеющиеся хронические болезни сердца и сосудов затрудняют лечение.
Пожилым людям, как правило, требуется больше времени на восстановление, так как обновление клеток идет медленнее, чем в молодости, а имеющиеся хронические болезни сердца и сосудов затрудняют лечение.
На разных этапах восстановительного лечения применяются:
- Медикаментозная терапия с помощью препаратов, улучшающих кровообращение и обменные процессы в головном мозге.
- Лечебная гимнастика для стимуляции физической активности. Правильно подобранные упражнения компенсируют бездействие погибших нервных клеток.
- Классический и точечный массаж, повышающий тонус мышц.
- Социальная адаптация. После инсульта многим пациентам приходится заново учиться ходить, говорить, координировать движения, обслуживать себя. На этом этапе очень важны профессиональная помощь врачей и поддержка близких. Быстрее освоиться и избежать стрессов помогают психологи.
-
Коррекция питания.
 Для успешного восстановления необходим сбалансированный рацион, исключающий тяжелую пищу (жирное, копченое, сладкое и т.д.) В меню должны быть фрукты, злаковые, овощи, постное мясо. Для установления правильного режима питания бывает необходима помощь диетолога.
Для успешного восстановления необходим сбалансированный рацион, исключающий тяжелую пищу (жирное, копченое, сладкое и т.д.) В меню должны быть фрукты, злаковые, овощи, постное мясо. Для установления правильного режима питания бывает необходима помощь диетолога.
При нарушениях легкой и средней степени возможно пребывание пациента дома с регулярным медицинским контролем. При тяжелых формах больному желательно находиться в стационаре под постоянным присмотром врачей.
Восстановительное лечение после инсульта в ЦКБ РАН
После инсульта жизнь продолжается, и то, какой она будет, во многом зависит от качества лечения и реабилитации в первые 2–3 месяца после болезни. В отделении реабилитации ЦКБ РАН для пациентов составляются индивидуальные программы, направленные на восстановление двигательных функций, коррекцию расстройств внимания, речи и памяти, других неврологических нарушений.
В реабилитации участвуют врачи разных специальностей: физиотерапевты, логопеды, психологи и нейропсихологи, диетологи, эрготерапевты и другие специалисты. Совместная работа профессионалов, а также использование инновационного оборудования сокращают риск развития осложнений и ускоряют процесс выздоровления.
Совместная работа профессионалов, а также использование инновационного оборудования сокращают риск развития осложнений и ускоряют процесс выздоровления.
Для записи на консультацию и уточнения стоимости услуг можно позвонить по телефону +7 (499) 400 47 33 или воспользоваться специальной формой на сайте.
Здесь человека учат заново — и ходить, и улыбаться
Время для визита заведующая отделением назначила по телефону: восемь утра. И мягко дала понять, что опаздывать у них не принято. Сразу за проходной нас встретили ее коллеги и повели удивлять.
За те несколько минут, пока фотокор «РГ» примерял разные объективы и выбирал точку съемки, железный Lokomat и подключенный к нему условный пациент прошагали условные 128 метров.
Рабочая информация высветилась на дисплее, и доктор Клочков предложил коллеге, который согласился исполнить для нас роль пациента, поменять «разгрузку». Иными словами, уменьшить или увеличить вес его тела, чтобы тем самым изменить давление на суставы и нижние конечности.
На участке роботизированной терапии, где установлены аппараты Lokomat, это возможно. А сами эти роботы нужны для восстановления навыков, утраченных в результате инсульта или другой беды.
— У нас такие аппараты используются для обучения правильной ходьбе в процессе реабилитации, — Антон Клочков немногословен и строг в формулировках. — Тут главное — соединить роботизированную механизацию с биомеханикой человека. Это аппарат швейцарский. Он позволяет дозировать нагрузку на нижние конечности и задавать желаемое мышечное усилие: от 5 процентов (остальные 95 — берет на себя робот) до 100, когда все или почти все человек уже делает сам.
Чем это хорошо? У врача, а значит, и у пациента есть выбор, при каком состоянии какую нагрузку задать. При этом робот контролирует, чтобы само движение выполнялось по правильной циклограмме, а у пациента есть свобода в выборе усилия. Можно разгружать и нагружать избирательно, по отдельным суставам — в колене, в бедре…
— Мы не учим тут чему-то новому, — вступают в разговор коллеги Антона.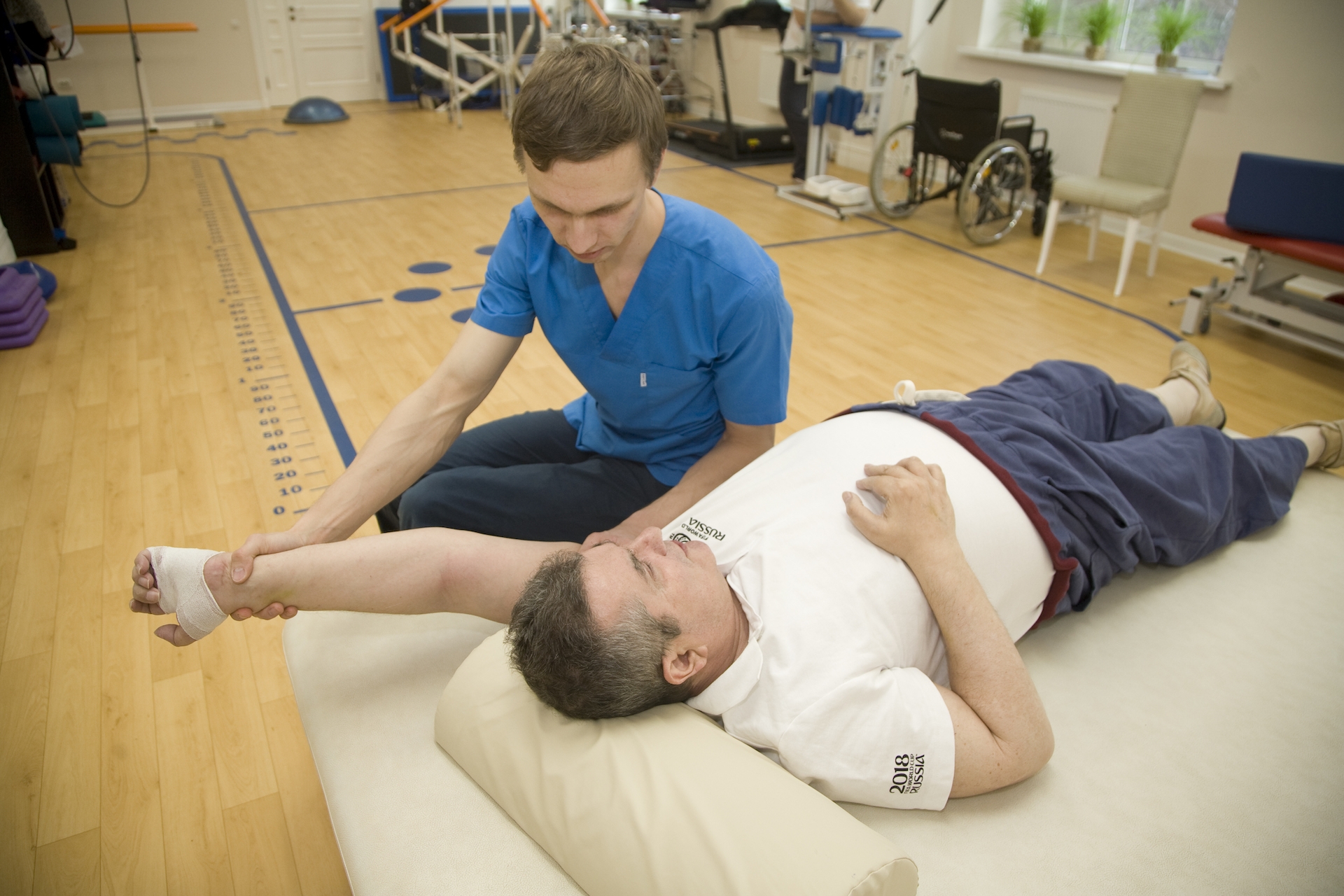 — Мы, образно говоря, помогаем вспомнить себя до болезни. И учим ходить, здороваться, писать и улыбаться так же, как человек делал это до заболевания.
— Мы, образно говоря, помогаем вспомнить себя до болезни. И учим ходить, здороваться, писать и улыбаться так же, как человек делал это до заболевания.
Цифра: 75 процентов и более в цене высокотехнологичного оборудования для нейрореабилитации больных после инсульта занимает программное обеспечение
Рядом с нашим работягой-роботом разрабатывал парализованную руку средних лет мужчина. Им оказался 42-летний предприниматель из Челябинской области Александр Коробцов. Строгие инструкции и неписаные правила, принятые в Центре неврологии, не предусматривают в таких случаях публичных интервью. Но Ульяна, жена Александра, вместе с которой он пришел на процедуру, да и он сам, когда мы представились, даже попросили специально упомянуть, что они без всякого блата попали в этот центр. Еще у себя дома в Магнитогорске нашли в Интернете адрес, списались, собрали необходимый пакет документов, прошли предварительный отбор на госпитализацию, потом посоветовались с друзьями, которые живут в Москве, и те согласились их на время приютить…
А мы тем временем двигаемся дальше и попадаем на получасовой ликбез к врачу-неврологу Александре Пойдашевой. В ее заведовании уже не роботы, а сплошь компьютеры, магнитные поля, 3D-модели и системы навигации по снимкам МРТ. Александра Георгиевна, как могла, растолковала гуманитариям, для чего используется и как работает метод ТМС — транскраниальной магнитной стимуляции.
В ее заведовании уже не роботы, а сплошь компьютеры, магнитные поля, 3D-модели и системы навигации по снимкам МРТ. Александра Георгиевна, как могла, растолковала гуманитариям, для чего используется и как работает метод ТМС — транскраниальной магнитной стимуляции.
— В его основе — стимуляция нейронов головного мозга переменным магнитным полем высокой индукции, — доктор Саша просит временно побыть испытуемым своего коллегу Романа Люкманова и надевает ему на голову плотную шапочку с электродами. — Переменное магнитное поле рождает электрическое, а уже оно возбуждает нейроны. При стимуляции нейронов моторной коры, то есть участка головного мозга, отвечающего за произвольные движения, возникает мышечное сокращение.
Александра Пойдашева «кликает» куда-то мышкой компьютера, прикладывает специальную магнитную катушку к голове и показывает, для убедительности, как дернулся один из пальцев на руке у Романа. Чтобы знать, куда именно «кликать», по снимкам МРТ конкретного человека с использованием уникальной навигационной системы (в этом и заключается ноу-хау) создается 3D-модель головного мозга конкретного испытуемого. И на ней становятся видны точки стимуляции.
И на ней становятся видны точки стимуляции.
По словам Пойдашевой, такая методика широко используется для предоперационного картирования опухолей головного мозга.
— Проще говоря, еще до операции мы можем сказать хирургу, где находятся зоны, отвечающие за движения в руках и ногах, при повреждении которых может развиться слабость в соответствующей мускулатуре.
Как и в случае с роботом Lokomat, почти все оборудование в кабинете-лаборатории доктора Пойдашевой импортное. В основном финское.
Компания «Нейрософт» из Иваново, пожалуй, единственная, кто делает что-то подобное в России. И даже в Бразилию пытаются продавать. Программное обеспечение — это основное в стоимости. В Научный центр неврологии такой комплект оборудования был поставлен в 2011 году, ПО еще не обновляли. Хотя, уверяли наши собеседники, уже есть стимуляторы нового поколения — дело не стоит на месте. Известно, что при университете в Хельсинки есть рабочая группа, которая создает более совершенную навигацию, в том числе для предоперационного картирования.
Сергей Семенов, с которым мы встретились в зале лечебной физкультуры, посетовал на ту же проблему. С его слов, практически все установленное оборудование в основном из Германии и Швейцарии. Пластичная, но очень тяжелая гиря, что он демонстрировал перед объективом моего коллеги, и та импортная. Рядом — имитатор лестницы с регулируемой высотой ступенек. Название — тренажер динамический «DST-8000».
Неужели у себя что-то подобное не можем сконструировать? В отношении наших аналогов Роман Люкманов высказался прямо:
— Есть, например, робот «СЛТ» — это как будто русский Lokomat. Но его вид столь недружелюбен, что к нему и здорового подпускать нельзя, не то что больного…
Как говорится, что есть, то есть. Из такого разговора, как из песни, слов не выкинешь.
В отделение нейрореабилитации и физиотерапии Научного центра неврологии, что в Москве на Волоколамском шоссе, мы напросились после того, как у нас, в «Российской газете», побывал директор этого центра член-корреспондент РАН Михаил Пирадов. «Хотите увидеть в действии новейшие медицинские технологии, когда инструментом врача становится не скальпель, но компьютер, а первым помощником — робот? Тогда приезжайте». И прямиком направил нас в отделение, которым руководит доктор медицинских наук, врач-невролог и нейрофизиолог Наталья Супонева.
«Хотите увидеть в действии новейшие медицинские технологии, когда инструментом врача становится не скальпель, но компьютер, а первым помощником — робот? Тогда приезжайте». И прямиком направил нас в отделение, которым руководит доктор медицинских наук, врач-невролог и нейрофизиолог Наталья Супонева.
Почему именно к вам, Наталья Александровна? Ведь Научный центр неврологии — это большое научное и клиническое учреждение, с несколькими отделениями, филиалами и богатой историей?
Наталья Супонева: Вы правы: у центра большой научно-исследовательский потенциал, со своей диагностической базой и клиникой. Кроме того, в составе нашего центра есть Институт мозга, где работали и работают опытнейшие сотрудники. Начинали еще с изучения мозга Ленина.
Они все у вас находятся?
Наталья Супонева: Это подразделение нашего центра в другом месте — на Воронцовом Поле. Там уникальный Музей мозга, где хранится, например, и мозг Сахарова.
Так почему же все-таки к вам?
Акцент: С помощью роботов и других устройств можно облегчить монотонную работу пациента над своим восстановлением
Наталья Супонева: Наверное, потому что реабилитация и нейрореабилитация — одно из самых перспективных сейчас направлений. Оно очень бурно развивается во всем мире и в нашей стране, в частности. Мы много сил вкладываем в образование своих сотрудников, в выведение на совершенно новый уровень той помощи и того спектра услуг, которые в рамках государственной программы должны оказываться нашим гражданам.
Оно очень бурно развивается во всем мире и в нашей стране, в частности. Мы много сил вкладываем в образование своих сотрудников, в выведение на совершенно новый уровень той помощи и того спектра услуг, которые в рамках государственной программы должны оказываться нашим гражданам.
Стоит, наверное, сказать и о том, что на базе нашего центра зародилась одна из первых школ нейрореабилитации. А мы традиции храним и развиваем.
Сейчас у нас замечательный коллектив — доктора молодые, очень образованные, стремящиеся не только добиться каких-то научных высот, но и чрезвычайно чутко относящиеся к своим пациентам. То есть это люди, которые по-настоящему желают развить новые технологии для того, чтобы помочь страдающим людям. Поэтому отделение, которое я возглавляю, является одним из самых перспективных в нашем центре.
Движение от традиционных, известных ранее методов — лечебного массажа, физиотерапии — к принципиально новым, с использованием компьютерной техники, как давно началось? Вы тут пионеры? Или у нас в стране есть более продвинутые центры?
Наталья Супонева: Мы, наверное, одни из самых продвинутых. А началось это перевооружение, пожалуй, с начала 2000-х, когда стали появляться первые высокотехнологичные устройства. Мы активно перенимали опыт из-за рубежа, где это было начато раньше, чем у нас. Уже в самом начале, осваивая эти методы пока только для практического использования, мы ощутили и комфорт от новой аппаратуры, и тот эффект, пользу, что она приносит пациентам.
А началось это перевооружение, пожалуй, с начала 2000-х, когда стали появляться первые высокотехнологичные устройства. Мы активно перенимали опыт из-за рубежа, где это было начато раньше, чем у нас. Уже в самом начале, осваивая эти методы пока только для практического использования, мы ощутили и комфорт от новой аппаратуры, и тот эффект, пользу, что она приносит пациентам.
Наша традиционная школа восcтановительного лечения никуда не делась. И, безусловно, остается очень важным звеном работа инструктора, врача непосредственно с больным.
Человеческое общение не может быть заменено роботом?
Наталья Супонева: Конечно. Но при всем том было доказано рядом исследований, что регулярное повторение одних и тех же движений, заданий дает больший эффект. И только с помощью различных устройств, роботов, машин и компьютерных технологий можно обеспечить эту монотонную и подчас не всегда интересную работу, которую совершает пациент над своим восстановлением. Очень важный аспект — это мотивация больного, который испытывает трудности и страдания, даже болезненные ощущения…
Поэтому присоединение различного рода обратной связи в виде компьютерных игр, мотивирующих на победу, в виде каких-то интересных пространственных изображений позволяет пациенту сохранить способность больше работать, больше заниматься и, соответственно, получать больший эффект.
Судя по тому, что видим, оборудование у вас почти сплошь импортное. Все ваши сотрудники осваивали его и проходили стажировку за границей?
Наталья Супонева: Многие.
Значит, как минимум должны знать английский и с компьютером быть на ты?
Наталья Супонева: С этим все в порядке. Но мы, принимая человека на работу, обращаем внимание: научный сотрудник, занимающийся развитием современных технологий, должен быть прежде всего врачом — иметь искреннее желание помочь больному человеку. Это один из залогов успеха.
А что касается международного сотрудничества, у нас активные контакты с Финляндией, Германией, Италией, США. Наш коллектив известен, и мы на хороших позициях.
Насколько я знаю, как минимум одна защищенная у вас диссертация напрямую связана с развитием такой техники.
Наталья Супонева: Да, мы заточены на клинический эффект, это наша цель. И мы, безусловно, изучаем эффективность уже созданного оборудования. Кроме того, активно работаем с опытными образцами техники, в том числе отечественных производителей. Тем самым помогаем инженерам, конструкторам усовершенствовать экзоскелеты и программы к ним, чтобы они стали более удобными в использовании и более эффективными. Это один из наших аспектов научно-исследовательской работы.
Кроме того, активно работаем с опытными образцами техники, в том числе отечественных производителей. Тем самым помогаем инженерам, конструкторам усовершенствовать экзоскелеты и программы к ним, чтобы они стали более удобными в использовании и более эффективными. Это один из наших аспектов научно-исследовательской работы.
Крайне важный момент — безопасность. Мы обязаны думать не только об эффективности, но и о безопасности новых методик, применяемых для реабилитации. Придаем этому повышенное внимание.
от первого лица
Михаил Пирадов, директор Научного центра неврологии, член-корреспондент РАН:
— С момента основания Научного центра неврологии пристальное внимание сотрудников направлено на изучение механизмов развития, диагностики, лечения и реабилитации инсульта. Как показывает статистика, в Москве он случается каждые 5 минут. Залог успешного лечения инсульта — оказать пациенту квалифицированную медицинскую помощь в рамках так называемого «терапевтического окна», это первые четыре часа после случившегося. И, конечно, должная реабилитация в последующий период.
И, конечно, должная реабилитация в последующий период.
В нашем центре доступны самые передовые технологии, позволяющие существенно ускорить реабилитацию пациентов и значительно улучшить качество их жизни. Например, благодаря роботизированным методам нейрореабилитации мы в 75 процентах случаев можем улучшить восстановление двигательных функций парализованной руки в раннем восстановительном периоде после инсульта. Благодаря методам стереотаксической нейрохирургии можно, например, избавить от тремора пациентов с болезнью Паркинсона и ряда других заболеваний.
Мы стремимся распространять наши знания и обмениваться опытом с коллегами. В прошлом году с участием представителей нашего центра организовано более 10 мероприятий в разных регионах страны. Кроме того, проводим скрининг состояния сосудов головного мозга для работников крупных предприятий России.
Среди задач на ближайшую перспективу — персонифицированная неврология: разработка новых молекулярных и клеточных технологий, направленных на замещение утраченных функций мозга, защиту когнитивного здоровья нации и создание прототипов искусственного интеллекта.
справка
Семь задач Научного центра неврологии в области реабилитации
Клинические исследования интерфейсов мозг-компьютер в реабилитации пациентов с инсультом и парезом в руке.
Исследование клинической эффективности различных видов биологической обратной связи.
Изучение клинической эффективности инновационных роботизированных систем для восстановления двигательных функций после инсульта и травм головного мозга.
Клинические исследования эффективности неинвазивной стимуляции мозга при различных заболеваниях нервной системы.
Картирование мозга (brain mapping) в норме и при патологии.
Изучение влияния магнитных и электрических полей на головной мозг.
Изучение нейрофизиологических основ кодирования, распределения и передачи информации в нервной системе человека.
Весь фоторепортаж Сергея Куксина из Отделения нейрореабилитации и физиотерапии Научного центра неврологии — на сайте www.rg.ru.
Основные особенности реабилитации после инсульта в пожилом возрасте
Существенное влияние на степень восстановления функций организма у пожилого человека, после перенесённого инсульта, имеет не только количество и расположение поражённых тканей мозга, но также своевременность и адекватность реабилитационных мероприятий. На основе анализа большого количества практических случаев установлено, что восстановление различных функций максимально эффективно в первые шесть месяцев, после перенесённого инсульта. Однако, конкретные сроки необходимые для восстановления, а также степень возможного восстановления всегда зависят от индивидуальных особенностей в каждом случае и могут длиться от года до двух лет.
Независимо от возраста человека перенёсшего инсульт, можно выделить основные принципы реабилитации:
- Раннее (от 2-х до 4-х недель) начало реабилитации.
- Комплексность, мультидисциплинарность и адекватность мероприятий по реабилитации.
- Систематичность и достаточная продолжительность срока реабилитационных мероприятий.

- Осознанное активное участие в реабилитации самого человека перенёсшего инсульт, а также его родственников или близких людей.
С возрастом вероятность возникновения инсульта значительно увеличивается. Этому способствуют, как причины связанные с естественными возрастными изменениями в организме, так и различные сопутствующие, в том числе хронические заболевания.
При разработке и проведении программ по восстановлению после перенесённого инсульта необходимо учитывать свойственные пожилому возрасту особенности:
- Различные имеющиеся заболевания сердечно-сосудистой системы. Наличие стенокардии, артериальная гипертония, недостаточность кровообращения и другие сердечно-сосудистые проблемы значительно затрудняют двигательную реабилитацию, что ведёт к медленному восстановлению активных движений. Прежде всего, необходим постоянный мониторинг артериального давления и частоты пульса, чтобы принимать соответствующие меры для поддержания стабильного состояния пожилого человека.

- Дыхательная система может быть нарушена как из-за поражения центральной регуляции ритма дыхательных движений, так и в результате застойных явлений в результате вынужденной неподвижности. Чтобы избежать столь часто возникающей в период после инсульта пневмонии, следует, как можно раньше проводить дыхательную гимнастику.
- Имеющиеся заболевания опорно-двигательного аппарата, которые могут препятствовать восстановлению двигательных функций организма. Это, прежде всего, остеопороз, а также заболевания суставов и патологические переломы костей. Также значение для восстановления двигательных функций имеет снижение мышечной массы и мышечной силы, часто распространённое в пожилом возрасте.
- Проблемы, связанные с нарушениями пищеварительной и выделительной системой. В рацион пожилого человека после инсульта рекомендуется включать продукты с высоким содержанием белков, углеводов, аминокислот и витаминов, количество жира при этом следует ограничивать. После приема пищи пожилой человек должен находиться в сидячем или полу сидячем положении не менее получаса.
 Следует внимательно следить за регулярным опорожнением кишечника и мочеиспусканием; в случае проблем или задержек в выделительных процессах нужно определить причину и начать соответствующее лечение.
Следует внимательно следить за регулярным опорожнением кишечника и мочеиспусканием; в случае проблем или задержек в выделительных процессах нужно определить причину и начать соответствующее лечение. - Нарушения органов чувств у пожилого человека, снижения зрения и слуха, что затрудняет ориентацию и движение в пространстве. Для эффективной реабилитации после инсульта необходимо проводить адекватное лечение имеющихся нарушений органов чувств.
- Снижение с возрастом когнитивных функций: оперативной памяти, внимания, скорости мыслительных процессов. В программах по восстановлению после инсульта достаточное место должно быть уделено занятиям по развитию мелкой моторики, которая непосредственно связана с когнитивными функциями человека.
- Психологические и эмоциональные проблемы характерные для пожилого возраста: одиночество, социальная изолированность, апатия, возможность развития депрессии. Все эти негативные факторы способны значительно затруднить, а то и вовсе свести на нет все усилия по реабилитации после инсульта.
 Для восстановления после инсульта особенно важно осознанное вовлечение человека перенёсшего инсульт в процесс реабилитации. Только положительный настрой самого человека перенёсшего инсульт на получение пользы от проводимых мероприятий по реабилитации позволяет добиваться наибольшего эффекта.
Для восстановления после инсульта особенно важно осознанное вовлечение человека перенёсшего инсульт в процесс реабилитации. Только положительный настрой самого человека перенёсшего инсульт на получение пользы от проводимых мероприятий по реабилитации позволяет добиваться наибольшего эффекта.
Реабилитация после инсульта | Реабилитационный центр Медскан в Москве
Ювелирную работу по восстановлению пациентов после инсульта в Центре «Медскан» ведет мультидисциплинарная команда высококлассных специалистов. Наша лаборатория по нейрофизиологии и биомеханике позволяет реализовывать программы реабилитации, индивидуально подобранные для каждого случая.
Инсульт – клинический синдром, развивающийся из-за острого нарушения мозгового кровообращения. Он характеризуется очаговыми неврологическими и/или общемозговыми расстройствами, которые сохраняются не менее 24 часов или приводят к смерти больного в это время или более ранние сроки.
Сегодня инсульт – основная причина длительной инвалидизации у взрослых. По разным оценкам от 80 до 86% выживших больных ограничены в возможностях, чаще всего – двигательных. Это одно из последствий ОНМК, острого нарушения мозгового кровообращения. По официальной статистике в течение 6 месяцев после инсульта 37% пациентов падают хотя бы раз. В 8% случаев такие падения приводят к переломам костей. Как следствие человек может лишиться независимости в повседневной жизни. Возникает высокий риск социальной изоляции пациента: из-за страха повторных падений человек просто боится выходить из дома.
По разным оценкам от 80 до 86% выживших больных ограничены в возможностях, чаще всего – двигательных. Это одно из последствий ОНМК, острого нарушения мозгового кровообращения. По официальной статистике в течение 6 месяцев после инсульта 37% пациентов падают хотя бы раз. В 8% случаев такие падения приводят к переломам костей. Как следствие человек может лишиться независимости в повседневной жизни. Возникает высокий риск социальной изоляции пациента: из-за страха повторных падений человек просто боится выходить из дома.
Поэтому одна из основных задач реабилитации больных после инсульта в Центре «Медскан» – восстановление двигательных функций, которые в наибольшей степени важны для социальной независимости и трудоспособности человека.
Комплексная реабилитация в Центре «Медскан» позволяет решать следующие задачи:
- повысить навыки передвижения за счет увеличения силы и подвижности мышц, прежде всего, ног;
- профилактировать падения и тренировать стояние;
- снизить спастичность мышц и бороться с контрактурами суставов;
- уменьшить отечность;
- снизить болевой синдром;
- улучшить мелкую моторику рук;
- вернуть речь.
В Центре Медскан полноценное восстановление после инсульта осуществляет мультидисциплинарная бригада врачей: невролог, нейрофизиолог, травматолог-ортопед, терапевт-кардиолог, врач ЛФК, психотерапевт.
Восстановление двигательной функции после повреждения ЦНС: есть ли потенциал, выходящий за рамки спонтанного восстановления? | Мозговые коммуникации
Аннотация
Что определяет эффективность подходов нейрореабилитации к исходу функции у субъектов с инсультом или спинным мозгом? Многие исследования утверждают, что улучшение функции основано на интенсивности тренировки, в то время как некоторые фактические исследования указывают на отсутствие дополнительного улучшения функции от более интенсивной тренировки после инсульта.Исходные факторы, по-видимому, определяют исход, такие как повреждение определенных трактов при инсульте и уровень поражения у пациентов с травмой спинного мозга, в то время как улучшение функции, достигаемое интенсивными тренировками, мало по сравнению со спонтанным восстановлением. Утверждается, что индивидуальная способность к выздоровлению существует в зависимости от таких факторов. Эта способность может быть использована путем повторяющегося выполнения функциональных движений (поддерживаемых по мере необходимости), независимо от интенсивности и применяемой технологии.Пожилым людям трудно преобразовать восстановление двигательного дефицита в функцию. Альтернативные, нетренировочные подходы к восстановлению двигательной функции, такие как эпидуральная или глубокая стимуляция мозга, а также восстановление ЦНС, все еще находятся на ранней клинической или трансляционной стадии.
Абстрактное графическое изображение
Абстрактное графическое изображение
Вопрос: Каким образом нейрореабилитация влияет на восстановление функций?
Число пациентов, страдающих поражением ЦНС, чаще всего вследствие инсульта, постоянно увеличивается из-за старения населения.Большинство этих пациентов проходят процедуры нейрореабилитации. Стандартного лечения двигательной недостаточности после повреждения ЦНС не существует, т. Е. Применяемые процедуры различаются между странами и центрами в пределах одной страны. Эффективность или превосходство любого подхода к реабилитации вряд ли можно продемонстрировать на прочной научной основе, поскольку этические вопросы не позволяют проводить сравнение между леченными и нелеченными пациентами, а надежные исследования, в которых сравниваются различные подходы или демонстрируются лучшие доказательства для вмешательства, встречаются редко. 1
Считается, что большинство подходов к реабилитации достигают улучшения функций за счет использования нейропластичности. 1–3 Предполагается, что на успех этой эксплуатации влияет ряд факторов, таких как возраст или тяжесть повреждения ЦНС 4 или, например, по сложности задачи. 5 В нейрореабилитации пациентов с инсультом или травмой спинного мозга идея использования нейропластичности обычно реализуется в реабилитации путем повторяющегося выполнения функциональных движений поврежденной конечности (ей), требующих синергетической активации мышц, 6 i.е. например, тянущие и захватывающие движения для верхних конечностей и шагающие движения для нижних конечностей. Тренировку можно дополнить пассивным растяжением мышц при наличии деформирующего спастического пареза. 7 , 8 У пациентов с инсультом и травмой спинного мозга при таком подходе обычно достигается некоторое восстановление функции, даже у пожилых людей, 9 с максимумом в течение примерно трех-четырех месяцев после повреждения ЦНС. 10 Однако результат функции зависит не только от тренировки, но и от других факторов, таких как инфекции, которые, как известно, препятствуют восстановлению функции. 11
Было предложено более интенсивная тренировка движений, чтобы привести к лучшему результату функции. 12 , 13 Как следствие, технология вошла в сферу нейрореабилитации. Были разработаны роботизированные устройства, которые позволили увеличить время обучения в сочетании с отслеживанием изменений в функциях. 12 , 14 За последние 25 лет на рынке появилось большое количество таких устройств с целью достижения большего эффекта реабилитации за счет оптимального использования нейропластичности за счет большего количества повторений движений. 14 , 15
Вопрос, лежащий в основе этого обзора, заключается в том, можно ли получить дополнительный, существенный прирост функции с помощью высокоинтенсивной тренировки по сравнению с восстановлением функции, достигаемой с помощью стандартной тренировки. Этот аспект связан с вопросом о том, насколько улучшение функции происходит в значительной степени спонтанно или, наоборот, из-за определенных подходов к реабилитации. Термин «спонтанный» в данном контексте рассматривается как восстановление функции после регулярного, (т.е. несколько раз в день), повторяющееся выполнение движений верхних / нижних конечностей, используемых в повседневной жизни, при необходимости личной / технической поддержки. Без выполнения таких движений, т.е. когда конечности остаются обездвиженными из-за пареза, спонтанного восстановления не ожидается. Вместо этого будут развиваться контрактуры мышц / суставов — аналогично состояниям с иммобилизацией конечностей по причинам, не связанным с повреждением ЦНС, например переломы костей. Предполагается, что возможность функционального восстановления заключается в сочетании разрешения неврапраксии и нейропластичности.
На основе фактических научных достижений и дискуссий в этой области, 14 , 16 , 17 утверждается, что большая часть функционального восстановления происходит до сих пор «спонтанно», так как определяется использованием индивидуально ограниченной емкости для восстановления. Кроме того, предполагается, что успех этой эксплуатации не зависит от конкретных реабилитационных вмешательств. 16 , 17
Факторы, определяющие результат функции
После повреждения головного мозга , включающего соединения пирамидных трактов с руками и пальцами, двигательный дефицит вряд ли можно компенсировать активацией других неповрежденных трактов / областей мозга. 18–20 В результате происходит довольно ограниченное восстановление (10–20%) парализованных пальцев. 21 , 22 Было высказано предположение, что незначительные признаки выздоровления возникают спонтанно (например, разрешение невропраксии?), То есть без доказательств тренировочного эффекта. 23 Напротив, после повреждения других областей мозга можно ожидать более благоприятного восстановления функции проксимальных мышц рук и ног (60–80%; Таблица 1). 18–20 Это достигается с помощью стандартной терапии, т.е.е. повторяющееся выполнение функциональных движений в течение ограниченного времени (например, 30–50 минут в день), которые поддерживаются по мере необходимости. 24
Таблица 1Основные аспекты нейрореабилитации и исходы верхних конечностей после инсульта или шейного отдела позвоночника
| . | Расположение . | Типовой курс восстановления . | Гол . | Реабилитационный подход . |
|---|---|---|---|---|
| Инсульт | Поврежденный кортикоспинальный тракт (CST) | Небольшое восстановление, особенно хроническое нарушение разгибания кисти / пальца | Prox. активация мышц руки; избежание мышечных контрактур; использование поврежденной конечности для функции поддержки / удержания | Prox. укрепление мышц рук; повторяющиеся пассивные движения конечностей; тренировка компенсаторных стратегий |
| Интактный CST | Спонтанное восстановление ~ 70% первоначального повреждения руки / кисти | Функция руки и простого захвата; одно- / бимануальные функции ADL | Функциональный досягаемость / захват и бимануальные (совместные) движения руками; укрепление разгибателей запястья / пальцев; простая тренировка движений с переходом в ADL; ограниченные дозозависимые тренировочные эффекты | |
| SCI | Уровень поражения C6 / 7 | Спазматический тонус сгибателей предплечья, угрожающий развитию тенодезного захвата | Тенодезный захват; бимануальный захват |
| . | Расположение . | Типовой курс восстановления . | Гол . | Реабилитационный подход . |
|---|---|---|---|---|
| Инсульт | Поврежденный кортикоспинальный тракт (CST) | Небольшое восстановление, особенно хроническое нарушение разгибания кисти / пальца | Prox. активация мышц руки; избежание мышечных контрактур; использование поврежденной конечности для функции поддержки / удержания | Prox.укрепление мышц рук; повторяющиеся пассивные движения конечностей; тренировка компенсаторных стратегий |
| Интактный CST | Спонтанное восстановление ~ 70% первоначального повреждения руки / кисти | Функция руки и простого захвата; одно- / бимануальные функции ADL | Функциональный досягаемость / захват и бимануальные (совместные) движения руками; укрепление разгибателей запястья / пальцев; простая тренировка движений с переходом в ADL; ограниченные дозозависимые тренировочные эффекты | |
| SCI | Уровень поражения C6 / 7 | Спазматический тонус сгибателей предплечья, угрожающий развитию тенодезного захвата | Тенодезный захват; бимануальный захват |
Основные аспекты нейрореабилитации и исходы верхних конечностей после инсульта или шейного отдела позвоночника
| . | Расположение . | Типовой курс восстановления . | Гол . | Реабилитационный подход . |
|---|---|---|---|---|
| Инсульт | Поврежденный кортикоспинальный тракт (CST) | Небольшое восстановление, особенно хроническое нарушение разгибания кисти / пальца | Prox. активация мышц руки; избежание мышечных контрактур; использование поврежденной конечности для функции поддержки / удержания | Prox.укрепление мышц рук; повторяющиеся пассивные движения конечностей; тренировка компенсаторных стратегий |
| Интактный CST | Спонтанное восстановление ~ 70% первоначального повреждения руки / кисти | Функция руки и простого захвата; одно- / бимануальные функции ADL | Функциональный досягаемость / захват и бимануальные (совместные) движения руками; укрепление разгибателей запястья / пальцев; простая тренировка движений с переходом в ADL; ограниченные дозозависимые тренировочные эффекты | |
| SCI | Уровень поражения C6 / 7 | Спазматический тонус сгибателей предплечья, угрожающий развитию тенодезного захвата | Тенодезный захват; бимануальный захват |
| . | Расположение . | Типовой курс восстановления . | Гол . | Реабилитационный подход . |
|---|---|---|---|---|
| Инсульт | Поврежденный кортикоспинальный тракт (CST) | Небольшое восстановление, особенно хроническое нарушение разгибания кисти / пальца | Prox. активация мышц руки; избежание мышечных контрактур; использование поврежденной конечности для функции поддержки / удержания | Prox.укрепление мышц рук; повторяющиеся пассивные движения конечностей; тренировка компенсаторных стратегий |
| Интактный CST | Спонтанное восстановление ~ 70% первоначального повреждения руки / кисти | Функция руки и простого захвата; одно- / бимануальные функции ADL | Функциональный досягаемость / захват и бимануальные (совместные) движения руками; укрепление разгибателей запястья / пальцев; простая тренировка движений с переходом в ADL; ограниченные дозозависимые тренировочные эффекты | |
| SCI | Уровень поражения C6 / 7 | Спазматический тонус сгибателей предплечья, угрожающий развитию тенодезного захвата | Тенодезный захват; бимануальный захват |
После повреждения спинного мозга улучшение функции верхних конечностей зависит от уровня и степени поражения. 10 При травмах шейного отдела спинного мозга возникает комбинированное повреждение центральных (спинномозговые пути) и периферических нервных структур (мотонейронов и корешков мышц рук, кистей и пальцев). Это приводит к парезу руки / кисти / пальца, связанному со смесью спастического и вялого мышечного тонуса 25 (Таблица 1). Поражение периферической нервной системы может составлять до 50% пареза. 26 Эта часть нервного повреждения имеет мало возможностей для восстановления. После завершения сенсомоторной травмы спинного мозга восстановление функции маловероятно. 24
Возраст пациентов мало влияет на восстановление неврологического дефицита у пациентов после инсульта 27 , 28 и SCI 29 субъектов, т.е. . Однако после травмы спинного мозга молодые люди по сравнению с пожилыми людьми могут лучше преобразовать восстановление дефицита двигательной системы в функции, необходимые в повседневной жизни. 29
Сделан вывод, что существует врожденная индивидуальная способность восстановления функции после инсульта или травмы спинного мозга, которая зависит от таких факторов, как локализация и тяжесть повреждения ЦНС.Эту способность можно определить на ранней стадии после повреждения ЦНС с помощью клинических, электрофизиологических 24 и визуализационных 19 исследований. Эти меры также могут использоваться в качестве прогностических факторов и, следовательно, для выбора подходящих реабилитационных процедур на раннем этапе после повреждения ЦНС.
Компенсаторная роль спастического мышечного тонуса
После инсульта / неполной травмы спинного мозга потеря надспинального возбуждения приводит к парезу и, как следствие, снижению подвижности.По мере развития спастического мышечного тонуса этот дефицит частично компенсируется (рис. 1). Функциональные движения, такие как шагание, могут выполняться на более низком уровне организации. 30 Таким образом, большинство субъектов, перенесших инсульт, восстанавливают функцию ходьбы, используя спастически-паретическую ногу, более или менее похожую на палку: поддержка тела в фазе опоры и обход ноги во время замаха (из-за уменьшения сгибания колена). Обычное отталкивание ноги в конце фазы стойки теряется. Как следствие, ограниченное улучшение способности ходить, достигнутое в ходе реабилитации после инсульта, связано с небольшим изменением биомеханических характеристик и характеристик активации мышц спастически-паретичной ноги. 24 , 31 Таким образом, улучшение мобильности происходит скорее за счет адаптационных изменений, чем за счет восстановления «нормальной» функции шагания.
Рисунок 1
Механизмы, вызывающие спастические движения. Поражение ЦНС, влияющее на двигательное поведение, приводит к потере надспинального возбуждения. Как следствие, происходят изменения проприоцептивной обратной связи, то есть изменения возбудимости спинномозговых рефлексов и мышечной функции, что отражается в изменении механических свойств мышц.Сочетание всех последствий первичного поражения приводит к различным проявлениям клинической спастичности и расстройства спастических движений. Изменено после Дитца и Синкьяера. 30
Рисунок 1
Механизмы, приводящие к выполнению спастических движений. Поражение ЦНС, влияющее на двигательное поведение, приводит к потере надспинального возбуждения. Как следствие, происходят изменения проприоцептивной обратной связи, то есть изменения возбудимости спинномозговых рефлексов и мышечной функции, что отражается в изменении механических свойств мышц.Сочетание всех последствий первичного поражения приводит к различным проявлениям клинической спастичности и расстройства спастических движений. Изменено после Дитца и Синкьяера. 30
Пациентам с шейной травмой спинного мозга (т. Е. C6 / 7) требуется спастический мышечный тонус для выполнения простого захвата (так называемый тенодезный захват). Кроме того, спастические проксимальные мышцы руки могут обеспечивать некоторую пассивную гравитационную поддержку для переноса объекта из одного места в другое (см. Таблицу 1).
Более интенсивное обучение: больше возможностей?
Несколько исследований показывают, что более интенсивными тренировками можно добиться дополнительного улучшения функций верхних и нижних конечностей.Об этом эффекте сообщалось для пациентов, перенесших инсульт, 1–3 , 32–35 , а также для пациентов с подострым 36 и хроническим 37 SCI.
Однако ни в одном из этих исследований дополнительный прирост функции не был связан с восстановлением функции, достигнутым при стандартной тренировке, или со спонтанным восстановлением функции. Фактически, для функции нижних конечностей улучшение результата, достигаемое более интенсивной тренировкой, невелико (или преходяще; ср.инжир. 3 из Hubli et al. 38 ) по отношению к приросту функции, достигаемому стандартным обучением у пациентов после инсульта 38 и SCI 36 . Что касается функции верхних конечностей у пациентов с хроническим постинсультным инсультом, нет данных о влиянии интенсивности тренировки на функциональное восстановление «доза-ответ». 39
Может ли более интенсивная тренировка опорно-двигательного аппарата улучшить функцию шага после инсульта? В большой группе (200 взрослых) субъектов подострого постинсульта с умеренными и тяжелыми нарушениями тренировка на беговой дорожке с опорой на вес тела не превосходила сеансов релаксации (такой же продолжительности и в дополнение к стандартной терапии) в отношении скорости ходьбы и повседневной активности. живой (ADL). 16 Соответственно, у субъектов с неполной травмой спинного мозга удвоение дневной тренировки локомоторного движения оказало лишь небольшое влияние на способность ходить. 36
Альтернативные нетренировочные подходы для восстановления двигательной функции
Ремонт SCI
Какие клетки лучше всего подходят для лечения повреждений головного или спинного мозга на основе трансплантации и какой вид повреждения ЦНС следует лечить в первую очередь? Эти вопросы остаются предметом постоянного расследования. 40 Применение шванновских клеток, 41 стволовых клеток 42 или аутотрансплантация обонятельных обволакивающих клеток: 43 Известно, что все эти типы клеток являются допустимыми для роста поврежденных аксонов спинного или надспинального тракта на животных моделях поражения ЦНС.
В случае трансплантации обонятельных клеток у субъектов с травмой спинного мозга не было обнаружено ни отрицательных, ни положительных эффектов у лиц с полным двигательным повреждением спинного мозга. 43 То же самое верно для трансплантации эмбриональных стволовых клеток в Китае 44 и для применения человеческих нейральных стволовых клеток в шейном отделе позвоночника 45 , которые оба не показали признаков восстановления моторики. Помимо репарации на основе клеток, в экспериментах на животных было показано, что применение Nogo-антител эффективно для репарации SCI. 46 , 47 Лечение антителами Nogo в настоящее время применяется у пациентов, страдающих шейной травмой спинного мозга, во второй фазе исследования.Если это лечение может быть успешно применено при травме спинного мозга у человека, его можно перевести в более сложное состояние повреждения головного мозга.
Лечение шейного отдела позвоночника направлено на улучшение функции руки / кисти. Проблема в том, что на шейном уровне существует комбинированное поражение центральных и периферических нервных структур. Восстановление грудного отдела спинного мозга снова будет функционально менее важным, поскольку в лучшем случае может быть достигнута элементарная ступенчатая функция.
Эпидуральная стимуляция спинного мозга и глубокая стимуляция головного мозга
Эпидуральная стимуляция спинных (грудо-поясничных) нейронных сетей облегчает выполнение шаговых движений у пациентов с травмой спинного мозга с сохраненными нисходящими связями.В сочетании со спастическим мышечным тонусом этот подход к стимуляции улучшает способность ходить. 48 Успех этого подхода ограничен, поскольку только элементарные шаги могут быть выполнены с опорой на костыли для поддержания равновесия тела. Это означает, что при таком подходе у субъекта возникают проблемы с переносом предмета из одного места в другое. Как следствие, для выполнения действий ADL путешествие на инвалидной коляске является более эффективным.
Также было показано, что глубокая стимуляция мозга улучшает двигательную функцию у грызунов с повреждением ЦНС. 49 Этот подход скоро будет переведен на людей.
Выводы
Вопрос, лежащий в основе этого обзора, заключается в том, насколько более интенсивное обучение приводит к дополнительному увеличению функциональности по сравнению со стандартным обучением. Ответ заключается в том, что с помощью интенсивных тренировок можно добиться дополнительного восстановления функций. Однако это усиление функции невелико, преходяще или даже может отсутствовать в связи со «спонтанным» восстановлением функции.Сделан вывод, что существует индивидуально ограниченная способность восстановления функции после инсульта или травмы спинного мозга, которая зависит от внутренних факторов, таких как локализация и тяжесть повреждения ЦНС.
Улучшение функции в пределах этой способности зависит от соответствующей активации пулов мотонейронов синергических мышц конечностей в условиях физиологического движения. Это означает, что использование этой способности основано на стандартном подходе к реабилитации, то есть на повторяющемся выполнении функциональных движений (при поддержке терапевта или устройства, если это необходимо).На этой основе восстановление функции достигается независимо от применяемого реабилитационного вмешательства.
Восстановление двигательной недостаточности после инсульта или травмы спинного мозга происходит независимо от возраста. Однако у субъектов с травмой спинного мозга прирост мощности двигательной системы лучше переводится в функцию у молодых, чем у пожилых субъектов.
Принимая во внимание эти аспекты, неотъемлемая часть реабилитации должна быть направлена на компенсацию остающегося двигательного дефицита усовершенствованными вспомогательными устройствами, которые позволяют вести самостоятельную жизнь, насколько это возможно для отдельного пациента.
Альтернативные дополнительные подходы к обучению, такие как эпидуральная анестезия или глубокая стимуляция мозга, могут в некоторой степени улучшить двигательную функцию, например улучшить способность выполнять шаговые движения у субъектов, страдающих повреждением ЦНС. Восстановление поврежденного спинного / головного мозга в настоящее время еще не доступно.
Этот обзор восстановления двигательной функции после повреждения ЦНС должен основываться на довольно ограниченных научных данных, имеющихся в области нейрореабилитации. Для окончательной оценки величины эффекта от более интенсивного подхода к обучению необходимы более крупномасштабные испытания, включающие определенные группы пациентов.
Новых данных в статье не генерировалось.
Стратегия поиска и критерии выбора
Было процитированооригинальных исследовательских работ, включающих достаточное количество пациентов, и обзоры, посвященные оригинальным ключевым исследованиям по влиянию реабилитации на исход двигательной функции у субъектов с инсультом и повреждением спинного мозга, опубликованные в высококачественных журналах за последние 20 лет.
Конкурирующие интересы
Авторы сообщают об отсутствии конкурирующих интересов.
Список литературы
1Хан
F
,Amatya
B
,Galea
MP
,Gonzenbach
R
,Kesselring
J.
Прикладная нейропластика:
Дж. Neurol
.2017
;264
(3
):603
—615
,2Cramer
SC
,Sur
M
,Dobkin
BH
и др.Использование нейропластичности для клинического применения
.Мозг
.2011
;134
(Pt 6
):1591
—1609
.3Dancause
N
,Nudo
RJ.
Формовочная пластичность для ускорения восстановления после травм
.Prog Brain Res
.2011
;192
:273
—295
.4Stein
DG
,Hoffman
SW.
Концепции пластичности ЦНС в контексте повреждения и восстановления головного мозга
.J Head Trauma Rehabil
.2003
;18
(4
):317
—341
.5Кэри
JR
,Bhatt
E
,Nagpal
A.
Задача, повышенная сложностью Neuroplastic.
Exerc Sport Sci Ред.
.2005
;33
(1
):24
—31
.6Dietz
V
,Ward
N.
Оксфордский учебник нейрореабилитации
, 2-е изд.Оксфорд
:Oxford University Press
;2020
,7Gracies
JM
,Brashear
A
,Jech
R
и др.Безопасность и эффективность абоботулинумтоксина А при гемипарезе у взрослых со спастичностью верхних конечностей после инсульта или черепно-мозговой травмы: двойное слепое рандомизированное контролируемое исследование
.Ланцет Нейрол
.2015
;14
(10
):992
—1001
,8Lorentzen
J
,Pradines
M
,Gracies
JM
J. О «спастической дистонии» Денни-Брауна — что это и что ее вызывает?Клин нейрофизиол
.2018
;129
(1
):89
—94
.9Jakob
W
,Wirz
M
,van Hedel
HJ
,Dietz
V.
Трудности пожилых пациентов с ТСМ переводить восстановление моторики — ежедневную функцию тела жилая деятельность
.J Нейротравма
.2009
;26
(11
):2037
—2044
.10Curt
A
,Van Hedel
HJ
,Klaus
D
,Dietz4
Восстановление после травмы спинного мозга: значение компенсации, нейропластичность и восстановление
.J Нейротравма
.2008
;25
(6
):677
—685
.11Failli
V
,Kopp
MA
,Gericke
C
и др.Функциональное неврологическое восстановление после травмы спинного мозга нарушено у пациентов с инфекциями
.Мозг
.2012
;135
(11
):3238
—3250
.12Чанг
WH
,Ким
YH.
Роботизированная терапия при реабилитации после инсульта
.J Ход
.2013
;15
(3
):174
—181
.13Kwakkel
G
,Wagenaar
RC
,Kollen
BJ
horst.
Прогнозирование инвалидности при инсульте — критический обзор литературы
.Возраст
.1996
;25
(6
):479
—489
,14Гассерт
R
,Dietz
V.
Реабилитационные роботы для лечения сенсомоторной недостаточности: перспектива
.J Neuroeng Rehabil
.2018
;15
(1
):46
.15Reinkensmeyer
D
,Dietz
V.
Технология нейрореабилитации
. 2-е изд.Нью-Йорк
:Springer Intl Publishing, Лондон
;2016
.16Ступица
AH
,Rackoll
T
,Grittner
U
и др.Физическая подготовка пациентов с подострым инсультом (PHYS-STROKE): многоцентровое рандомизированное контролируемое слепое исследование по конечным точкам
.БМД
.2019
;366
:l5101
-17Stinear
CM
,Lang
CE
,Zeiler
S
,Byblow
WD.
Достижения и проблемы реабилитации после инсульта
.Ланцет Нейрол
.2020
;19
(4
):348
—360
. 18Kwakkel
G
,Kollen
B
,Lindeman
E.
Понимание модели функционального восстановления после инсульта: факты и теории
.Рестор Neurol Neurosci
.2004
;22
(3-5
):281
—299
,19Прабхакаран
S
,Zarahn
E
,Riley
C
и др.Индивидуальная изменчивость способности к восстановлению моторики после ишемического инсульта
.Neurorehabil Neural Repair
.2008
;22
(1
):64
—71
.20Винтерс
C
,van Wegen
EE
,Daffertshofer
A
k4000000000Kw Обобщаемость модели пропорционального восстановления для верхней конечности после ишемического инсульта
.Neurorehabil Neural Repair
.2015
;29
(7
):614
—622
.21Rowe
JB
,Chan
V
,Ingemanson
ML
,Cramer
SC
,Wolbrecht
ET 9000ensme
.
Роботизированная помощь для тренировки движения пальцев с использованием модели Хебба: рандомизированное контролируемое испытание
.Neurorehabil Neural Repair
.2017
;31
(8
):769
—780
.22Waddell
KJ
,Strube
MJ
,Bailey
RR
и др.Улучшает ли специализированная тренировка работоспособность верхних конечностей в повседневной жизни после инсульта?
Neurorehabil Neural Repair
.2017
;31
(3
):290
—300
.23Byblow
WD
,Stinear
CM
,Barber
PA
,MA0004 MA0005 Petoe4
SJ.
Пропорциональное восстановление после инсульта зависит от кортикомоторной целостности
.Энн Нейрол
.2015
;78
(6
):848
—859
.24Dietz
V
,Fouad
K.
Восстановление сенсомоторных функций после травмы спинного мозга
.Мозг
.2014
;137
(Pt 3
):654
—667
0,25Dietz
V
,Curt
A.
Неврологические аспекты восстановления спинного мозга: перспективы и проблемы
.Ланцет Нейрол
.2006
;5
(8
):688
—694
.26Curt
A
,Dietz
V.
Нейрографическая оценка интрамедуллярных двигательных мозговых повреждений спинного мозга при поражении шейного отдела позвоночника функция
.Спинной мозг
.1996
;34
(6
):326
—332
.27Bagg
S
,Pombo
AP
,Hopman
W.
Влияние возраста на функциональные результаты после реабилитации после инсульта
.Инсульт
.2002
;33
(1
):179
—185
,28Lang
CE
,Macdonald
JR
,Reisman
DS
и др.Наблюдение за объемами двигательной практики при реабилитации после инсульта
.Arch Phys Med Rehabil
.2009
;90
(10
):1692
—1698
,29Wirz
M
,Dietz
V.
Восстановление сенсомоторной функции и активности повседневной жизни после травмы шейного отдела спинного мозга Влияние возраста
лет.J Нейротравма
.2015
;32
(3
):194
—199
.30Dietz
V
,Sinkjaer
T.
Спастическое двигательное расстройство: нарушение рефлекторной функции и измененная механика мышц
.Ланцет Нейрол
.2007
;6
(8
):725
—733
.31Den Otter
AR
,Geurts
AC
,Mulder
T
,Duysens Восстановление походки не связано с изменениями во временном паттерне мышечной активности при ходьбе на беговой дорожке у пациентов с постинсультным гемипарезом
.Clin Neurophysiol
.2006
;117
(1
):4
—15
.32Дункан
P
,Студенски
S
,Ричардс
L
и др.Рандомизированное клиническое исследование лечебных упражнений при подостром инсульте
.Инсульт
.2003
;34
(9
):2173
—2180
. 33Globas
C
,Becker
C
,Cerny
J
и др.Выжившие после хронического инсульта получают пользу от высокоинтенсивных аэробных упражнений на беговой дорожке: рандомизированное контрольное исследование
.Neurorehabil Neural Repair
.2012
;26
(1
):85
—95
. 34Kwakkel
G
,Wagenaar
RC
,Twisk
JW
,Lankoets
0004,0004 LankJC.
Интенсивность тренировки ног и рук после первичного инсульта средней мозговой артерии: рандомизированное исследование
.Ланцет
.1999
;354
(9174
):191
—196
.35Langhorne
P
,Coupar
F
,Pollock
A.
Восстановление двигателя после хода двигателя..Ланцет Нейрол
.2009
;8
(8
):741
—754
,36Wirz
M
,Mach
O
,Maier
D
и др.Эффективность автоматизированной тренировки опорно-двигательного аппарата у пациентов с острым неполным повреждением спинного мозга: рандомизированное контролируемое многоцентровое исследование
.J Нейротравма
.2017
;34
(10
):1891
—1896
.37Wirz
M
,Zemon
DH
,Rupp
R
и др.Эффективность автоматизированной тренировки опорно-двигательного аппарата у пациентов с хронической неполной травмой спинного мозга: многоцентровое исследование
.Arch Phys Med Rehabil
.2005
;86
(4
):672
—680
.38Hubli
M
,Dietz
V
,Bolliger
M.
нейрональная активность позвоночника функциональность после травмы спинного мозга
.Neurorehabil Neural Repair
.2012
;26
(2
):188
—196
.39Lang
CE
,Strube
MJ
,Bland
MD
и др.Дозозависимая доза тренировки верхних конечностей для конкретных задач у людей по крайней мере через 6 месяцев после инсульта: фаза II, простое слепое, рандомизированное, контролируемое испытание
.Энн Нейрол
.2016
;80
(3
):342
—354
.40Tetzlaff
W
,Okon
EB
,Karimi-Abdolrezaee
S.
Систематический обзор методов клеточной трансплантации при травмах спинного мозга
.J Нейротравма
.2011
;28
(8
):1611
—1682
.41Bunge
MB
,Pearse
DD.
Стратегии трансплантации, способствующие восстановлению поврежденного спинного мозга
.J Rehabil Res Dev
.2003
;40
(4 Suppl 1
):55
—62
.42Fortun
J
,Hill
CE
,Bunge
MB.
Комбинаторные стратегии с трансплантацией шванновских клеток для улучшения восстановления поврежденного спинного мозга
.Neurosci Lett
.2009
;456
(3
):124
—132
.43Mackay-Sim
A
,Feron
F
,Cochrane
J
и др.Трансплантация аутологичных обонятельных клеток при параплегии человека: 3-летнее клиническое испытание
.Мозг
.2008
;131
(Pt 9
):2376
—2386
.44Добкин
BH
,Curt
A
,Guest
J. из крупнейшего человеческого эксперимента по хронической травме спинного мозга
.Neurorehabil Neural Repair
.2006
;20
(1
):5
—13
.45Леви
AD
,Андерсон
KD
,Okonkwo
DO
,Park
P
и др.Клинические результаты многоцентрового исследования трансплантации нервных стволовых клеток человека при хроническом повреждении шейного отдела спинного мозга
.J Нейротравма
.2019
;36
(6
):891
—902
.46Schwab
ME.
Функции белков Nogo и их рецепторов в нервной системе
.Нат Рев Neurosci
.2010
;11
(12
):799
—811
.47Zorner
B
,Schwab
ME.
Anti-Nogo на ходу: от животных моделей до клинических испытаний
.Ann N Y Acad Sci
.2010
;1198
(Suppl 1
):E22
—34
.48Wagner
FB
,Mignardot
JB
,Le Goff-Mignardot al.
CG
CG
Целенаправленная нейротехнология восстанавливает ходьбу у людей с травмой спинного мозга
.Природа
.2018
;563
(7729
):65
—71
.49Бахманн
LC
,Матис
A
,Линдау
NT
,Felder
Felder
M
,Schwab
ME.
Глубокая стимуляция локомоторной области среднего мозга улучшает паретическую функцию задних конечностей после травмы спинного мозга у крыс
.Научный перевод медицины
.2013
;5
(208
):208ra146
.SCI =
CST =
© Автор (ы) (2021). Опубликовано Oxford University Press от имени Гарантов Мозга.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное повторное использование, распространение и воспроизведение на любом носителе при условии, что оригинал работа правильно процитирована.механизмов восстановления двигательной функции после инсульта | Цереброваскулярные заболевания | JAMA Neurology
Инсульт — основная причина длительной нетрудоспособности во всем мире и состояние, от которого не существует общепринятого лечения. Разработка новых эффективных терапевтических стратегий зависит от лучшего понимания механизмов, лежащих в основе восстановления функции. Неинвазивные методы изучения функции мозга, включая функциональную магнитно-резонансную томографию, позитронно-эмиссионную томографию, транскраниальную магнитную стимуляцию, электроэнцефалографию и магнитоэнцефалографию, привели к недавним исследованиям, которые выявили некоторые из этих действующих механизмов, что привело к разработке новых подходов к двигательной реабилитации.
Инсульт — основная причина инвалидности во всем мире. Ценность специфических реабилитационных методов лечения, направленных на помощь в адаптации к нарушениям, в настоящее время хорошо известна, но терапевтические стратегии, предназначенные для восстановления функции путем минимизации нарушений, по сравнению с этим, разработаны плохо. В этом обзоре рассматриваются успехи, достигнутые в понимании того, как реорганизация мозга после очагового повреждения связана с функциональным восстановлением и как эти идеи могут быть преобразованы в клиническую пользу для пациентов.
Мозг как пластическая структура
Термин пластичность часто используется при рассмотрении механизмов восстановления после очаговой травмы головного мозга. Более 50 лет назад Хебб 1 постулировал, что увеличение синаптической эффективности происходит во время обучения, когда активация одного нейрона многократно вызывает возбуждение в другом нейроне, с которым он связан, что привело к понятию пластичности как поведенческой адаптации (т. ), что связано с изменением функции на уровне синапса.Выраженный в системной структуре, термин пластичность может относиться к изменениям в мозговых сетях, которые имеют поведенческие последствия с течением времени. Кора головного мозга с ее бесчисленными синаптическими связями является идеальным местом для проявления пластичности. 2 Пластические изменения на корковом уровне могут происходить разными способами. Во-первых, неоднократно было продемонстрировано, что обогащенная среда и обучение навыкам у взрослых животных связаны с ростом дендритов, увеличением дендритных шипов и синаптогенезом. 3 Во-вторых, долговременная потенциация и долговременная депрессия являются механизмами изменения синаптической эффективности в гиппокампе 4 и неокортексе при определенных условиях. 5 Действительно, обучение двигательным навыкам на животных моделях сопровождается изменениями силы связей в первичной моторной коре головного мозга. 6 Кроме того, есть свидетельства того, что эти механизмы могут действовать и в моторном обучении человека. 7 , 8 В-третьих, кортикальные карты поддерживаются, по крайней мере, частично, за счет γ-аминомасляной кислоты и могут быть намеренно изменены фармакологическими манипуляциями 9 и непреднамеренно повреждениями.Связь между изменением структуры мозга и изменением поведения твердо установлена.
Работа на животных моделях недвусмысленно продемонстрировала, что очаговое повреждение во взрослом мозге делает обширные области коры более способными изменять структуру и функции в ответ на афферентные сигналы, как это ранее наблюдалось в развивающемся мозге. Изменения, вызванные активностью в этих областях, могут быть усилены экспериментальными манипуляциями 10 или фармакологическими вмешательствами 11 и коррелируют с функциональным восстановлением.Эти открытия явно очень интересны для врачей. Предполагается, что аналогичные вызванные травмой изменения происходят в мозге человека, и что манипуляции с этими процессами могут способствовать восстановлению. Такие методы, как функциональная магнитно-резонансная томография и позитронно-эмиссионная томография, которые позволяют измерять связанную с задачей активацию мозга с превосходным пространственным разрешением; транскраниальная магнитная стимуляция (ТМС), безопасный, неинвазивный способ возбуждения или подавления коры головного мозга человека с высоким временным разрешением; магнитоэнцефалография и электроэнцефалография с еще большим временным разрешением позволяют изучать эти изменения.
Как мозг человека реагирует на очаговое повреждение?
После очаговой травмы головного мозга, приведшей к моторному дефициту, степень повреждения кортикоспинального тракта хорошо коррелирует с восстановлением моторики. He et al., , 12, предположили, что прерывание проекций от первичной моторной коры (M1) к моторным нейронам спинного мозга приведет к увеличению задействования вторичных моторных областей, таких как дорсолатеральная премоторная кора (PMd) и дополнительная моторная область.Недавние исследования на обезьянах продемонстрировали, что вторичные моторные области имеют прямые проекции на мотонейроны спинного мозга, хотя они менее многочисленны и менее возбуждающи, чем те, которые находятся в M1. Таким образом, хотя они могут способствовать восстановлению, маловероятно, что они полностью заменят прогнозы от M1. Эта точка зрения подтверждается недавним исследованием функциональной визуализации, проведенным у пациентов с хроническим инсультом, которое продемонстрировало отрицательную линейную корреляцию между исходом и связанной с задачей активацией мозга в ряде вторичных моторных областей, таких как PMd, дополнительная моторная зона и поясная моторная зона 13 (рисунок 1).Пациенты без остаточных нарушений имеют относительно нормальные карты активации по сравнению с контрольной группой, в то время как пациенты с более выраженными нарушениями задействуют большие участки вторичных моторных областей. Но способствуют ли эти регионы выздоровлению? Нарушение ипсилезии PMd 14 и контратезии PMd 15 с помощью TMS увеличивает время моторной реакции у пациентов с хроническим инсультом, но не в контрольной группе. Кроме того, ТМС на ипсилезионную ПМД была разрушительной у пациентов с небольшими нарушениями, 14 , в то время как ТМС на противоположные ПМД была более разрушительной у пациентов с более сильными двигательными нарушениями, 15 , что указывает на функционально релевантное привлечение контратолевых ПМД у тех, кто больше всего в ней нуждался.Кроме того, кажется, что некоторые вторичные моторные области могут взять на себя новые функции после функционального восстановления. Ипсилезионный PMd, в частности, по-видимому, ведет себя как «исполнительная» моторная область, подобная M1, при этом активация, связанная с заданием, линейно возрастает в зависимости от увеличения силы захвата руки у тех, кто с неполным восстановлением, но не в контроле. 16 Таким образом, появляются доказательства, подтверждающие функциональную значимость рекрутирования вторичных моторных областей. У некоторых пациентов результат может быть ограничен степенью повреждения прямых кортикоспинальных проекций, но привлечение и адаптация выживших вторичных моторных областей в обоих полушариях может помочь пациентам достичь наилучших результатов. 14 , 15 Хотя эти результаты описаны у пациентов с хроническим инсультом, задействование вторичных моторных областей происходит у пациентов с большим дефицитом как в ранней, так и в хронической фазе после инсульта. 16
Первичная моторная кора (M1) делится на передний (область Бродмана [BA] 4a) и задний (BA4p) сегменты. Об отрицательной корреляции между размером активации и исходом сообщалось в ипсилезионных вентральных BA4a и BA4p, а также в контрацептивных BA4p, но не в BA4a. 13 Кажется очевидным, что неповрежденный ипсилезионный M1 вносит значительный вклад в функциональное восстановление, 17 , но роль контрацептивного M1 менее ясна. Несмотря на то, что контрочувствительный M1 рекрутируется пациентами с хроническим инсультом с неполным выздоровлением, его нарушение с помощью TMS, по-видимому, не ухудшает выполнение двигательных задач паретичной рукой у пациентов с различной степенью выздоровления. 17 Что более важно, возможно, что активность контрацептивного M1 отрицательно влияет на выздоровление у некоторых пациентов, внося свой вклад в аномальные межполушарные взаимодействия во время произвольного движения паретичной руки. 18 Роль контрацептивного поражения M1 после инсульта явно требует дальнейшего изучения.
В хронических условиях, похоже, поврежденный мозг будет использовать уцелевшие структуры и сети, которые могут генерировать моторные сигналы в той или иной форме для мотонейронов спинного мозга. Кроме того, некоторые области берут на себя новую роль в моторных характеристиках. Такие исследования не говорят нам о том, как развивалось это реорганизованное государство. Подробные исследования с использованием продольной функциональной магнитно-резонансной томографии у аналогичных пациентов указывают на начальную гиперактивацию во многих первичных и вторичных двигательных областях, за которой следует фокусировка на нормальном паттерне активации, параллельном выздоровлению. 16 Такие изменения напоминают изменения, наблюдаемые в нормальном мозге во время обучения двигательным навыкам. В мозге с повреждениями вполне вероятно, что выжившие элементы хорошо сохранившихся нейронных систем, такие как те, которые обслуживают обучение двигательным навыкам, будут задействованы для максимального функционального восстановления моторики. Степень, в которой механизмы, лежащие в основе реорганизации головного мозга, успешны, вероятно, зависит от функциональной целостности остальных областей. Хроническое течение инсульта также может иметь значение, поскольку гипервозбудимость коры, вызванная ранним поражением, по-видимому, способствует ее пластичности.Достигнуты успехи, но для разработки более эффективных терапевтических стратегий потребуется более четкое понимание механизмов, лежащих в основе реорганизации головного мозга.
Возможные стратегии усиления реакции человеческого мозга на травму
Очевидно, что после очаговой травмы в головном мозге человека происходят функционально значимые адаптивные изменения.Но что движет этими изменениями? Можем ли мы их модулировать? Урок, полученный на животных моделях, заключается в том, что манипуляции с окружающей средой, поведенческими и фармакологическими контекстами могут влиять на реорганизацию головного мозга и, следовательно, на процесс восстановления функции. Как эти уроки могут принести пользу пациентам? Исходя из наших знаний о том, как мозг реагирует на очаговое повреждение и как это связано с восстановлением, мы можем генерировать основанные на гипотезах подходы к нейрореабилитации. Например, на двигательные характеристики паретичной руки теоретически может влиять ряд различных операционных стратегий (рис. 2):
Уменьшение соматосенсорного воздействия от неповрежденной руки, как при кожной анестезии, приводит к повышению производительности руки без анестезии у здоровых добровольцев. 19 У пациентов с хроническим инсультом кожная анестезия неповрежденной руки приводит к улучшению поведения паретичной руки, которое кратковременно превышает продолжительность анестезии 20 (обозначено цифрой 1 на рисунке 2). Эти результаты согласуются с предполагаемым положительным влиянием иммобилизации неповрежденной руки (что снижает соматосенсорное воздействие от иммобилизованной конечности) у пациентов с хроническим инсультом, проходящих терапию движением, вызванную ограничениями.
Увеличение соматосенсорного ввода от паретичной руки, например, с помощью соматосенсорной стимуляции, может улучшить двигательную функцию. 21 (обозначено цифрой 2 на рисунке 2).Моторная тренировка паретичной руки, проводимая во время реабилитационного лечения, также увеличивает соматосенсорное воздействие и приводит к хорошо задокументированным улучшениям в поведении.
Анестезия части тела проксимальнее паретичной кисти (плечо, 3 на рис. 2) может стать еще одним вариантом улучшения двигательной функции кисти. 22 В этом случае анестезия областей плечевого сплетения, которые иннервируют пораженную верхнюю конечность, но не пораженную руку, у пациентов с хроническим инсультом приводит к зависящим от тренировки улучшениям двигательной функции паретичной руки, что согласуется с точка зрения, что кортикальное представительство паретической руки простиралось на близлежащее глухое представление плеча.
Пластичность в пораженной моторной коре может быть увеличена (4 на рисунке 2). Может быть важным усиление способности периинфарктных и непервичных двигательных областей пораженного полушария реагировать на двигательную тренировку или другие нейрореабилитационные вмешательства. Стимуляция коры может изменять активность моторной коры головного мозга у животных 23 и модулировать пластичность коры у людей. Например, TMS, синхронно применяемая к моторной коре головного мозга человека, занятой двигательной тренировкой, повышает пластичность, зависящую от использования, в противоположной руке. 24 В целом, эти результаты предполагают, что неинвазивная кортикальная стимуляция может представлять собой дополнение к двигательной тренировке в усилиях по восстановлению утраченной функции после корковых поражений, таких как инсульт. В соответствии с этой точкой зрения, недавнее исследование показало, что неинвазивная кортикальная стимуляция может улучшить двигательную функцию у пациентов с хроническим инсультом (Фридхельм Хуммель, доктор медицины, Пабло Цельник, доктор медицины, Паскаль Жиро, доктор медицины, доктор философии, Агнес Флор, доктор медицины, Ван-Сун Ву, Доктор философии, Кристиан Герлофф, доктор медицины и LGC, неопубликованные данные, 2004 г.
Активность интактной моторной коры может быть подавлена (5 на рисунке 2). В дополнение к локальным эффектам в месте стимуляции кортикальная стимуляция, применяемая к одному месту, может вызывать отдаленные эффекты на функцию и поведение коры. 25 Например, ТМС, примененная к одной моторной коре, вызывает изменения активации в позитронно-эмиссионных томографических снимках в противоположной моторной коре. Низкочастотная повторяющаяся ТМС, применяемая к одной моторной коре, подавляет возбудимость моторной коры в гомонимном моторном представлении в противоположном полушарии 26 , что согласуется с концепцией физиологического баланса реципрокных тормозных проекций между обоими полушариями.Недавние исследования показали, что этот баланс нарушается у пациентов с корковыми поражениями, такими как инсульт, в процессе генерации произвольного движения паретичной рукой. В частности, у некоторых из этих пациентов обнаруживается аномально высокий межполушарный тормозной драйв от M1 в интактном полушарии до M1 в пораженном полушарии, 18 — обнаружение, которое более заметно у людей с более слабыми нарушениями. Следовательно, возможно, что одним из способов усиления моторной функции паретичной руки является подавление активности в ипсилатеральной, неповрежденной моторной коре (с целью уменьшения аномального торможения от неповрежденного к пораженному полушарию), гипотеза ниже изучение.Предыдущее исследование действительно показало, что ТМС с частотой 1 Гц, примененная к одной моторной коре у здоровых людей, приводит к улучшению моторных характеристик ипсилатеральной руки. 27
Фармакологические вмешательства могут усилить процессы восстановления, воздействуя на адренергическую и дофаминергическую нейротрансмиссию. В дополнение к ранее описанным поведенческим и физиологическим вмешательствам на процессы восстановления могут существенно влиять фармакологические стратегии, которые влияют на адренергическую и дофаминергическую нейротрансмиссию. 28
Вероятно, что методы нейровизуализации (функциональная магнитно-резонансная томография, позитронно-эмиссионная томография) и электрофизиологические (ТМС, электроэнцефалография, магнитоэнцефалография) улучшат наше понимание механизмов, лежащих в основе положительных эффектов конкретных вмешательств. Недавние исследования показали повышенную активацию, связанную с заданием, в пораженных полушариях (например, в M1 или PMd) и пониженную активацию в здоровых полушариях после периода лечения, 29 -31 , но еще предстоит определить, относятся ли эти результаты к механизмы или только последствия реабилитационного процесса.Дальнейшие эксперименты, которые проверяют влияние вмешательств на определенные аспекты функции мозга, например, пластичность, зависящую от использования, 7 в различных группах пациентов, могут помочь раскрыть основные механизмы. Такой подход может позволить нацелить лечение на подходящих пациентов. Кроме того, время вмешательства также может иметь значение. Например, изменение внимания к двигательной задаче может быть более или менее полезным в зависимости от хронического характера инсульта. 32
Таким образом, недавние исследования начали раскрывать механизмы, лежащие в основе пластичности коры головного мозга человека и ее связь с восстановлением двигательной функции после очаговых поражений головного мозга.На основе этого более глубокого понимания тестируются новые интервенционные стратегии, которые вселяют надежду на разработку новых методов лечения этого состояния.
Для корреспонденции: Леонардо Г. Коэн, Отдел физиологии коры человека, Национальный институт неврологических расстройств и инсульта, корп. 10, кабинет 5N226, Национальные институты здравоохранения, Бетесда, Мэриленд 20817 (cohen@ninds.nih.gov).
Принята к публикации: 16 июля 2004 г.
Вклад авторов: Доктора Уорд и Коэн внесли равный вклад во все аспекты этого исследования.
1.Hebb DO Организация поведения . Нью-Йорк, штат Нью-Йорк: John Wiley & Sons; 1949
3.Иванко TLGreenough WT. Физиологические последствия морфологически определяемой синаптической пластичности: потенциальное использование для изучения восстановления после повреждения. Нейрофармакология 2000; 39765-776PubMedGoogle ScholarCrossref 5.Hess GDonoghue JP Долгосрочная потенциация и долговременная депрессия горизонтальных связей в моторной коре головного мозга крыс. Acta Neurobiol Exp (Warsz) 1996; 56397-405PubMedGoogle Scholar6.Rioult-Pedotti М. С. Фридман DHess GDonoghue JP Укрепление горизонтальных корковых связей после обучения навыкам. Nat Neurosci 1998; 1230-234PubMedGoogle ScholarCrossref 7.Butefisch CMDavis BCWise SP и другие.Механизмы зависимой от использования пластичности моторной коры головного мозга человека. Proc Natl Acad Sci U S A 2000; 973661-3665PubMedGoogle ScholarCrossref 8.Ziemann UIliac TVPauli CMeintzschel FRuge D Обучение изменяет последующую индукцию долговременной пластичности, подобной потенцированию, и долговременной депрессии, в моторной коре головного мозга человека. J Neurosci 2004; 241666-1672PubMedGoogle ScholarCrossref 9.Jacobs KMDonoghue JP Изменение корковой моторной карты путем выявления скрытых внутрикортикальных связей. Science 1991; 251944- 947PubMedGoogle ScholarCrossref 10. Нудо RJWise BMSiFuentes FMilliken GW Нейронные субстраты для влияния реабилитационных тренировок на восстановление моторики после ишемического инфаркта. Science 1996; 2721791-1794PubMedGoogle ScholarCrossref 11.Фини DMGonzalez Закон WA Амфетамин, галоперидол и опыт взаимодействуют, влияя на скорость восстановления после повреждения моторной коры. Science 1982; 217855-857PubMedGoogle ScholarCrossref 12.Он SQDum RPStrick П.Л. Топографическая организация кортикоспинальных проекций лобной доли: двигательные зоны на боковой поверхности полушария. J Neurosci 1993; 13952- 980PubMedGoogle Scholar13.Ward NSBrown MMThompson AJFrackowiak RS Neural корреляты исходов после инсульта: поперечное исследование фМРТ. Мозг 2003; 1261430–1448PubMedGoogle ScholarCrossref 14. Фридман EAHanakawa TChung MHummel FLeiguarda RCCohen LG Реорганизация премоторной коры головного мозга человека после восстановления после инсульта. Мозг 2004; 127747-758PubMedGoogle ScholarCrossref 15. Йохансен-Берг HRushworth М.Ф. Богданович МДКищка UWimalaratna SMatthews PM Роль ипсилатеральной премоторной коры в движении рук после инсульта. Proc Natl Acad Sci U S A 2002; 98-14523PubMedGoogle ScholarCrossref 16. Ward NSBrown MMThompson AJFrackowiak RS Neural корреляты восстановления моторики после инсульта: продольное исследование фМРТ. Мозг 2003; 1262476-2496PubMedGoogle ScholarCrossref 17.Werhahn KJConforto ABKadom NHallett MCohen LG Вклад ипсилатеральной моторной коры в восстановление после хронического инсульта. Ann Neurol 2003; 54464-472PubMedGoogle ScholarCrossref 18.Murase NDuque JMazzocchio RCohen Л.Г. Влияние межполушарных взаимодействий на двигательную функцию при хроническом инсульте. Ann Neurol 2004; 55400-409PubMedGoogle ScholarCrossref 19.Werhahn KJMortensen Ян Бовен RWZeuner KECohen LG Повышенная тактильная пространственная острота зрения и обработка коры головного мозга при острой деафферентации кисти. Nat Neurosci 2002; 5936-938PubMedGoogle ScholarCrossref 20.Floel ANagorsen UWerhahn КДж и другие. Влияние соматосенсорного ввода на двигательную функцию у пациентов с хроническим инсультом. Ann Neurol 2004; 56206-212PubMedGoogle ScholarCrossref 21.Conforto А.Б.Каэлин-Ланг ACohen LG Увеличение силы мышц рук у больных с инсультом после соматосенсорной стимуляции. Ann Neurol 2002; 51122-125PubMedGoogle ScholarCrossref 22.Muellbacher WRichards CZiemann U и другие. Улучшение функции рук при хроническом инсульте. Arch Neurol 2002; 5
-1282PubMedGoogle ScholarCrossref 23. Nudo RJJenkins В.М.Мерзених MM Повторяющаяся микростимуляция изменяет корковое представление движений у взрослых крыс. Somatosens Mot Res 1990; 7463-483PubMedGoogle ScholarCrossref 24.Butefisch CХурана В.Копылев LCohen LG Улучшение кодирования моторной памяти в первичной моторной коре с помощью корковой стимуляции. J Нейрофизиол 2004;
0-2116PubMedGoogle ScholarCrossref 25.Siebner HRPeller М.Уиллох F и другие. Длительная корковая активация после повторяющейся ТМС моторной коры: исследование метаболизма глюкозы. Неврология 2000; 54956- 963PubMedGoogle ScholarCrossref 26.Schambra HMSawaki LCohen LG Модуляция возбудимости моторной коры головного мозга человека (M1) транскраниальной магнитной стимуляцией 1 Гц контралатерального M1. Clin Neurophysiol 2003; 114130-133PubMedGoogle ScholarCrossref 27.Кобаяши MHutchinson STheoret HSchlaug GPascual-Leone Повторяющаяся ТМС моторной коры улучшает ипсилатеральные последовательные простые движения пальцев. Неврология 2004; 6291-98PubMedGoogle ScholarCrossref 28.Butefisch CMDavis BCSawaki L и другие. Модуляция зависимой от употребления пластичности d-амфетамином. Ann Neurol 2002; 5159-68PubMedGoogle ScholarCrossref 29.Pariente JLoubinoux ICarel C и другие.Флуоксетин регулирует двигательную активность и активацию мозга у пациентов, выздоравливающих после инсульта. Ann Neurol 2001; 50718-729PubMedGoogle ScholarCrossref 30. Йохансен-Берг HDawes HGuy CSmith SMWade DTM Этьюз PM Корреляция между улучшением моторики и измененной активностью фМРТ после реабилитационной терапии. Brain 2002; 1252731-2742PubMedGoogle ScholarCrossref 31.Schaechter JDKraft EHilliard TS и другие.Восстановление моторики и кортикальная реорганизация после принудительной двигательной терапии у пациентов с инсультом: предварительное исследование. Neurorehabil Neural Repair 2002; 16326-338PubMedGoogle ScholarCrossref 32. Ward NSBrown MMThompson AJFrackowiak RS Влияние времени после инсульта на активацию мозга при выполнении двигательной задачи. Ann Neurol 2004; 55829-834PubMedGoogle ScholarCrossrefИсследование: Генная терапия может восстановить зрение после инсульта
Ключевые результаты исследования
Большинство инсультов случаются, когда закупоривается артерия в головном мозге.Приток крови к нервной ткани прекращается, и эти ткани обычно умирают. Из-за расположения основных артерий в головном мозге многие инсульты влияют на двигательную функцию. Однако некоторые из них влияют на зрение, в результате чего пациенты теряют зрение или находят его нарушенным или ухудшенным. Исследовательская группа под руководством Александра Чубыкина из Университета Пердью, доцента биологических наук в Колледже наук, в сотрудничестве с командой под руководством Гун Чена из Цзинаньского университета, Китай, открыла способ использования генной терапии для превращения глиальных клеток мозга. в нейроны, восстанавливая зрительную функцию и давая надежду на восстановление двигательной функции.
Нейроны не регенерируют. Мозг может иногда перераспределять свои нервные пути в достаточной степени, чтобы восстановить некоторые зрительные функции после инсульта, но этот процесс медленный, неэффективный, а у некоторых пациентов этого никогда не происходит. Терапия стволовыми клетками, которая может помочь, основывается на поиске иммунного соответствия и является обременительной и сложной. Эта новая генная терапия, продемонстрированная на мышиной модели, более эффективна и многообещающа.
«Мы напрямую перепрограммируем локальные глиальные клетки в нейроны», — сказал Чубыкин.«Нам не нужно имплантировать новые клетки, поэтому иммуногенное отторжение отсутствует. Этот процесс легче осуществить, чем терапию стволовыми клетками, и при этом меньше повреждается мозг. Мы помогаем мозгу исцелять себя. Мы видим, как восстанавливаются связи между старыми нейронами и вновь перепрограммированными нейронами. Мы можем наблюдать, как мыши возвращаются к своему зрению ».
Исследования Чубыкина особенно важны, потому что зрительную функцию легче измерить, чем двигательные навыки, точно измерить, используя методы, включая оптическое отображение на живых мышах, для отслеживания развития и созревания недавно преобразованных нейронов в течение нескольких недель.Совершенствование и понимание этой техники может привести к аналогичной технике восстановления двигательной функции. Это исследование устраняет разрыв в понимании основной интерпретации нейронов и функций органов.
Опыт профессора Purdue
Чубыкин — эксперт в том, как нейроны реагируют на зрительные переживания, а также на такие состояния, как аутизм и ишемический инсульт. Он связан с Институтом интегративной неврологии Пердью и Центром исследования аутизма Пердью.
Название журнала
Границы клеточной биологии и развития. Статья доступна в Интернете.
Финансирование
Грант Национального института психического здоровья РФ1 Mh223401
Краткое описание методов
Команда смоделировала ишемический инсульт, поражающий зрительные центры в мозгу мышей, отображая и измеряя степень неврального и зрительного повреждения. Затем они использовали аденоассоциированные вирусы для доставки NeuroD1 к глиальным клеткам в пораженной части мозга.Они наблюдали и измеряли, как глиальные клетки были перепрограммированы в нейроны и интегрированы в зрительную кору. После этого они измерили реакцию этих клеток на зрительный стимул и составили карту развития зрительной коры, чтобы измерить восстановление зрительной функции.
Контактное лицо для писателей / СМИ: Бриттани Стефф, bsteff@purdue.edu
Источник: Александр Чубыкин, chubykin@purdue.edu
Восстановление после инсульта: современные концепции и перспективы на будущее | Неврологические исследования и практики
Амели М., Грефкес К., Кемпер Ф., Ригг Ф. П., Реме А. К., Карбе Х. и др. (2009). Дифференциальные эффекты высокочастотной повторяющейся транскраниальной магнитной стимуляции на ипсилезионную первичную моторную кору при инсульте корковой и подкорковой средней мозговой артерии. Анналы неврологии, 66 , 298–309.
PubMed Статья Google ученый
Bendszus, M., Bonekamp, S., Berge, E., Boutitie, F., Brouwer, P., Gizewski, E., et al. (2019). Рандомизированное контролируемое исследование для проверки эффективности и безопасности тромбэктомии при инсульте с расширенным поражением и расширенным временным окном. Международный журнал инсульта, 14 , 87–93.
PubMed Статья Google ученый
Bernhardt, J., Hayward, K. S., Kwakkel, G., Ward, N. S., Wolf, S. L., Borschmann, K., et al. (2017). Согласованные определения и общее видение новых стандартов в исследованиях восстановления после инсульта: рабочая группа по вопросам восстановления и реабилитации после инсульта. Нейрореабилитация и восстановление нервной системы, 31 , 793–799.
PubMed Статья Google ученый
Бестманн, С., Суэйн, О., Бланкенбург, Ф., Рафф, К. К., Тео, Дж., Вейскопф, Н. и др. (2010). Роль контратезионной дорсальной премоторной коры после инсульта, как изучено с одновременным TMS-fMRI. Журнал неврологии, 30 , 11926–11937.
CAS PubMed PubMed Central Статья Google ученый
Бонхофф, А.К., Хоуп, Т., Бздок, Д., Гуггисберг, А.Г., Хаве, Р.Л., Дюклоу, С.П., Рем, А.К., Финк, Г.Р., Грефкес, К., и Боуман, Х. (2020a). Пропорциональное восстановление: байесовское моделирование двигательной активности после инсульта. Мозг . https://doi.org/10.1093/brain/awaa146.
Bonkhoff, AK, Espinoza, FA, Gazula, H., Vergara, VM, Hensel, L., Michely, J., Paul, T., Rehme, A., Volz, LJ, Fink, GR , И Калхун, В.Д.(2020b). Грефкес С. Острый ишемический инсульт изменяет предпочтение головным мозгом различных состояний динамической связи. Мозг . https://doi.org/10.1093/brain/awaa101.
PubMed Статья PubMed Central Google ученый
Bonstrup, M., Krawinkel, L., Schulz, R., Cheng, B., Feldheim, J., Thomalla, G., et al. (2019). Низкочастотные колебания мозга отслеживают восстановление моторики при инсульте человека. Анналы неврологии, 86 , 853–865.
PubMed Статья Google ученый
Борич М. Р., Уитон Л. А., Броди С. М., Лахани Б. и Бойд Л. А. (2016). Оценка межполушарных корковых ответов на транскраниальную магнитную стимуляцию при хроническом инсульте: исследование ТМС-ЭЭГ. Neuroscience Letters, 618 , 25–30.
CAS PubMed PubMed Central Статья Google ученый
Кармайкл, С. Т., Вей, Л., Ровайнен, К. М., и Вулси, Т. А. (2001). Новые паттерны интракортикальных проекций после фокального коркового инсульта. Нейробиология болезней, 8 , 910–922.
CAS PubMed Статья Google ученый
Кармайкл, С. Т., Катирвелу, Б., Швеппе, К. А., и Ни, Э. Х. (2017). Молекулярные, клеточные и функциональные события в отрастании аксонов после инсульта. Экспериментальная неврология, 287 , 384–394.
CAS PubMed Статья Google ученый
Каррера Э. и Тонони Г. (2014). Диашизис: прошлое, настоящее, будущее. Мозг, 137 , 2408–2422.
PubMed Статья Google ученый
Chollet, F., DiPiero, V., Wise, R.J., Brooks, D.J., Dolan, R.J., & Frackowiak, R.S. (1991). Функциональная анатомия восстановления моторики после инсульта у людей: исследование с помощью позитронно-эмиссионной томографии. Анналы неврологии, 29 , 63–71.
CAS PubMed Статья Google ученый
Чоудхури Р. Н., Хасан А. Т., Ур Р. Ю., Хан С. И., Хуссейн А. Р. и Ахсан С. (2014). Характер неврологических заболеваний среди пациентов, госпитализированных в больницу третичного уровня. BMC Research Notes, 7 , 202.
PubMed PubMed Central Статья Google ученый
Крамер, С. С. (2008). Восстановление мозга человека после инсульта: I. Механизмы самопроизвольного выздоровления. Анналы неврологии, 63 , 272–287.
PubMed Статья Google ученый
Дикхофф-Кребс, С., Пул, Э. М., Сарфельд, А. С., Реме, А. К., Эйкхофф, С. Б., Финк, Г. Р. и др. (2017). Межиндивидуальные различия в подключении моторной сети и поведенческой реакции на iTBS у пациентов с инсультом. Neuroimage Clinical, 15 , 559–571.
PubMed PubMed Central Статья Google ученый
Дуглас, М. Р., Пик, Д., Стурман, С. Г., Сивагуру, А., Кларк, К. Э., и Николл, Д. Дж. (2011). Консультации по стационарному неврологу: стоимость и стоимость. Клиническая медицина (Лондон, Англия), 11 , 215–217.
CAS Статья Google ученый
Феда С., Никубашман О., Schurmann, K., Matz, O., Tauber, S.C., Wiesmann, M., et al. (2019). Эндоваскулярное лечение инсульта не исключает высоких показателей тромболизиса. Европейский журнал неврологии, 26 , 428 – e33.
CAS PubMed Статья Google ученый
Фёрч К., Миссельвиц Б., Зитцер М., Стейнмец Х. и Нойман-Хефелин Т. (2008). Прогнозируемое бремя инсульта в немецкой федеральной земле Гессен до 2050 года. Deutsches Ärzteblatt International, 105 , 467–473.
PubMed PubMed Central Google ученый
Фристон, К. Дж., Харрисон, Л., и Пенни, В. (2003). Динамическое причинно-следственное моделирование. Neuroimage, 19 , 1273–1302.
CAS PubMed Статья Google ученый
GBD 2016 Neurology Collaborators. (2020). Глобальное, региональное и национальное бремя неврологических расстройств, 1990-2016 гг .: систематический анализ исследования глобального бремени болезней, 2016 г. Lancet Neurology, 18 , 459–480.
Google ученый
Гоял М., Менон Б. К., ван Цвам В. Х., Диппель Д. В., Митчелл П. Дж., Демчук А. М. и др. (2016). Эндоваскулярная тромбэктомия после ишемического инсульта крупных сосудов: метаанализ данных отдельных пациентов из пяти рандомизированных исследований. Lancet, 387 , 1723–1731.
PubMed Статья Google ученый
Грау-Санчес, Дж., Мунте, Т. Ф., Альтенмюллер, Э., Дуарте, Э., и Родригес-Форнеллс, А. (2020). Потенциальные преимущества музыки при реабилитации моторики верхних конечностей после инсульта. Обзоры неврологии и биоповеденческих исследований, 112 , 585–599.
PubMed Статья Google ученый
Грефкес К. и Финк Г. Р. (2011). Реорганизация церебральных сетей после инсульта: новые идеи нейровизуализации с подходами к подключению. Мозг, 134 , 1264–1276.
PubMed PubMed Central Статья Google ученый
Грефкес К. и Финк Г. Р. (2014). Основанные на подключении подходы при инсульте и восстановлении функции. Lancet Neurology, 13 , 206–216.
PubMed Статья Google ученый
Грефкес К. и Финк Г. Р. (2016). Неинвазивная стимуляция мозга после инсульта: пришло время для крупных рандомизированных контролируемых исследований! Текущее мнение в неврологии, 29 , 714–720.
CAS PubMed Статья Google ученый
Грефкес, К., Новак, Д. А., Эйкхофф, С. Б., Дафотакис, М., Куст, Дж., Карбе, Х. и др. (2008). Корковая связность после подкоркового инсульта оценивается с помощью функциональной магнитно-резонансной томографии. Анналы неврологии, 63 , 236–246.
PubMed Статья Google ученый
Грефкес, К., Новак, Д. А., Ван, Л. Е., Дафотакис, М., Эйкхофф, С. Б., и Финк, Г. Р. (2010). Модуляция корковой связности у пациентов с инсультом с помощью rTMS, оцененная с помощью фМРТ и динамического причинно-следственного моделирования. Neuroimage, 50 , 233–242.
PubMed Статья Google ученый
Грефкес К. и Уорд Н. С. (2014). Кортикальная реорганизация после инсульта: насколько и насколько функционально? Невролог, 20 , 56–70.
PubMed Статья Google ученый
Хамада М., Мурас Н., Хасан А., Баларатнам М. и Ротвелл Дж. К. (2013). Роль интернейронных сетей в формировании пластичности моторной коры человека. Кора головного мозга, 23 , 1593–1605.
PubMed Статья Google ученый
Hamzei, F., Erath, G., Kucking, U., Weiller, C., & Rijntjes, M.(2020). Анатомия поражений головного мозга после инсульта позволяет прогнозировать эффективность зеркальной терапии. Европейский журнал неврологии . https://doi.org/10.1111/ejn.14698.
Хау Р. Л., Скотт С. Х. и Дюклоу С. П. (2018). Пропорциональное восстановление после инсульта. Инсульт, 50 , 204–211.
Артикул Google ученый
Hensel, L., Grefkes, C., Tscherpel, C., Ringmaier, C., Kraus, D., Hamacher, S., et al. (2019). Прерывистая стимуляция выброса тета, применяемая во время ранней реабилитации после инсульта: протокол исследования для рандомизированного контролируемого исследования. BMJ Open, 9 , e034088.
PubMed PubMed Central Статья Google ученый
Хоуп, Т. М. Х., Фристон, К., Прайс, К. Дж., Лефф, А. П., Ротштейн, П., и Боуман, Х. (2019). Восстановление после инсульта: все-таки не так пропорционально? Мозг, 142 , 15–22.
PubMed Статья Google ученый
Хордакр, Б., Гош, Р., Голдсуорси, М. Р., и Риддинг, М. К. (2019). Биомаркеры транскраниальной магнитной стимуляции-ЭЭГ моторной функции верхних конечностей после инсульта. Журнал инсульта и цереброваскулярных заболеваний, 28 , 104452.
PubMed Статья Google ученый
Howard, G., & Goff, D.С. (2012). Сдвиги населения и будущее инсульта: прогнозы будущего бремени инсульта. Анналы Нью-Йоркской академии наук, 1268 , 14–20.
PubMed PubMed Central Статья Google ученый
Ильмониеми Р. Дж. И Кичич Д. (2010). Методика комбинированной ТМС и ЭЭГ. Топография мозга, 22 , 233–248.
PubMed Статья Google ученый
Йохансен-Берг, Х., Рашворт, М. Ф., Богданович, М. Д., Кишка, У., Вималаратна, С., и Мэтьюз, П. М. (2002). Роль ипсилатеральной премоторной коры в движении рук после инсульта. Proceedings of the National Academy of Sciences of the United States of America, 99 , 14518–14523.
CAS PubMed PubMed Central Статья Google ученый
Ким, С. Ю., Оллред, Р. П., Адкинс, Д. Л., Теннант, К.А., Донлан Н. А., Клейм Дж. А. и др. (2015). Опыт с «хорошей» конечностью вызывает аберрантную синаптическую пластичность в перилезионной коре после инсульта. Журнал неврологии, 35 , 8604–8610.
CAS PubMed PubMed Central Статья Google ученый
Китагава К. (2007). Экспрессия генов, опосредованная CREB и цАМФ-ответными элементами, в ишемическом мозге. Журнал FEBS, 274 , 3210–3217.
CAS PubMed Статья Google ученый
Кваккель Г., Коллен Б. Дж., Ван дер Гронд Дж. И Прево А. Дж. (2003). Вероятность восстановления подвижности в вялой верхней конечности: влияние тяжести пареза и времени, прошедшего с момента возникновения острого инсульта. Инсульт, 34 , 2181–2186.
PubMed Статья Google ученый
Lefaucheur, J.П., Алеман, А., Бэкен, К., Беннингер, Д. Х., Брунелин, Дж., Ди, Л. В. и др. (2020). Основанные на фактах рекомендации по терапевтическому использованию повторяющейся транскраниальной магнитной стимуляции (пТМС): обновление (2014-2018). Клиническая нейрофизиология , 31 (5), 1168-1169.
PubMed Статья Google ученый
Манганотти П., Аклер М., Мазьеро С. и Дел Ф. А. (2015). Вызванные ТМС ответы N100 как прогностический фактор острого инсульта. Функциональная неврология, 30 , 125–130.
PubMed PubMed Central Google ученый
Nettekoven, C., Volz, L.J., Kutscha, M., Pool, E.M., Rehme, A.K., Eickhoff, S.B., et al. (2014). Дозозависимые эффекты тета-всплеска rTMS на возбудимость коры и связность двигательной системы человека в состоянии покоя. Журнал неврологии, 34 , 6849–6859.
CAS PubMed PubMed Central Статья Google ученый
Nettekoven, C., Volz, L.J., Leimbach, M., Pool, E.M., Rehme, A.K., Eickhoff, S.B., et al. (2015). Межиндивидуальная вариабельность корковой возбудимости и связности моторной сети после нескольких блоков rTMS. Neuroimage, 118 , 209–218.
PubMed PubMed Central Статья Google ученый
Нг, С. Х., Вонг, А. В. К., Чен, К. Х., Тан, С. С., Мюллер-Рименшнайдер, Ф., Чан, Б. П.L., et al. (2019). Факторы инсульта, связанные с использованием тромболизиса в больницах Сингапура и США: перекрестное сравнительное исследование. Цереброваскулярные заболевания, 47 , 291–298.
PubMed Статья Google ученый
Нисимура Ю., Оноэ Х., Моричика Ю., Перфильев С., Цукада Х. и Иса Т. (2007). Зависящие от времени центральные компенсаторные механизмы ловкости пальцев после травмы спинного мозга. Science, 318 , 1150–1155.
CAS PubMed Статья Google ученый
Новак Д. А., Грефкес К., Дафотакис М., Эйкхофф С., Куст Дж., Карбе Х. и др. (2008). Влияние низкочастотной повторяющейся транскраниальной магнитной стимуляции контратезионной первичной моторной коры на кинематику движения и нервную активность при подкорковом инсульте. Архив неврологии, 65 , 741–747.
PubMed Статья Google ученый
Pellicciari, M. C., Bonni, S., Ponzo, V., Cinnera, A. M., Mancini, M., Casula, E. P., et al. (2018). Динамическая реорганизация ТМС-вызванной активности у пациентов с подкорковым инсультом. Neuroimage, 175 , 365–378.
PubMed Статья Google ученый
Pool, E. M., Leimbach, M., Binder, E., Nettekoven, C., Eickhoff, S. B., Fink, G. R., et al. (2018). Сетевая динамика занимается модуляцией двигательного поведения у пациентов с инсультом. Картирование мозга человека, 39 , 1078–1092.
PubMed Статья Google ученый
Prabhakaran, S., Zarahn, E., Riley, C., Speizer, A., Chong, J. Y., Lazar, R.M, et al. (2008). Индивидуальная изменчивость способности к восстановлению моторики после ишемического инсульта. Нейрореабилитация и нейроремонт, 22 , 64–71.
PubMed Статья Google ученый
Реме, А.К., Айкхофф, С.Б., Ротчи, К., Финк, Г.Р., и Грефкес, К. (2012). Мета-анализ оценки вероятности активации двигательной нервной активности после инсульта. Neuroimage., 59 , 2771–2782.
PubMed Статья Google ученый
Реме А. К., Эйкхофф С. Б., Ван Л. Е., Финк Г. Р. и Грефкес К. (2011a). Динамическое причинно-следственное моделирование корковой активности от острой до хронической стадии после инсульта. Neuroimage, 55 , 1147–1158.
PubMed Статья Google ученый
Реме, А. К., Финк, Г. Р., фон Крамон, Д. Ю., и Грефкес, К. (2011b). Роль противоположной моторной коры для восстановления моторики в первые дни после инсульта оценивалась с помощью продольного FMRI. Кора головного мозга, 21 , 756–768.
PubMed Статья Google ученый
Реме А.К., Фольц Л.Дж., Фейс Д.Л., Бомилькар-Фокке И., Либих Т., Эйкхофф С.Б. и др. (2015a). Выявление нейровизуализационных маркеров двигательной инвалидности при остром инсульте с помощью методов машинного обучения. Кора головного мозга, 25 , 3046–3056.
CAS PubMed Статья Google ученый
Реме, А. К., Волц, Л. Дж., Фейс, Д. Л., Эйкхофф, С. Б., Финк, Г. Р., & Грефкес, К. (2015b). Индивидуальное прогнозирование хронических двигательных исходов в острой стадии после инсульта: поведенческие параметры по сравнению с функциональной визуализацией. Human Brain Mapping, 36, , 4553–4565.
PubMed PubMed Central Статья Google ученый
Роджерс Дж., Миддлтон С., Уилсон П. Х. и Джонстон С. Дж. (2019). Прогнозирование функциональных исходов после инсульта: обсервационное исследование одноканальной ЭЭГ в острой форме. Темы реабилитации после инсульта , 1–12.
Розанова, М., Госсериес, О., Касаротто, С., Боли, М., Казали, А.Г., Бруно, М. А. и др. (2012). Восстановление корковой эффективной связи и восстановление сознания у вегетативных пациентов. Мозг, 135 , 1308–1320.
PubMed PubMed Central Статья Google ученый
Ротвелл, Дж. К. (2016). Можно ли улучшить восстановление моторики при инсульте с помощью неинвазивной стимуляции мозга? Успехи экспериментальной медицины и биологии, 957 , 313–323.
PubMed Статья Google ученый
Заур Д., Ланге Р., Баумгаертнер А., Шракнеппер В., Уиллмес К., Рийнтьес М. и др. (2006). Динамика реорганизации языка после инсульта. Мозг, 129 , 1371–1384.
PubMed Статья Google ученый
Schroeter, M., Rezazadegan, K., Erbguth, F., Kiefer, R., Neumann-Haefelin, T., Redecker, C., et al. (2019). Struktur der Neurologischen Kliniken в Германии: Ergebnisse der 13.Erhebung der Deutschen Gesellschaft für Neurologie. DGNeurologie, 2 , 154–164.
Артикул Google ученый
Сигел, Дж. С., Зейтцман, Б. А., Рэмси, Л. Е., Ортега, М., Гордон, Э. М., Дозенбах, Н. У. Ф. и др. (2018). Возрождение модульных мозговых сетей в восстановлении после инсульта. Cortex, 101 , 44–59.
PubMed PubMed Central Статья Google ученый
Стагг, К.Дж., И Йохансен-Берг, Х. (2013). Изучение эффектов транскраниальной стимуляции постоянным током при восстановлении после инсульта с помощью магнитно-резонансной томографии. Frontiers in Human Neuroscience, 7 , 857.
PubMed PubMed Central Статья Google ученый
Стэгг, К. Дж., О’Ши, Дж., Кинсес, З. Т., Вулрич, М., Мэтьюз, П. М., и Йохансен-Берг, Х. (2009). Модуляция связанной с движением корковой активации путем транскраниальной стимуляции постоянным током. Европейский журнал неврологии, 30 , 1412–1423.
CAS PubMed Статья Google ученый
Стинеар, К. М. (2017). Прогнозирование восстановления моторики после инсульта: достижения в области биомаркеров. Lancet Neurology, 16 , 826–836.
PubMed Статья Google ученый
Stockert, A., Wawrzyniak, M., Klingbeil, J., Wrede, K., Kummerer, D., Hartwigsen, G., et al. (2020). Динамика реорганизации языка после левого височно-теменного и лобного инсульта. Мозг, 143 , 844–861.
PubMed Статья Google ученый
Thomalla, G., Simonsen, C.Z., Boutitie, F., Andersen, G., Berthezene, Y., Cheng, B., et al. (2018). Тромболизис под контролем МРТ при инсульте с неизвестным временем начала. Медицинский журнал Новой Англии, 379 , 611–622.
PubMed Статья Google ученый
Tscherpel, C., & Grefkes, C. (2019). Стимуляция мозга для лечения двигательного дефицита, связанного с инсультом. Nervenarzt, 90 , 1005–1012.
PubMed Статья Google ученый
Tscherpel, C., Hensel, L., Lemberg, K., Freytag, J., Michely, J., Volz, L.J., et al. (2020a). Возраст влияет на вклад ипсилатеральных областей мозга в кинематику движений. Картирование человеческого мозга, 41 , 640–655.
PubMed Статья Google ученый
Tscherpel, C., Hensel, L., Lemberg, K., Vollmer, M., Volz, L.J., Fink, G.R., et al. (2020b). Дифференциальная роль контратолевых лобно-теменных областей в корковой реорганизации после инсульта. Стимуляция мозга, 13 , 614–624.
PubMed Статья Google ученый
Черпель, К., Дерн, С., Хенсель, Л., Циманн, У., Финк, Г. Р., и Грефкес, К. (2020c). Чувствительность мозга позволяет индивидуально определять восстановление моторики после инсульта. Мозг . https://doi.org/10.1093/brain/awaa127.
ван дер Влит, Р., Селлес, Р. В., Андринопулу, Э. Р., Найланд, Р., Рибберс, Г. М., Френс, М. А., Мескерс, К., Кваккель, Г. (2020). Прогнозирование восстановления нарушения моторики верхних конечностей после инсульта: смешанная модель. Энн Нейрол, 87 (3), 383-393.
PubMed PubMed Central Статья Google ученый
Volz, L. J., Rehme, A. K., Michely, J., Nettekoven, C., Eickhoff, S. B., Fink, G. R., et al. (2016). Формирование ранней реорганизации нейронных сетей способствует развитию двигательной функции после инсульта. Кора головного мозга, 26 , 2882–2894.
CAS PubMed Статья Google ученый
Volz, L.Дж., Фоллмер, М., Мичели, Дж., Финк, Г. Р., Ротвелл, Дж. К., и Грефкес, К. (2017). Зависящая от времени функциональная роль контратолевой моторной коры после инсульта. Neuroimage Clin, 16 , 165–174.
CAS PubMed PubMed Central Статья Google ученый
фон Монаков К. (1914). Die Lokalisation im Grosshirn und der Abbau der Funktion durch kortikale Herde . Висбаден: Бергманн, Дж.Ф ..
Google ученый
Ван, Л. Э., Финк, Г. Р., Дикхофф, С., Реме, А. К., Эйкхофф, С. Б., & Грефкес, К. (2011). Норадренергическое усиление улучшает связность моторной сети у пациентов с инсультом. Анналы неврологии, 69 , 375–388.
PubMed Статья Google ученый
Wang, L.E., Tittgemeyer, M., Imperati, D., Diekhoff, S., Амели М., Финк Г. Р. и др. (2012). Дегенерация мозолистого тела и восстановление двигательной функции после инсульта: исследование мультимодальной магнитно-резонансной томографии. Human Brain Mapping, 33 , 2941–2956.
PubMed Статья Google ученый
Уорд, Н. С. (2017). Восстановление функции мозга после инсульта — сокращение разрыва между животными и людьми. Обзоры природы. Неврология, 13 , 244–255.
PubMed Статья Google ученый
Уорд, Н. С., Браун, М. М., Томпсон, А. Дж., И Фраковяк, Р. С. (2003). Нейронные корреляты восстановления моторики после инсульта: продольное исследование фМРТ. Мозг, 126 , 2476–2496.
CAS PubMed PubMed Central Статья Google ученый
Винтерс, К., ван Веген, Э. Э., Даффертсхофер, А., и Кваккель, Г. (2015). Обобщаемость модели пропорционального восстановления для верхней конечности после ишемического инсульта. Нейрореабилитация и восстановление нервной системы, 29 , 614–622.
PubMed Статья Google ученый
Возвращение к жизни после инсульта: Равиндер Сингх, доктор медицины: невролог и специалист по головным болям
Инсульт поражает более 700 000 американцев каждый год, и более полумиллиона из них выживают и начинают путь реабилитации. Цель — помочь пациентам восстановить свою жизнь. Это означает повторное обучение навыкам, утраченным из-за инсульта, и восстановление как можно большей независимости.Наши специалисты рассказывают, что вы или ваш близкий можете ожидать от реабилитации после инсульта.
Жизнь после инсульта
Инсульт может вызывать различные нарушения в зависимости от пораженной части мозга и тяжести инсульта. Как правило, инсульт может вызвать паралич или трудности с контролем движения, проблемы с памятью и мышлением, проблемы с использованием речи и сенсорные расстройства.
После того, как у вас или у вашего любимого человека случился инсульт, вы можете рассчитывать вместе со своей командой по уходу на цели, которые помогут вам максимально восстановить свою жизнь.
Цель постинсультной реабилитации
Хотя реабилитация не устраняет повреждение головного мозга, связанное с инсультом, она помогает выжившим после инсульта заново приобретать жизненно важные навыки, в том числе:
- Выступление
- Познание
- Управление точным двигателем
- Физическая координация
Это самые важные навыки для самостоятельного управления повседневной жизнью.
Рекавери у всех разные
Восстановление после инсульта индивидуально для каждого человека.Восстановление начинается с первого дня, а реабилитация начинается в больнице сразу после инсульта. Чаще всего реабилитация начинается в течение двух дней после инсульта и может продолжаться в течение недель, месяцев или нескольких лет.
Некоторые люди полностью выздоравливают, в то время как другие могут иметь длительную инвалидность. Для большинства выживших после инсульта выздоровление происходит постепенно и непредсказуемо. Поддержка друзей, семьи и опекунов является ключом к выздоровлению.
Реабилитация после инсульта
Программа реабилитации после инсульта очень индивидуальна.Тип инсульта и его тяжесть являются факторами при разработке наиболее подходящей программы реабилитации. Большинство людей, переживших инсульт, могут рассчитывать на выполнение упражнений на моторику и подвижность, а также на терапию диапазона движений.
Упражнения на моторику
Максимальное восстановление мелкой моторики — один из важнейших аспектов восстановления после инсульта. Мелкая моторика позволяет нам совершать движения с помощью мышц рук и запястий. Повседневные занятия, такие как держать ручку, писать и держать посуду для еды, требуют мелкой моторики.Переобучение мелкой моторики помогает людям, пережившим инсульт, самостоятельно кормиться и хвататься за предметы.
Упражнения на подвижность
Восстановление подвижности является одной из основных целей реабилитации после инсульта, поскольку помогает пациентам заново научиться ходить с использованием средств передвижения, включая трости и ходунки. Пациенты, которые не могут ходить, учатся пользоваться инвалидными колясками и самокатами. В терапию включены упражнения, укрепляющие мышцы и мышечную координацию.
Терапия по диапазону движений
Выполнение упражнений на диапазон движений помогает улучшить баланс, силу и работу суставов. Это помогает пациентам двигаться с полным диапазоном движений без боли. Частые и регулярные упражнения в течение первых шести месяцев после инсульта помогают восстановить сенсорную и двигательную функцию. Для достижения наилучшего результата упражнения на диапазон движений следует начинать как можно скорее после инсульта.
В реабилитации после инсульта участвует бригада врачей, медсестер и ряд терапевтов.Здесь, в Premier Neurology Group, специалист по неврологии доктор Равиндер Сингх координирует уход за пациентами, перенесшими инсульт, и рекомендует программу реабилитации, которая наилучшим образом соответствует вашим потребностям. Доктор Сингх дает рекомендации по изменениям, которые пациенты могут внести для предотвращения второго инсульта, включая контроль высокого кровяного давления, принятие диеты, полезной для сердца, и снижение веса, если у вас избыточный вес.
Когда дело доходит до восстановления после инсульта, на счету каждый день. Вы можете быть уверены, что наша команда будет рядом с вами на каждом этапе пути.Позвоните в наш офис в Беверли-Хиллз, Калифорния, чтобы назначить консультацию или записаться на прием онлайн сегодня.
Хирургическая процедура может помочь восстановить руку и
изображение: Результаты международных многоцентровых клинических испытаний показывают, что хирургическая процедура может помочь восстановить функцию кисти и руки после инсульта посмотреть еще
Предоставлено MicroTransponder Inc.
ЛОС-АНДЖЕЛЕС. Ежегодно более 795 000 человек в Соединенных Штатах страдают инсультом. Из них примерно 80% теряют функцию руки, и до 50-60% этой популяции все еще испытывают проблемы через шесть месяцев.
Традиционно пациенты, перенесшие инсульт, пытаются восстановить двигательную функцию посредством физической реабилитации, когда пациенты заново осваивают доинсультные навыки, такие как движения поедания и хватание. Однако у большинства пациентов в конечном итоге наблюдается стабилизация состояния, и со временем улучшение прекращается.
Теперь результаты клинических испытаний, опубликованные в Lancet , дают пациентам новую надежду на их выздоровление.
Пациенты, получившие новое лечение, сочетающее стимуляцию блуждающего нерва (VNS) и реабилитацию, показали улучшение двигательной недостаточности верхней части тела по сравнению с теми, кто получал фиктивную (неактивную форму) стимуляцию и реабилитацию. Блуждающий нерв, который считается естественной антенной для мозга, проходит от груди и живота до ствола мозга и регулирует многие функции организма.
«Это невероятно захватывающая новость для всех, кто занимается реабилитацией после инсульта и функциональным восстановлением, и представляет собой уникальное пересечение нейрохирургии и нейрореабилитации», — сказал Чарльз Лю, доктор медицинских наук, ведущий нейрохирург исследования и директор Центра нейрореставрации USC в Кеке. Медицина ОСК. «Эти результаты исследования являются первыми в своем роде и открывают новые возможности для пациентов с инсультом, позволяя им восстановить больше функций руки даже спустя годы после перенесенного инсульта.«
В этом международном многоцентровом клиническом исследовании 53 участника с умеренной и тяжелой слабостью руки от 9 месяцев до 10 лет после инсульта прошли реабилитацию в сочетании с VNS. Пятьдесят пять пациентов с одинаковыми параметрами получили фиктивную стимуляцию. Исследование было рандомизированным и тройным слепым.
У тех, кто получал стимуляцию нерва, в шею вставляли проволоку, которая оборачивалась вокруг блуждающего нерва. Затем провод был подключен к устройству генератора импульсов, имплантированному в грудную клетку.Те, кто получал имитацию, получали имплантаты плацебо.
После хирургической процедуры все пациенты получили шестинедельное лечение в клинике, которое включало такие задачи, как дотянуться и схватить, имитировать прием пищи, а также открывать и закрывать контейнеры. После госпитализации пациенты продолжили лечение курсом ежедневной домашней терапии.
При сравнении двух групп пациентов пациенты, получавшие нервную стимуляцию, получили более высокие баллы по нескольким стандартизированным показателям функциональности плеча.
«Результаты были не только клинически значимыми, но и тот факт, что эти пациенты находились после инсульта не менее девяти месяцев, а в некоторых случаях и лет спустя, указывает на возможность того, что значимые улучшения могут быть достигнуты даже спустя годы после инсульта», — сказал Лю. Он также является руководителем отдела инноваций и исследований и заведующим кафедрой нейрохирургии и ортопедии в Национальном реабилитационном центре Rancho Los Amigos.
Считается, что устройство запускает высвобождение нейромодуляторов мозга, которые регулируют реакции организма, для усиления двигательных цепей в мозге, связанных с движением, что позволяет мозгу эффективно переучивать задачи.VNS уже широко используется для лечения эпилепсии и играет все более важную роль в лечении тяжелой депрессии.
«Слишком долго пациенты с инсультом сталкивались с ограниченными возможностями выздоровления», — сказал Лю. «Это новое лечение означает прорыв, который может изменить жизнь многих пациентов с инсультом, а также представляет собой подход, который, безусловно, будет исследован для многих других приложений функционального восстановления в будущем».
###
Система VNS, использованная для исследования, принадлежит MicroTransponder Inc., компания-разработчик медицинского оборудования, спонсировавшая исследование.
Ведущие авторы исследования: Джесси Доусон, доктор медицины, Колледж медицины, ветеринарии и естественных наук, Университет Глазго в Шотландии; Тереза Дж. Кимберли, доктор философии, Массачусетская больница общего профиля; и Navzer Engineer, MD, PhD, MicroTransponder Inc.
Для получения дополнительной информации о Keck Medicine из USC, пожалуйста, посетите news.KeckMedicine.org.
Заявление об ограничении ответственности: AAAS и EurekAlert! не несут ответственности за точность выпусков новостей, размещенных на EurekAlert! участвующими учреждениями или для использования любой информации через систему EurekAlert.
Музыкальная терапия для восстановления двигательного дефицита после инсульта — Полный текст
По данным Всемирной организации здравоохранения, инсульт является одной из основных причин приобретенной инвалидности в развитых странах. Инсульт — это цереброваскулярное заболевание, при котором кровоснабжение головного мозга нарушается в результате ишемического или геморрагического события в мозговых артериях. Дефицит моторики, выражающийся в потере силы и ловкости, присутствует у большинства пациентов. Такой дефицит ограничивает выполнение повседневной деятельности (инвалидность) и влияет на участие пациентов в их сообществах (инвалидность), влияя на различные роли, которые они играют в различных социальных, знакомых и рабочих контекстах.Следовательно, снижается качество жизни пациентов, а также их эмоциональная валентность и настроение, которые могут перерасти в психическое расстройство (например, депрессию и апатию).
В дополнение к экономическим затратам на лечение после инсульта, явно подрывается способность пациентов трудоспособного возраста вносить свой вклад в общество посредством развития оплачиваемой профессии. Таким образом, уход за пациентами, которые не могут успешно восстановить свою двигательную функцию, требует больших затрат.В этом отношении инсульт является важным приоритетом здравоохранения из-за прямых (медицинских) и косвенных (например, безработица и потеря автономии) затрат.
Сделаны соответствующие выводы в области неотложной медицинской помощи при инсульте (т.е. минимизация осложнений, оптимизация лечения, тромбоз и стандартизированные инсультные отделения в больницах). Тем не менее, в области нейрореабилитации все еще имеется мало научных данных, которые однозначно подтверждают применение определенных методов лечения, которые используются в нескольких центрах.Таким образом, чрезвычайно важно исследовать методы моторной реабилитации, чтобы предоставить клиницистам доказательства их эффективности.
Один из подходов — проверка методов лечения, которые могут способствовать пластичности мозга, способности, при которой мозг изменяет свою структуру, функции и связи. Пластичность мозга может возникать спонтанно после поражения, но также обнаруживается во время и после обучения. Многие последовательные исследования продемонстрировали пластичность мозга на корковом и подкорковом уровнях благодаря обучению двигательным навыкам у здоровых людей.Таким образом, вмешательства, предполагающие приобретение новых двигательных навыков, могут быть хорошим подходом для содействия восстановлению двигательных функций у пациентов с инсультом. Примером двигательного навыка, включающего тонкие движения рук, является игра на музыкальном инструменте, деятельность с которой уникальна и требует сложных требований к центральной нервной системе. Взаимодействие между слуховой и двигательной системами устанавливается во время музыкального исполнения, поскольку звук инструмента обрабатывается и предполагается использовать для корректировки движений.Кроме того, было доказано, что музыкальное обучение приводит к структурным и функциональным изменениям в двигательных областях.
Недавно Шнайдер и его коллеги разработали новый инструмент нейрореабилитации для восстановления двигательного дефицита после инсульта: терапию с музыкальной поддержкой (MST). В этой терапии пациентов обучают игре на MIDI-пианино и электронном барабане для тренировки тонких и грубых движений соответственно. Исследования на острой и хронической стадиях показали, что пациенты улучшают свои двигательные функции благодаря терапии и что эти изменения сопровождаются пластичностью мозга.Однако до сих пор не существует четких доказательств преимущества этой терапии (MST) по сравнению с традиционной терапией, проводимой в больнице у подострых пациентов. Кроме того, ни одно предыдущее исследование не сравнивало напрямую изменения, наблюдаемые в головном мозге у пациентов с острым инсультом, с использованием функциональной и структурной нейровизуализации после МТ по сравнению с традиционной или стандартной терапией.
Мы предлагаем многоцентровое рандомизированное контролируемое исследование для проверки преимуществ MST по сравнению с традиционным лечением у пациентов с подострым инсультом с двигательной недостаточностью.В этом исследовании определены 3 группы лечения (обучение MST в больнице, обучение MST дома и традиционное лечение). Участники из всех групп будут оцениваться до и после лечения для оценки двигательных и когнитивных функций, эмоционального статуса, качества жизни и пластичности мозга, связанных с лечением, которые оцениваются с помощью методов нейровизуализации.


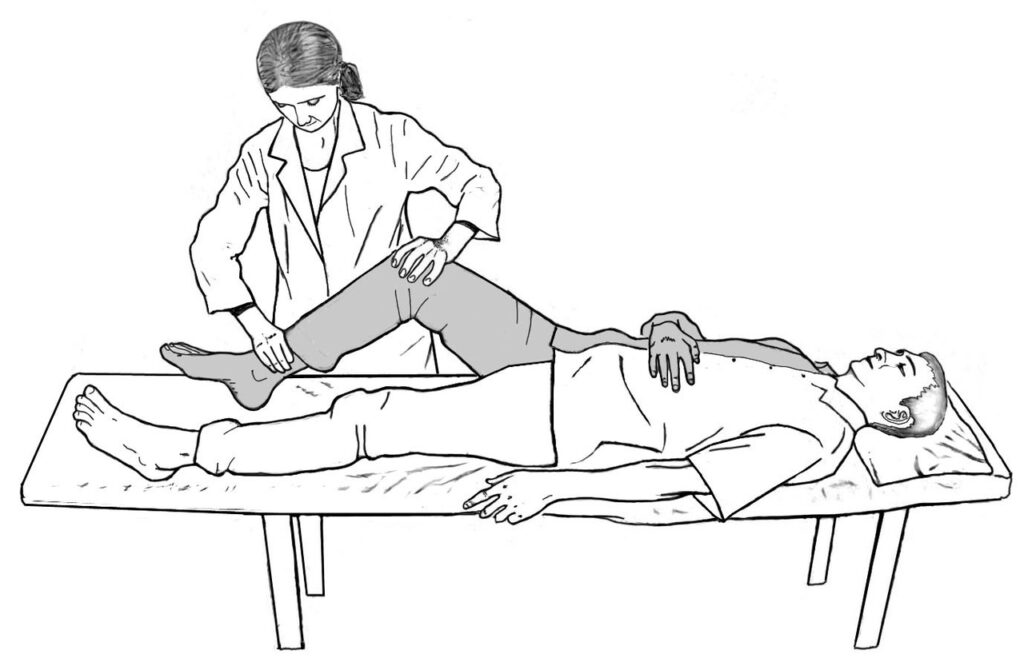


 Для успешного восстановления необходим сбалансированный рацион, исключающий тяжелую пищу (жирное, копченое, сладкое и т.д.) В меню должны быть фрукты, злаковые, овощи, постное мясо. Для установления правильного режима питания бывает необходима помощь диетолога.
Для успешного восстановления необходим сбалансированный рацион, исключающий тяжелую пищу (жирное, копченое, сладкое и т.д.) В меню должны быть фрукты, злаковые, овощи, постное мясо. Для установления правильного режима питания бывает необходима помощь диетолога.

 Следует внимательно следить за регулярным опорожнением кишечника и мочеиспусканием; в случае проблем или задержек в выделительных процессах нужно определить причину и начать соответствующее лечение.
Следует внимательно следить за регулярным опорожнением кишечника и мочеиспусканием; в случае проблем или задержек в выделительных процессах нужно определить причину и начать соответствующее лечение. Для восстановления после инсульта особенно важно осознанное вовлечение человека перенёсшего инсульт в процесс реабилитации. Только положительный настрой самого человека перенёсшего инсульт на получение пользы от проводимых мероприятий по реабилитации позволяет добиваться наибольшего эффекта.
Для восстановления после инсульта особенно важно осознанное вовлечение человека перенёсшего инсульт в процесс реабилитации. Только положительный настрой самого человека перенёсшего инсульт на получение пользы от проводимых мероприятий по реабилитации позволяет добиваться наибольшего эффекта.